Clear Sky Science · zh
MOV10,一种新型免疫疗法靶点与预后生物标志物,通过调控自噬促进胶质瘤进展
这项脑癌研究为何重要
胶质母细胞瘤是一种侵袭性极强的脑癌,治疗非常困难。即便经过手术、放疗和化疗,大多数患者在确诊后只能活数月。该研究聚焦于一种在这些肿瘤中异常活跃的分子MOV10。研究者通过展示MOV10如何帮助癌细胞生长、躲避免疫系统并抵抗细胞死亡,指出了一个潜在的更有效治疗靶点——同时也可能成为预测患者预后的标志物。
致命脑瘤的隐秘帮手
研究团队首先挖掘了包含数百例胶质瘤患者的公共癌症数据库,这些数据库含有基因和临床信息。他们发现,参与细胞内RNA处理的蛋白MOV10在胶质瘤组织中比正常脑组织呈现更高的表达水平。肿瘤中MOV10表达较高的患者总体存活期较短,这一关联在校正了年龄、肿瘤分级和关键基因特征后仍然成立。基于这些因素,研究者构建了一个数学模型,表明MOV10水平有助于预测患者生存概率,提示MOV10可作为预后生物标志物。
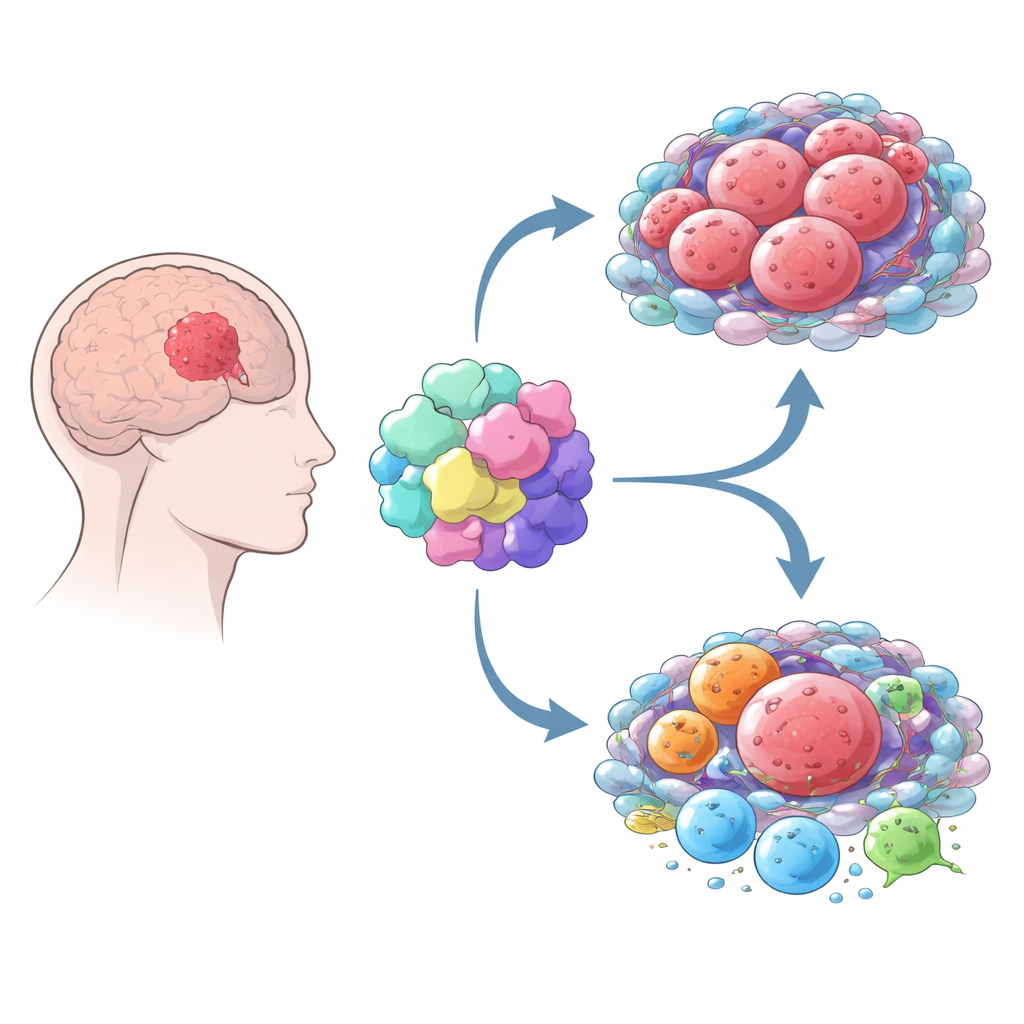
MOV10如何重塑肿瘤“邻里”
肿瘤并非孤立生长——它会劫持周围的免疫细胞和支持细胞构成的“邻里”。通过结合多种计算工具,作者显示高MOV10的胶质瘤周围比低MOV10的肿瘤富含更多种类的免疫和基质细胞。但这并非有效的免疫攻击。相反,高MOV10肿瘤含有更多巨噬细胞,尤其是通常被称为M2的亚型,这类细胞通常支持肿瘤生长并抑制免疫反应。这些肿瘤还显示出耗竭T细胞的特征增强以及免疫“刹车”通路(如PD-1和CTLA-4)活性更高。总体模式提示MOV10与一种抑制性免疫环境相关,使机体防御力被削弱。
从大数据到实验室细胞
为超越相关性,研究者在患者样本和培养细胞中直接检测了MOV10。他们证实MOV10在胶质瘤组织中比在正常脑组织更丰富,且多种常用的胶质瘤细胞系也表现出高表达。当用小干扰RNA降低培养皿中胶质瘤细胞的MOV10时,细胞分裂变慢,克隆形成减少,并且在人工膜上的迁移和侵袭能力下降。驱动细胞周期进展和侵袭的蛋白含量降低,支持了MOV10积极促进侵袭性行为而非被动存在的观点。
将MOV10与免疫细胞及自清理通路联系起来
研究还探讨了MOV10如何与两类关键过程相互作用:与肿瘤相关巨噬细胞的行为以及细胞自身的“自清洁”系统——自噬。在人体肿瘤样本中,MOV10与类似M2的巨噬细胞在同一区域共定位。在共培养体系中,当胶质瘤细胞被设计为降低MOV10表达时,迁向它们的M2样巨噬细胞更少,暗示肿瘤细胞中的MOV10有助于吸引或支持这些促肿瘤免疫细胞。与此同时,基因分析将MOV10与若干参与自噬的基因联系起来。利用可标记细胞回收结构的荧光探针,团队显示下调MOV10会增加胶质瘤细胞的自噬活性并诱发更多程序性细胞死亡。自噬和凋亡标志性蛋白的变化支持了这些观察。
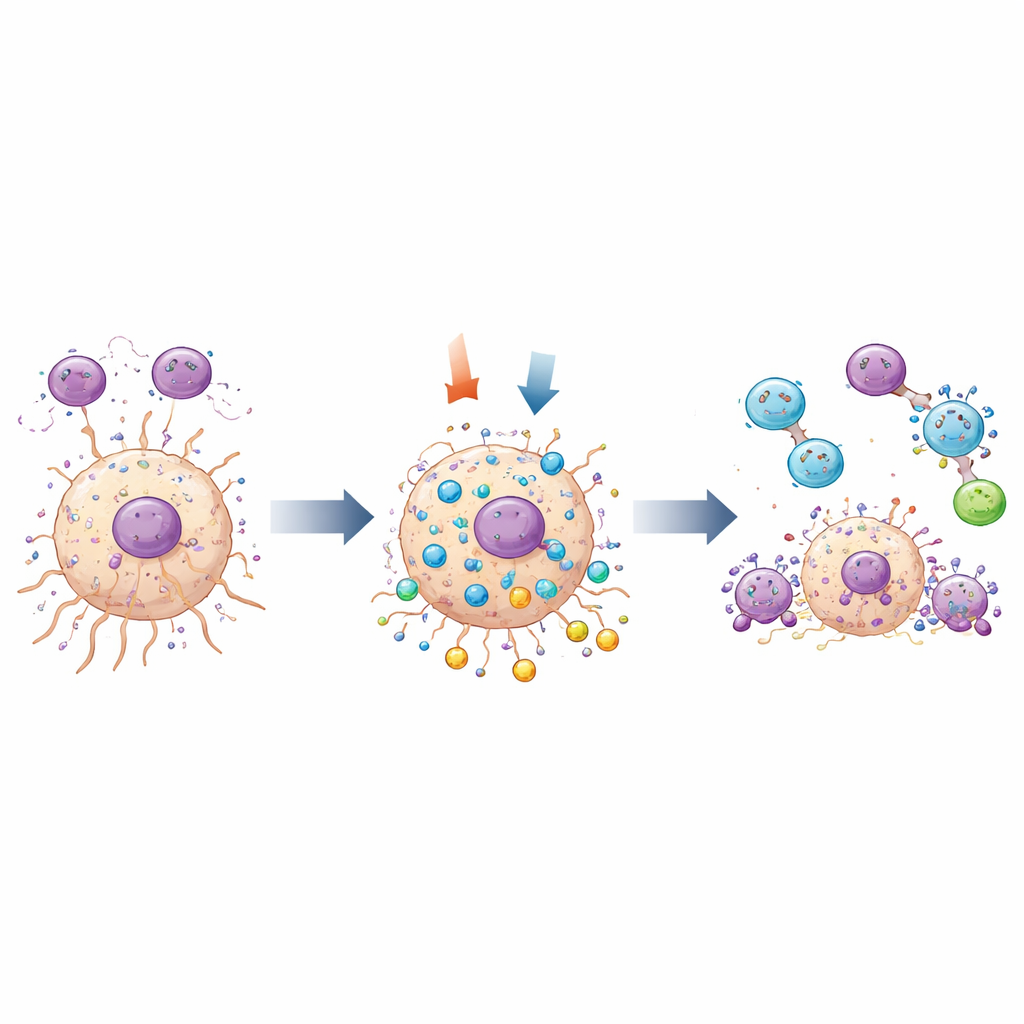
对未来治疗的意义
综合来看,研究结果将MOV10描绘成胶质瘤的多面“盟友”:它促进肿瘤细胞生长与侵袭,帮助构建富含促肿瘤巨噬细胞的免疫抑制性微环境,并抑制细胞的自毁与回收机制。当沉默MOV10时,胶质瘤细胞生长受抑、死亡增加,且似乎减少了招募有害免疫细胞类型的能力。对非专业读者而言,关键信息是:MOV10既像“温度计”又像“开关”——其在肿瘤中的水平可能有助于预测患者预后,而降低其表达理论上可使脑瘤对治疗更为敏感。尽管仍需进一步的动物研究和最终的临床试验,MOV10现在已成为对抗这一致死性脑癌的有前景的靶点之一。
引用: Wang, F., Ruan, L., Yang, W. et al. MOV10, a novel immunotherapy and prognostic biomarker, contributes to glioma development by regulating autophagy. Sci Rep 16, 9501 (2026). https://doi.org/10.1038/s41598-026-40396-8
关键词: 胶质母细胞瘤, 脑肿瘤免疫疗法, MOV10 蛋白, 肿瘤微环境, 自噬与凋亡