Clear Sky Science · zh
负载BMSCs外泌体的水凝胶促进在体大鼠肩袖损伤的修复
为什么肩部肌腱愈合很重要
肩袖撕裂是引起手臂疼痛和无力的常见原因,尤其在老年人和活跃人群中更为常见。即便通过手术将撕裂的肌腱重新固定到骨骼,愈合部位通常也以脆弱的瘢痕组织形式恢复,容易再次断裂。本研究在大鼠模型中测试了一种新策略,以增强机体自身的修复能力:一种软性水凝胶“贴片”,负载来源于干细胞的微小生物囊泡,旨在帮助肌腱更强、更接近原始结构地再生。
小囊泡,大修复潜能
研究者关注的是外泌体——由骨髓干细胞自然释放的微小囊泡。这些囊泡携带蛋白质和遗传物质,能够影响附近细胞,像分子明信片一样指示组织如何生长和修复。研究团队没有移植完整的干细胞(这可能带来安全问题),而是从大鼠干细胞培养物中提取外泌体,确认其大小和结构,然后将其混入一种名为GelMA的明胶基水凝胶中。该材料可以注射为液体,并通过光照快速固化,形成稳定的局部储库,在损伤部位缓慢释放外泌体。
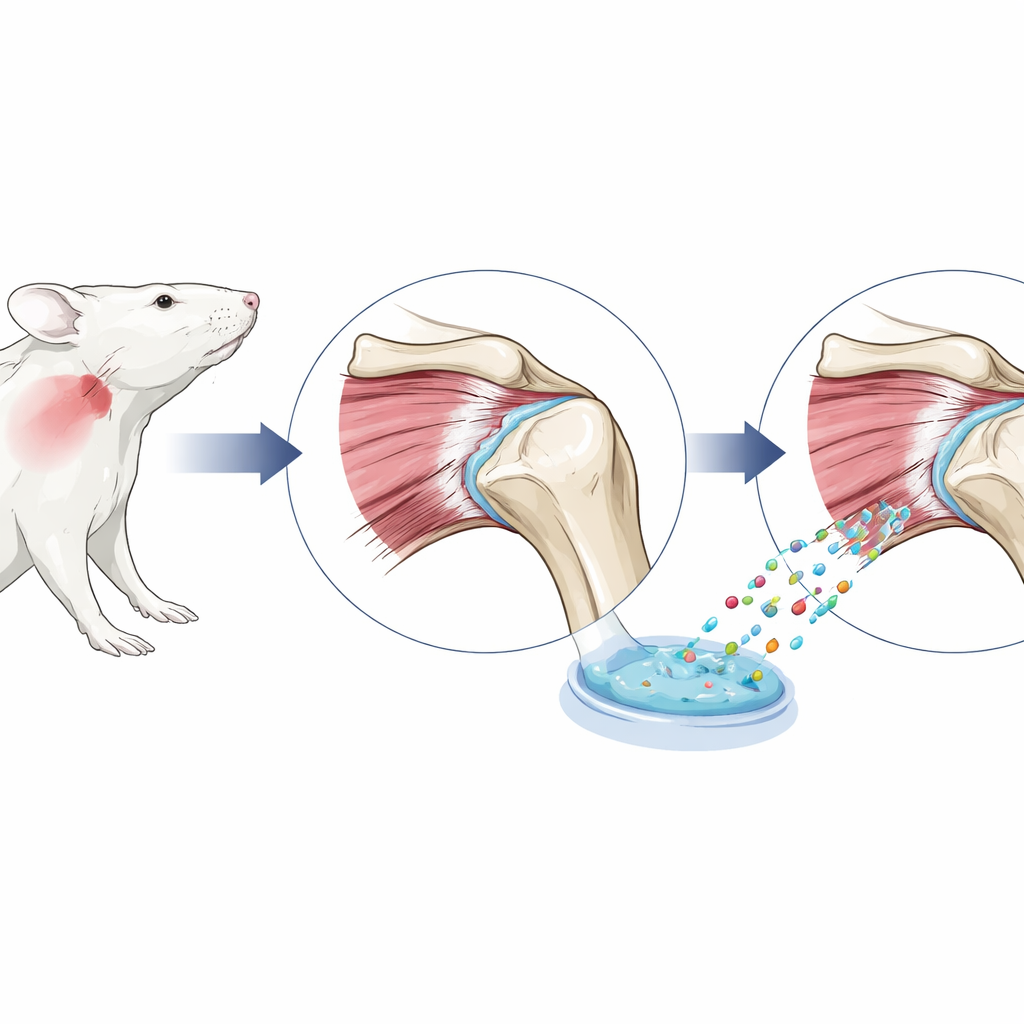
用于肩袖修复的大鼠模型
为了模拟人类肩袖手术,科学家在大鼠中外科性分离并修复了一条关键的肩部肌腱。动物被分为若干组:有的仅接受标准修复;有的仅注入空白水凝胶;有的接受负载干细胞外泌体的水凝胶;另一组接受相同的外泌体水凝胶并同时给予一种可阻断TGF-β1信号分子的药物。另设一组健康、未受伤的大鼠作为基线。术后六周,研究团队通过测量力学强度、显微镜下检查组织结构以及分析与肌腱和肌腱-骨愈合相关的基因活性来评估修复效果。
更强且组织更有序的修复
接受外泌体负载水凝胶处理的大鼠,其肌腱修复在力学性能上更接近正常健康肩部。肌腱-骨连接的最大承载力和刚度均显著高于标准修复或空白水凝胶组,并且与未受伤对照相似。显微镜下,外泌体组在肌腱-骨界面显示出更致密、连续且更平行的胶原纤维,血管和炎性细胞较少——这些特征更接近天然、良好整合的连接,而非脆弱的瘢痕组织。区分不同胶原类型的染色显示,该组的胶原构成比例趋近于正常组织。
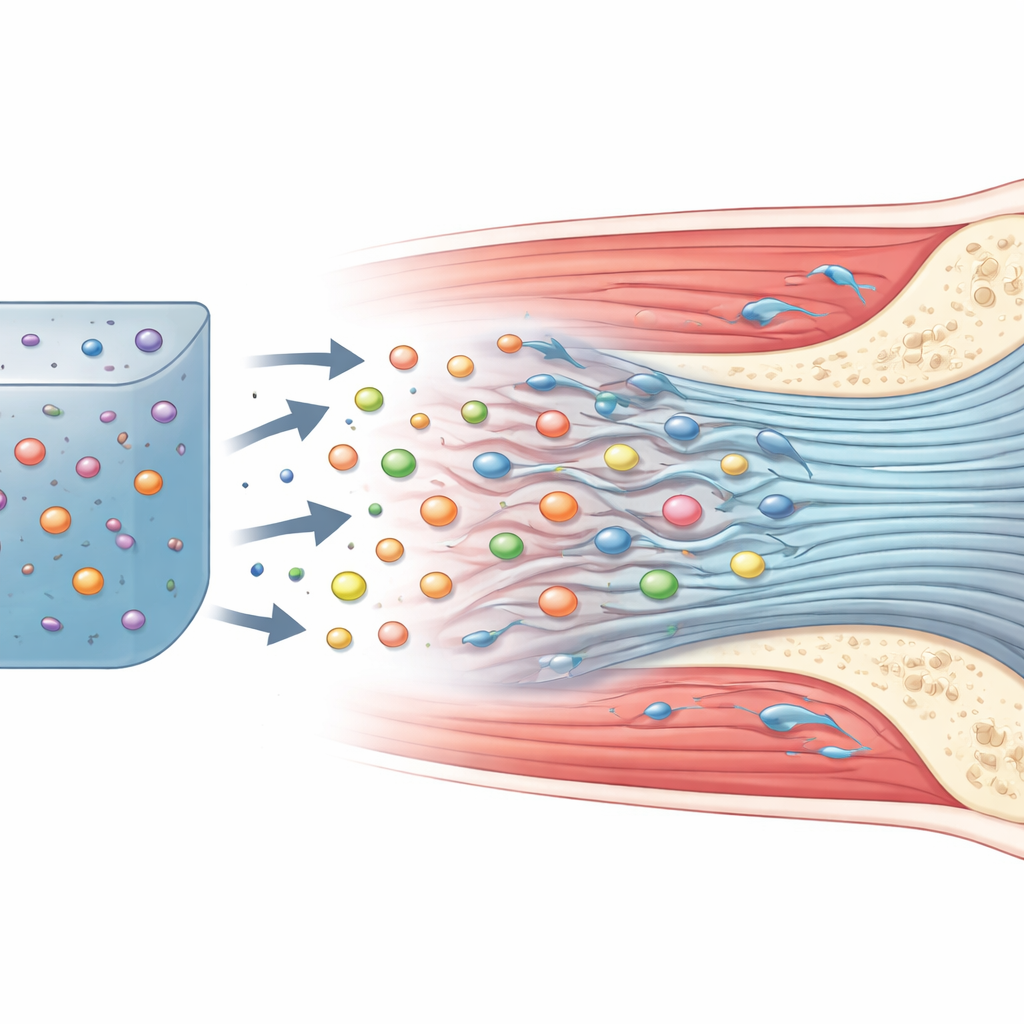
关键的信号通路在发挥作用
为弄清外泌体的作用机制,团队测量了若干与肌腱结构和愈合相关基因的表达。在外泌体组中,与强韧肌腱基质、肌腱细胞表型和组织重塑相关的标志物均较其他处理组升高。当化学阻断TGF-β1通路时,这些益处在很大程度上消失:力学强度下降,胶原组织结构变差,愈合相关基因的活性降低。这提示外泌体部分通过增强TGF-β1信号来发挥作用,促进愈合界面的细胞增殖和胶原生成。
这对患者意味着什么
简单来说,这项大鼠研究表明,来源于干细胞的外泌体水凝胶贴片可以帮助外科修复的肩部肌腱更有力且更有序地重新连接到骨骼,并且TGF-β1这一关键信号在该效应中起核心作用。在该策略能用于人类患者之前还需大量工作——包括长期安全性评估和更大动物的试验——但这一方法指向了未来肩部手术的新方向:外科医生不仅缝合撕裂组织,还可能递送一种有针对性的、无细胞的“药物”,以悄然引导机体重建更自然、更耐用的肌腱-骨连接。
引用: Peng, K., Wang, S., Li, J. et al. Bmscs loaded exosome hydrogel promotes the repair of rotator cuff injury in rats in vivo. Sci Rep 16, 9447 (2026). https://doi.org/10.1038/s41598-026-40392-y
关键词: 肩袖修复, 外泌体水凝胶, 骨髓间充质干细胞, 肌腱愈合, TGF-β信号通路