Clear Sky Science · zh
反复植入失败患者子宫内膜受容性变化期间的可变剪接和差异基因表达
为什么有些胚胎无法着床
许多接受体外受精的夫妇面临一个令人沮丧的谜题:即便移植了高质量胚胎,仍可能无法怀孕。本研究聚焦于子宫内膜——子宫的黏膜层,旨在理解为何一些女性会反复发生着床失败。通过检查基因如何开启或关闭、它们的转录本如何被剪切与重排,以及在子宫短暂准备接受胚胎的窗口期内免疫细胞如何表现,研究揭示了新的分子线索,未来可能指导更精确的检测与治疗。
子宫短暂的“欢迎”窗口
着床只能在每个周期的一个短时段内发生,此时子宫内膜变得“受容”。研究者比较了90例有生育史女性与73例反复植入失败女性的组织样本,均在三个关键时间点取得:在内膜变得受容之前、受容窗口期以及窗口关闭后不久。利用高通量RNA测序,他们测量了哪些基因处于活跃状态以及这些基因的RNA信息如何被处理。该设计使他们能够追踪健康内膜如何为胚胎做准备,以及在有反复着床失败的女性中这种准备如何出错。 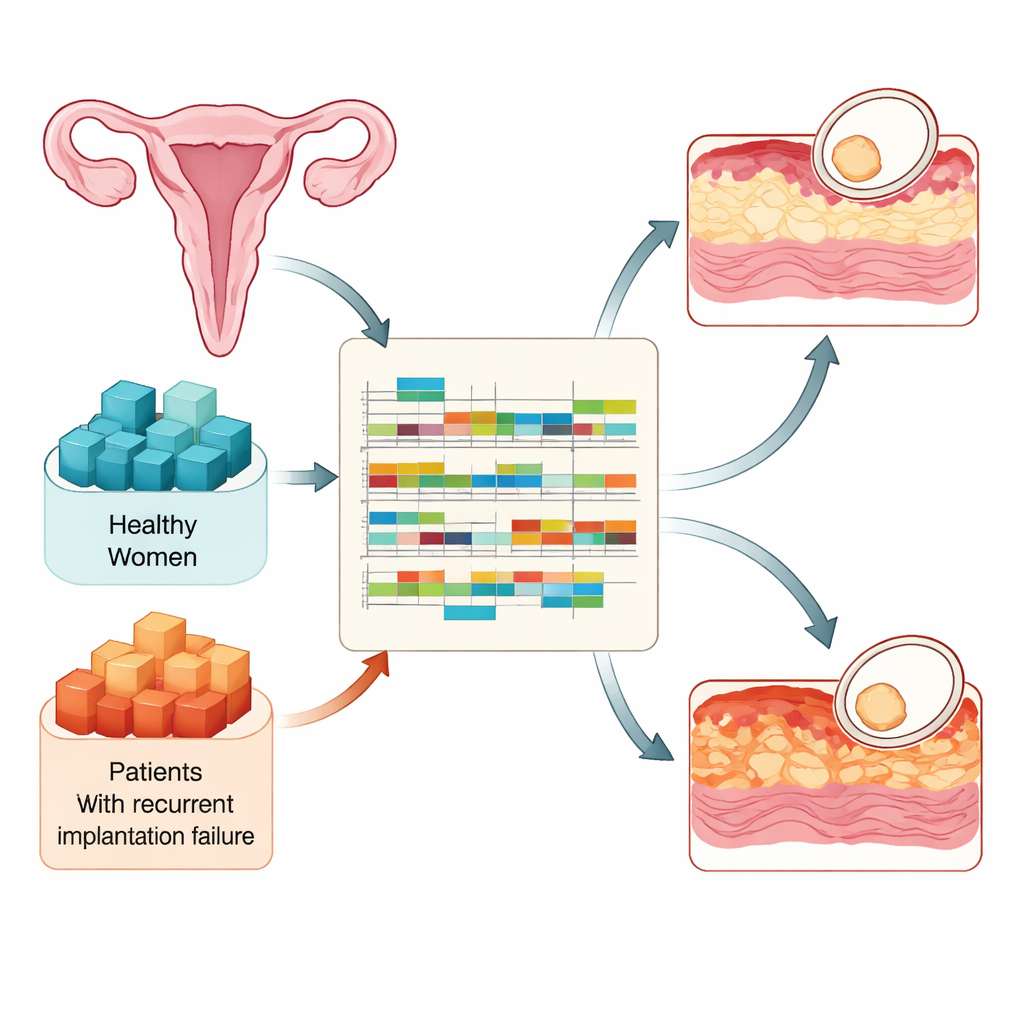
基因信息的剪切与重排
除了简单统计每个基因有多少表达外,团队还着重研究了可变剪接——单个基因如何被剪成不同的转录本变体,从而产生不同的蛋白形式。他们在若干比较中发现了超过一百万次的剪接事件,其中两类——整段跳过和互斥外显子选择——尤其常见。当只考虑既频繁又统计学上稳健的改变时,他们观察到数百到数千处剪接改变,主要发生在内膜从非受容期向受容期转变过程中,尤其是从早期(预受容期)进入着床窗口时。许多这些变化发生在基因总量不变的情况下,这意味着蛋白的形式发生了改变而基因总体活性并未变化。
细胞黏附、重塑与免疫交流
受剪接改变和表达变化影响的基因大量参与细胞如何相互黏附、细胞内部支架如何重组以及它们如何发送和接收免疫信号。这些功能在子宫内膜从单纯屏障转变为能够欢迎并锚定胚胎、同时重塑血管的表面时至关重要。在有生育能力的女性和发生植入失败的女性中,受容期都伴随着这些通路的强烈重塑,但反复失败的女性往往表现出更频繁或模式不同的剪接改变。其中一些基因已被建议作为理想着床窗口的标记,这强化了这样的观点:不仅基因的活性重要,其产物的精确形式也决定了内膜何时真正准备就绪。
免疫细胞与一个关键的剪接调控因子
研究团队还从相同的RNA数据中推估了组织中存在的免疫细胞类型。在植入失败的女性中,受容期相比早期表现出更少的杀伤性T细胞和静息的自然杀伤细胞,但单核细胞和某些巨噬细胞增多。随后,窗关闭后,模式再次发生变化,表现为活化的自然杀伤细胞和巨噬细胞亚型的改变。其中若干免疫细胞的变化与特定的剪接事件紧密一致,提示基因信息重塑与免疫平衡之间存在联系。在控制剪接的蛋白中,一种名为KHDRBS3的蛋白作为中心枢纽显著突出,与许多改变的事件相连,并且在内膜变为受容时无论在有生育能力的女性还是受影响女性中水平均一致下降。这暗示它可能有助于驱动伴随着床窗口开启而发生的剪接模式转换。 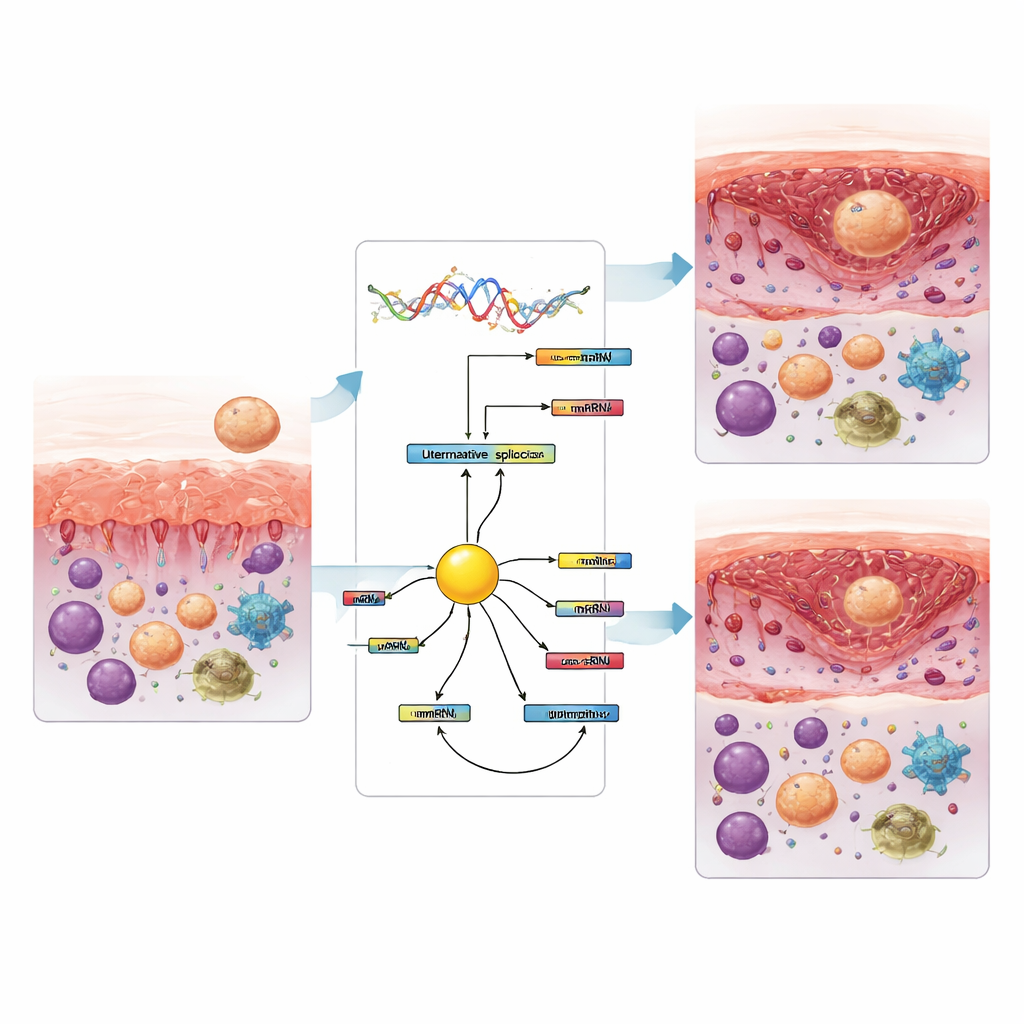
指向未来的检测与治疗
为了将这些分子模式转化为潜在疗法,研究者询问现有的小分子药物是否可能逆转他们观察到的异常剪接特征。通过将他们的基因列表与大型药物反应数据库匹配,他们鉴定出若干获批或在研的化合物,这些药物靶向与着床相关的基因,包括影响免疫反应或激素相关通路的制剂。虽然这些距离在临床上用于该情境尚有很大距离,但为实验室测试提供了起始路线图。
这对患者意味着什么
总体而言,该研究表明,着床失败并非只是“错误”基因的问题,而是这些基因如何被编辑成不同的信息以及子宫内环境的免疫调控如何随时间调整。研究强调了KHDRBS3及相关因子作为这一过程有前景的调控者,并揭示了可能支持或阻碍胚胎着床的协同免疫细胞变化。从长远看,这些见解可能促成更精细的检测,确定女性受容窗口的真正时间和质量,以及针对性地调整基因信息或免疫平衡的治疗,以提高胚胎着床的成功率。
引用: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
关键词: 子宫内膜受容性, 反复植入失败, 可变剪接, 子宫免疫细胞, 辅助生殖