Clear Sky Science · zh
曲氏胞苷联合针对CD13的组织因子tTF-NGR治疗晚期复发或难治性软组织肉瘤:转化数据、临床安全性与疗效
这项研究为何重要
晚期软组织肉瘤患者——这类罕见癌症发生于肌肉、脂肪或其他支撑组织——常常面临有效治疗选项耗尽的困境。本研究探讨了一种新的两步给药策略,旨在将现有的化疗药物困留于肿瘤内并切断肿瘤的血供,期望在控制病情的同时保持可控的副作用。
一种需要更好选择的罕见癌症
软组织肉瘤仅占成人癌症的约1%,但一旦转移或无法手术切除,常表现为侵袭性强。标准化疗可延缓肿瘤进展,但晚期患者的生存仍然较差。曲氏胞苷是第一线治疗失败后常用的药物之一,其作用包括损伤癌细胞DNA并影响肿瘤微环境中的细胞。然而,许多肿瘤最终仍会复生,这促使研究者寻找在不大幅增加患者伤害的前提下增强其疗效的方法。
针对肿瘤的两步“陷阱”
研究团队测试了他们称为“曲氏胞苷陷阱”(TRABTRAP)的概念。首先,患者接受为期24小时的曲氏胞苷静脉输注。随后两到三天,他们接受第二种药物tTF-NGR。这种工程化蛋白能定位到主要存在于肿瘤供血血管上的标记物CD13。当tTF-NGR依附于这些血管时,会触发局部凝血并阻断血流,导致肿瘤部分坏死。其构想是先给予曲氏胞苷使其渗入肿瘤,然后通过tTF-NGR关闭肿瘤微血管的“出口”,将药物困留在最需要的部位,从而放大两种治疗的协同效果。
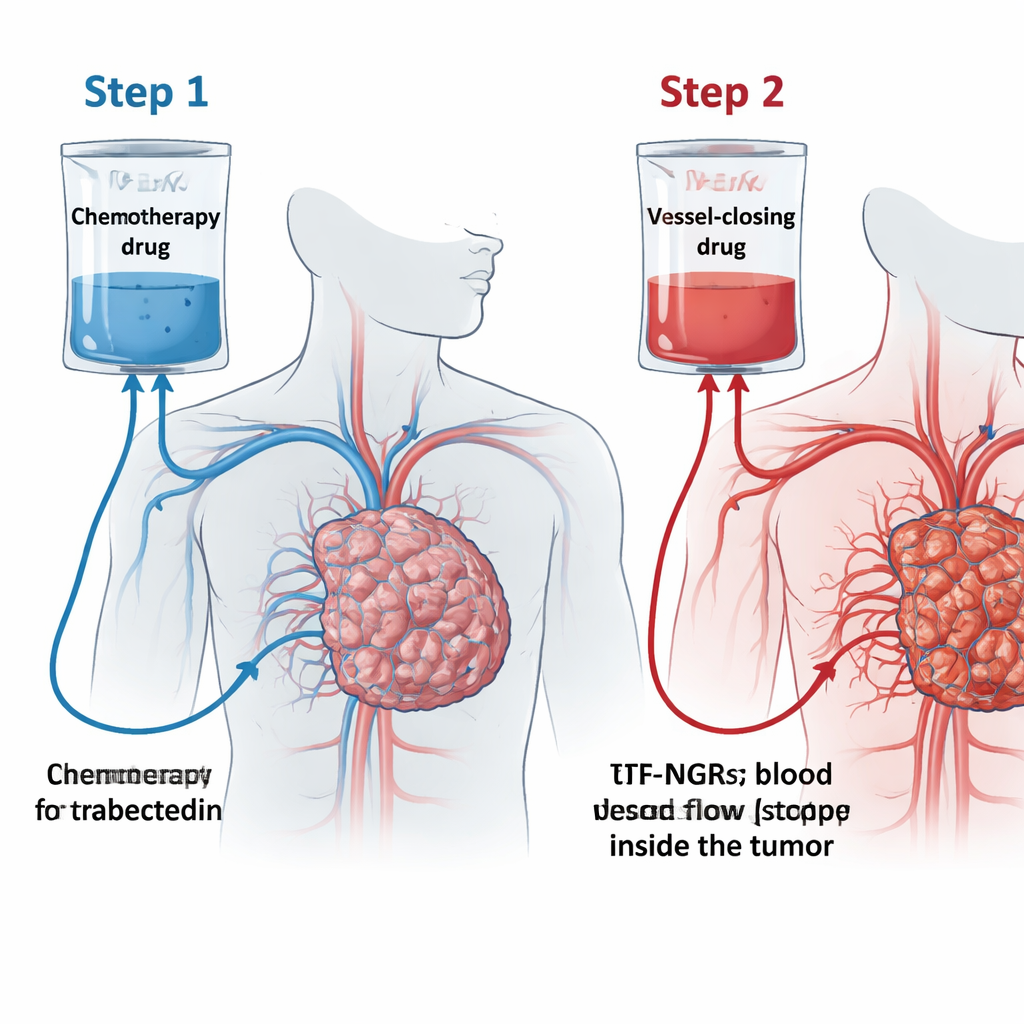
从实验室到早期患者试验
在实验室实验中,研究者发现曲氏胞苷使血管内皮细胞和肉瘤细胞在表面呈现更多的一种支持凝血的脂类分子。这一改变使tTF-NGR在这些细胞上触发局部凝血的效果更佳,正是关闭肿瘤血管所需的作用。在携带人源肉瘤的鼠模型中,先用曲氏胞苷再用tTF-NGR的给药顺序比单药更能缩小肿瘤。由于动物模型中肿瘤在联合治疗下坏死得很彻底,团队无法可靠测量被困留的曲氏胞苷量,但更强的肿瘤控制支持了“陷阱”这一基本构想。
在真实患者中寻找安全剂量
本文的核心是TRABTRAP试验在19名晚期、既往治疗充分的软组织肉瘤患者中进行的安全性“运行期”。所有患者都接受了标准剂量的曲氏胞苷。第二种药物tTF-NGR从此前单药使用时可耐受的最高剂量开始,当出现严重不良反应时则谨慎降量。在较高剂量下,一些患者出现了明显的心脏相关或凝血问题,例如血液检测提示的无症状心肌损伤、小肺栓塞或深静脉血栓。这些事件在停用或减少tTF-NGR并给予相应治疗后可逆,但提示需要采用更低剂量。在曲氏胞苷给药后两天内每次0.5 mg/m²的tTF-NGR方案下,六名患者至少完成了两周期且未出现剂量限制性毒性,有些患者甚至持续治疗达14个周期。
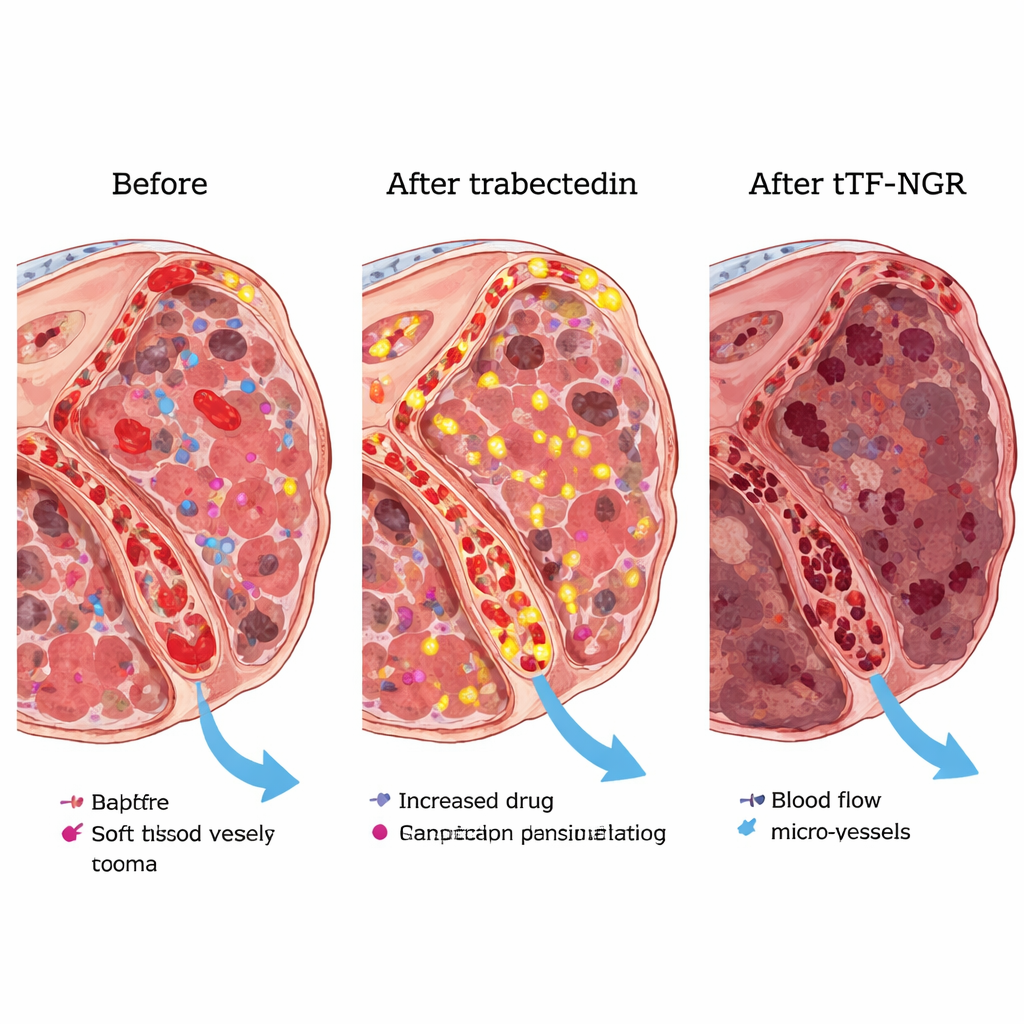
早期获益迹象与药物相互作用
尽管该部分研究规模太小,无法证明疗效,但结果令人鼓舞。在19名患者中,大多数人在一定时间内实现了疾病控制,其中两例出现明确的部分肿瘤缩小。在对曲氏胞苷常见敏感的脂肪肉瘤或平滑肌肉瘤患者中,近三分之二在首次主要评估时表现为疾病稳定或部分反应。一名患者的详细MRI显示,所选剂量的tTF-NGR能够选择性地减少肿瘤灶内的血流。血液检测显示,在曲氏胞苷之后使用时,tTF-NGR在血液中停留时间更长且表现出更强的活性,这有助于解释为何联合使用时的安全剂量低于单药使用时的剂量。
对患者意味着什么
对于面临晚期软组织肉瘤的患者,TRABTRAP代表了一种精心设计的尝试,通过将现有化疗与靶向闭合血管的剂联用以增强疗效。安全性运行期显示,在调整剂量后,该组合可以重复给药,副作用虽显著但在密切监测下总体可管理且可逆。尽管尚不能断言其能延长生存或持续性缩小肿瘤,但早期令人鼓舞的疾病控制和对肿瘤血流的明确影响支持继续推进至更大规模、随机对照的试验。如果未来结果积极,这一两步策略可能为肉瘤治疗开辟新途径,并可能激发针对其他难治肿瘤的类似策略。
引用: Hessling, K., Brand, C., Schwöppe, C. et al. Trabectedin plus CD13-targeted tissue factor tTF-NGR against advanced relapsed or refractory soft tissue sarcoma: translational data, clinical safety and efficacy. Sci Rep 16, 7389 (2026). https://doi.org/10.1038/s41598-026-40362-4
关键词: 软组织肉瘤, 曲氏胞苷, 肿瘤血管, 靶向凝血治疗, 联合化疗