Clear Sky Science · zh
基于凝集素的原生糖RNA检测与表达谱分析
RNA 穿上糖衣
我们的细胞携带大量RNA分子,最广为人知的是作为将基因信息转化为蛋白质的信使。近年来,科学家发现了一个令人意外的转折:一些RNA上装饰着复杂的糖链,甚至出现在细胞外。这些“带糖”的RNA,被称为糖RNA,似乎影响免疫细胞的迁移、癌症的扩散以及机体对感染的反应。本文所述研究引入了一种更简便的方式来识别这些难以捉摸的分子,并绘制了它们在体内出现的位置图谱,为新的诊断和治疗开辟了道路。
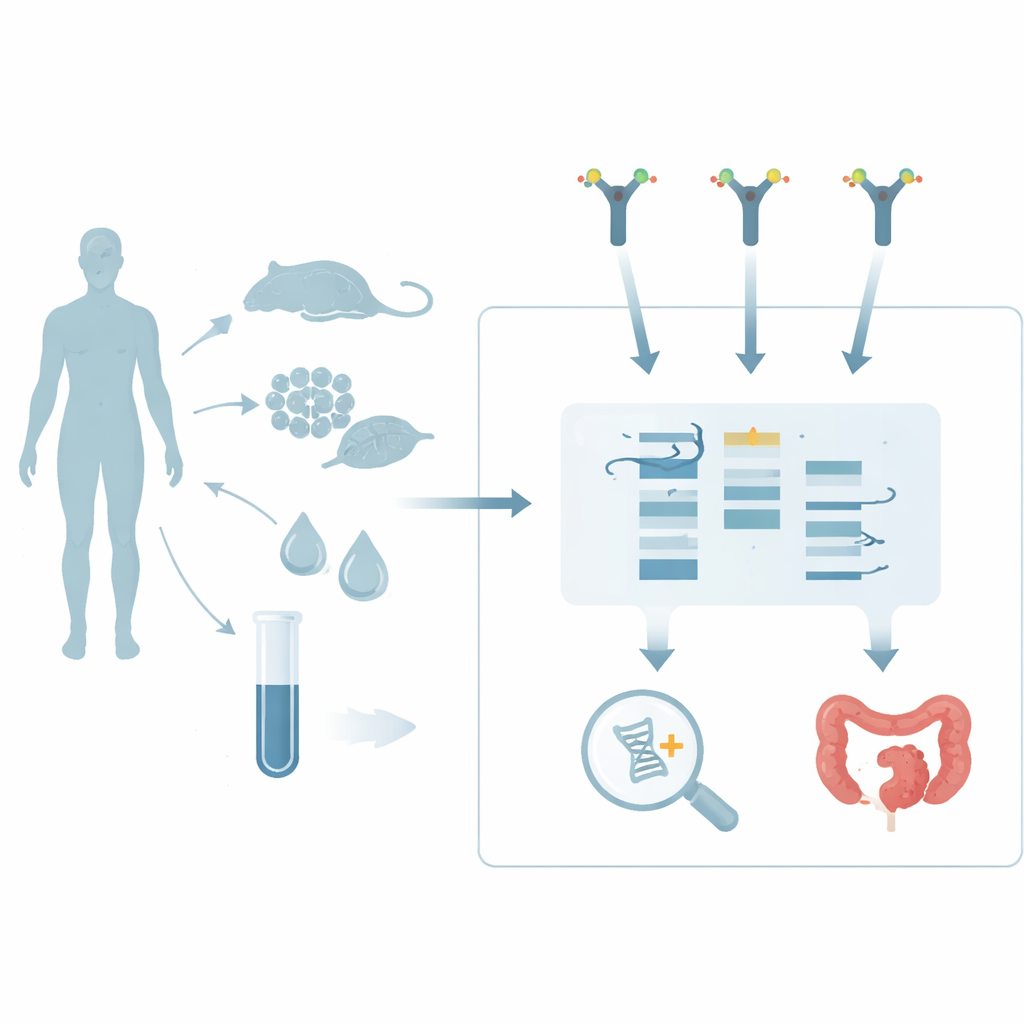
识别带糖RNA的新方法
迄今为止,发现糖RNA一直需要技术要求较高的方法。一种做法是让活细胞或动物摄取人工糖构件,这些构件随后出现在新合成的糖链上,随后可以被标记并可视化。另一种称为rPAL的方法,会在纯化的RNA某些糖上进行化学改造,从而使其可被检测。这两种策略都具灵敏性,但各有缺点:一种依赖能吸收探针的活体系,另一种仅能识别带有特定糖末端的一部分糖RNA。本文作者开发了一种更直接的替代方法,可直接作用于提取的RNA。他们的方法——基于凝集素的检测(LBD)——依赖凝集素这类天然蛋白识别特定的糖形状,在印迹膜上结合糖RNA,类似于抗体识别蛋白质。
微调简洁的实验流程
为建立LBD,团队首先从培养的人类单核细胞中分离总RNA,并用常规的北方印迹方法按大小分离分子。随后他们测试了24种不同的凝集素,评估其突出显示特定糖RNA条带的能力,并将结果以rPAL作为参照进行比较。若干凝集素有效,但一种来自番茄的凝集素LEL显示出尤其强的信号,成为他们的首选探针。研究者随后优化了常规步骤——如何将RNA转移到膜上、选择哪种膜材料、如何阻断背景结合、孵育时间以及凝集素用量——直到信号既清晰又可重复,同时保持协议足够简单,便于典型分子生物学实验室执行。
验证灵敏度、特异性及所见对象
一个关键问题是LBD是否既灵敏又真正特异于糖RNA。通过在不同RNA量下将LBD与代谢标记和rPAL并列比较,作者发现LBD可检测到大约半微克的总RNA,灵敏度与已建立的方法相当。为测试特异性,他们用酶处理样品:切割RNA、DNA、蛋白质或切除修饰糖链的N-连接糖。只有破坏RNA本身或去除其糖链的处理会消除信号,而切割DNA或消化蛋白的酶处理则无影响。阻断细胞内糖链组装的药物也显著降低了LBD信号。综上,这些检验表明凝集素方法确实响应糖修饰的RNA,而不是污染物。
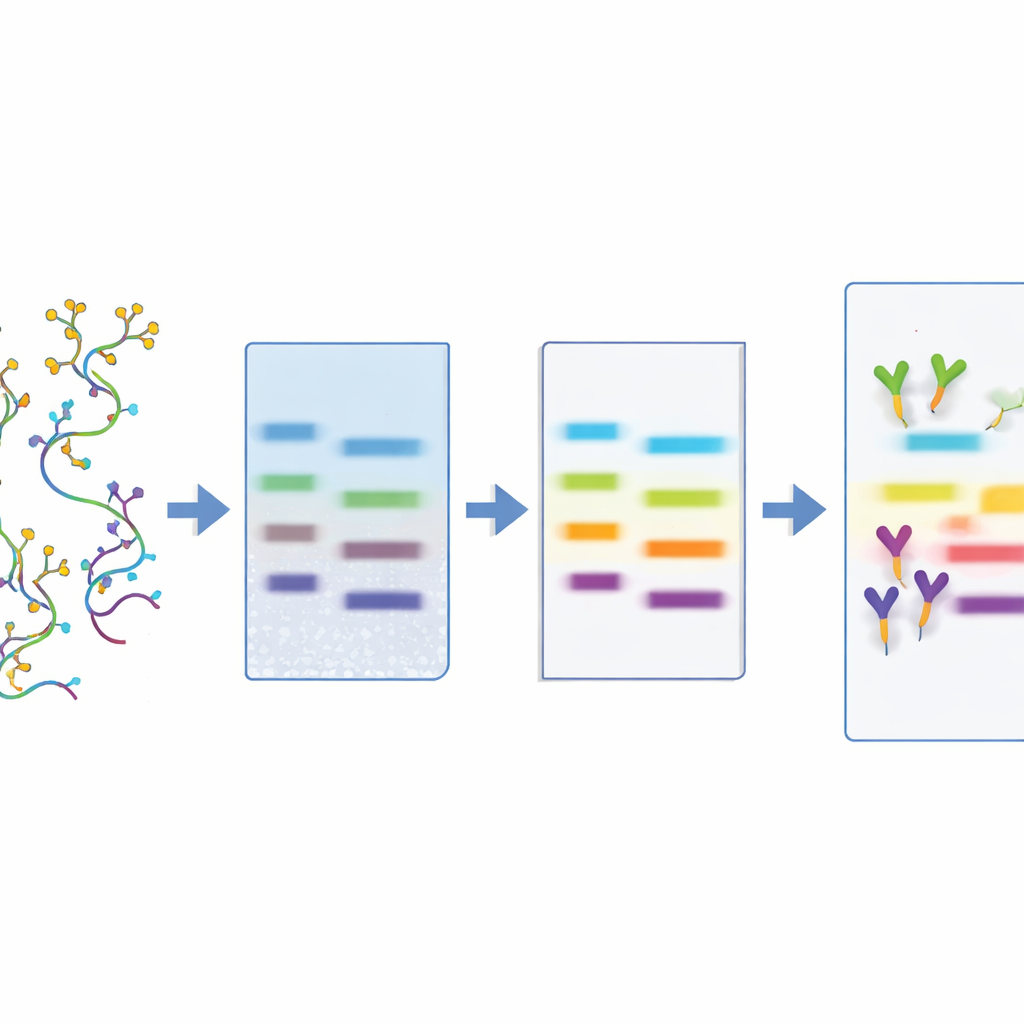
带糖RNA在健康与疾病中的分布
有了该方法,团队在来自小鼠、大鼠和人类的多种细胞、组织和体液中调查了糖RNA的出现情况。他们在免疫相关细胞(如单核细胞、中性粒细胞和白细胞)、形成外界屏障的器官(如肠道和呼吸道)以及某些脑区和心脏地区检测到特别强的信号。有趣的是,在一些主要器官(包括肝、肾和骨骼肌)中,糖RNA缺失或含量很低。LBD还在某些组织中显示出多个条带,不同凝集素识别到不同子集的条带,提示存在多样的糖RNA“口味”,具有不同的糖修饰。重要的是,作者在人体血浆、尿液、粪便和羊水中检测到游离的糖RNA,暗示这些分子可以在细胞外循环,并可能通过相对非侵入性的检测进行采样。
与癌症的关联及未来医疗用途
研究还探讨了糖RNA模式在癌症中的变化。在配对的人体组织样本中,乳腺癌和结肠癌组织显示出比正常组织更高水平的糖RNA,且在转移性疾病中信号最强。在转移性乳腺癌中,糖RNA条带在凝胶上的迁移模式与原发肿瘤不同,提示可能存在与疾病进展相关的结构变化。这类与肿瘤相关的变体最终可能有助于区分侵袭性癌症或指导靶向治疗。因为LBD使用易得的试剂并避免了活体标记步骤,它为筛查大量样品并跨方法比较提供了实用途径,揭示了不同检测策略所强调的糖RNA集合既有重叠也不完全相同。
对日常健康的重要性
简而言之,这项工作提供了一套工具,可以识别一类新近被认识的生物分子,这些分子帮助细胞相互交流,尤其是在免疫系统以及直接接触微生物和毒素的体表。通过展示一种简单的糖结合探针能够可靠地在组织、体液和肿瘤中揭示糖RNA,该研究为将这些分子转化为炎症、感染或肿瘤扩散的指示剂奠定了基础。尽管仍需要更灵敏的临床检测和更深入的功能研究,基于凝集素的检测大大降低了许多实验室探索糖RNA分布及其在健康与疾病中作用的门槛。
引用: Li, Y., Qian, Y., Li, X. et al. Lectin-based detection and expression profiling of native glycoRNAs. Sci Rep 16, 9031 (2026). https://doi.org/10.1038/s41598-026-40291-2
关键词: 糖RNA, 基于凝集素的检测, 细胞表面RNA, 生物标志物, 癌症转移