Clear Sky Science · zh
用于基于原型的可解释数字病理学有丝分裂检测的自适应样本选择
这对癌症护理为何重要
病理学家在显微镜下观察癌组织样本时,统计正在分裂的肿瘤细胞数量有助于判断癌症的侵袭性并选择治疗方案。人工智能现在可以在数字切片中快速识别这些分裂细胞,但其决策过程常常对专家而言是个谜。本文提出了一种称为自适应样本选择(AES)的方法,使得人工智能系统能通过指向支持或反驳每个判断的真实既往病例来“展示其推理”,从而使自动化的有丝分裂检测更具透明性并在临床上更值得信赖。
识别分裂细胞的挑战
正在分裂的肿瘤细胞(称为有丝分裂像)体积小、稀少且外观多样。在常见的紫红色染色下,它们可能与无害结构(如正在死亡的细胞或某些免疫细胞)非常相似。人工专家必须在巨大的数字切片中逐一查找,这一过程既缓慢又易疲劳且主观性强。现代深度学习系统在这项任务上可以达到或超过专家水平,但它们行为如同黑箱:对每个疑似细胞给出一个分数,却没有清晰解释其依据。在医学领域,治疗决策可能改变生命,这种缺乏透明性成为将人工智能纳入日常临床实践的重大障碍。
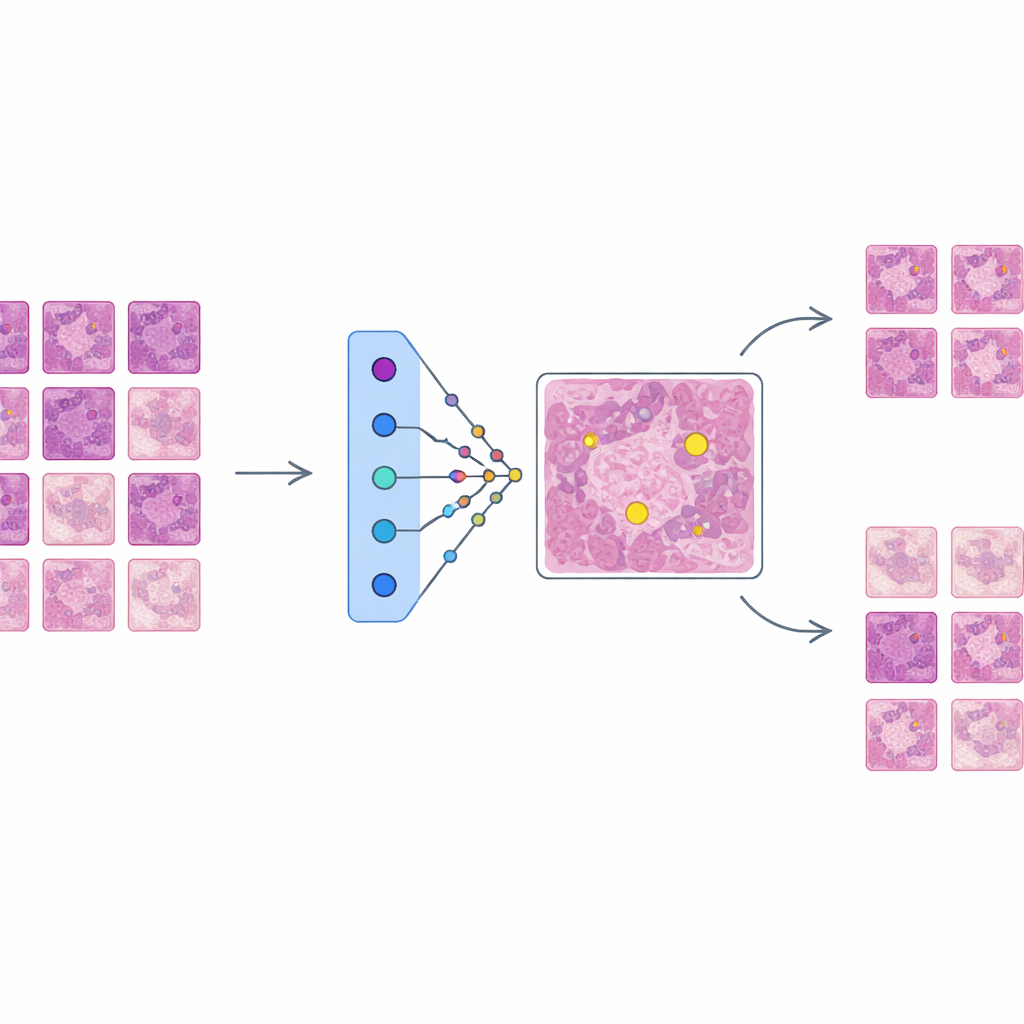
构建强大但不透明的检测器
作者首先训练了一个基于 Faster R-CNN 架构的最先进目标检测网络,在一个名为 MIDOG++ 的大规模多样化数据集中寻找有丝分裂像。该数据来自人类与犬只肿瘤、多个癌种和不同实验室,包含超过一万一千个经过仔细标注的分裂细胞。为保留细微结构,切片被分割成小图像块并进行大量增强,以模拟染色和成像的现实变化。所得检测器在多种肿瘤类型上取得了稳健的性能,F1 分数高达 0.84,证明其准确但复杂——正是那类在临床中需要更好解释的系统。
教会 AI 用示例自我阐释
AES 作为解释层叠加在已训练的检测器之上,而不是改变检测器本身的工作方式。对于检测器标记为可能有丝分裂的每个候选区域,AES 会在训练数据中构建的真实组织图像库中查找。从该库中,它选择一小组“支持性”示例(与真实有丝分裂相似)和一组“反驳性”示例(更像非有丝分裂细胞)。在幕后,AES 将检测器的置信度视为一片平滑景观,并使用径向基函数等数学工具来近似该置信度在局部的变化。只有那些对局部置信度有实质影响的原型会被保留,因此单个决策的解释通常涉及大约十个精心挑选的示例,而不是数百个几乎无关的例子。
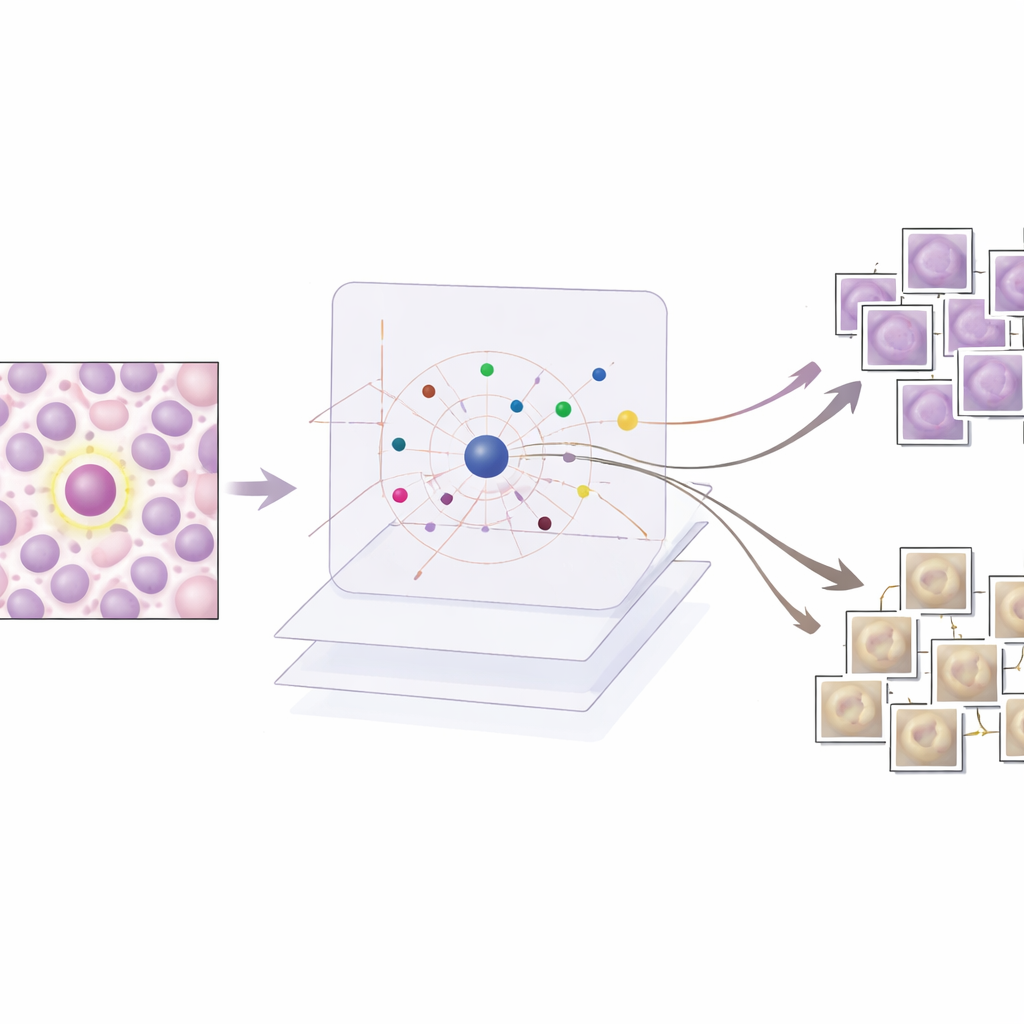
这些示例揭示了 AI 的决策
研究者从定量和定性两方面评估了 AES。定量上,他们展示了大约 190 张原型图像的紧凑字典就能非常准确地模拟检测器的置信度,同时每例显示的示例数量低到足以供人工审阅。定性上,他们检查了三种常见情形。当检测器明显正确时,AES 仅返回强力支持决策的有丝分裂原型,这令临床人员放心。对于误报,该方法呈现出误导检测器的相似质地或染色模式的类有丝分裂示例,通常还伴随若干较弱的非有丝分裂原型,提示不确定性。对于漏检的有丝分裂,AES 往往主要返回非有丝分裂或模糊示例,指向训练数据中的盲点并提示需要新增或更好标注的样本。
从黑箱到协作工具
通过将每个预测绑定到少数真实、已标注的组织图像块,AES 让复杂的 AI 检测器更像一位以既往病例为依据来证明自己决策的人类同事。该系统不仅报告某个细胞是否可能在分裂,还通过支持与反驳原型的组合与影响力显示其原因及置信度。这一设计让病理学家能够快速确认强有力的预测,集中注意力于边界或令人困惑的区域,并识别可指导后续训练的系统性错误模式。尽管该方法为有丝分裂检测而开发,但相同思路可扩展到数字病理学的其他任务,推动人工智能从不透明的自动化走向可质询、可信赖并可被临床人员不断完善的基于病例的辅助系统。
引用: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
关键词: 可解释人工智能, 数字病理学, 有丝分裂检测, 基于原型的模型, 癌症诊断