Clear Sky Science · zh
通过甘露糖受体选择性清除单克隆抗体取决于糖链配对
为什么药物上的糖模式很重要
当今许多重磅药物是单克隆抗体——可在血液中停留数周并能精确靶向癌症和自身免疫性疾病等病症的工程化蛋白质。但注射后并非所有抗体的行为都相同。本研究提出了一个看似简单却后果重大问题:附着在抗体上的精细“糖模式”如何决定机体清除它的速度?这是否也会影响诸如免疫反应之类的副作用?
微小糖链作为交通信号
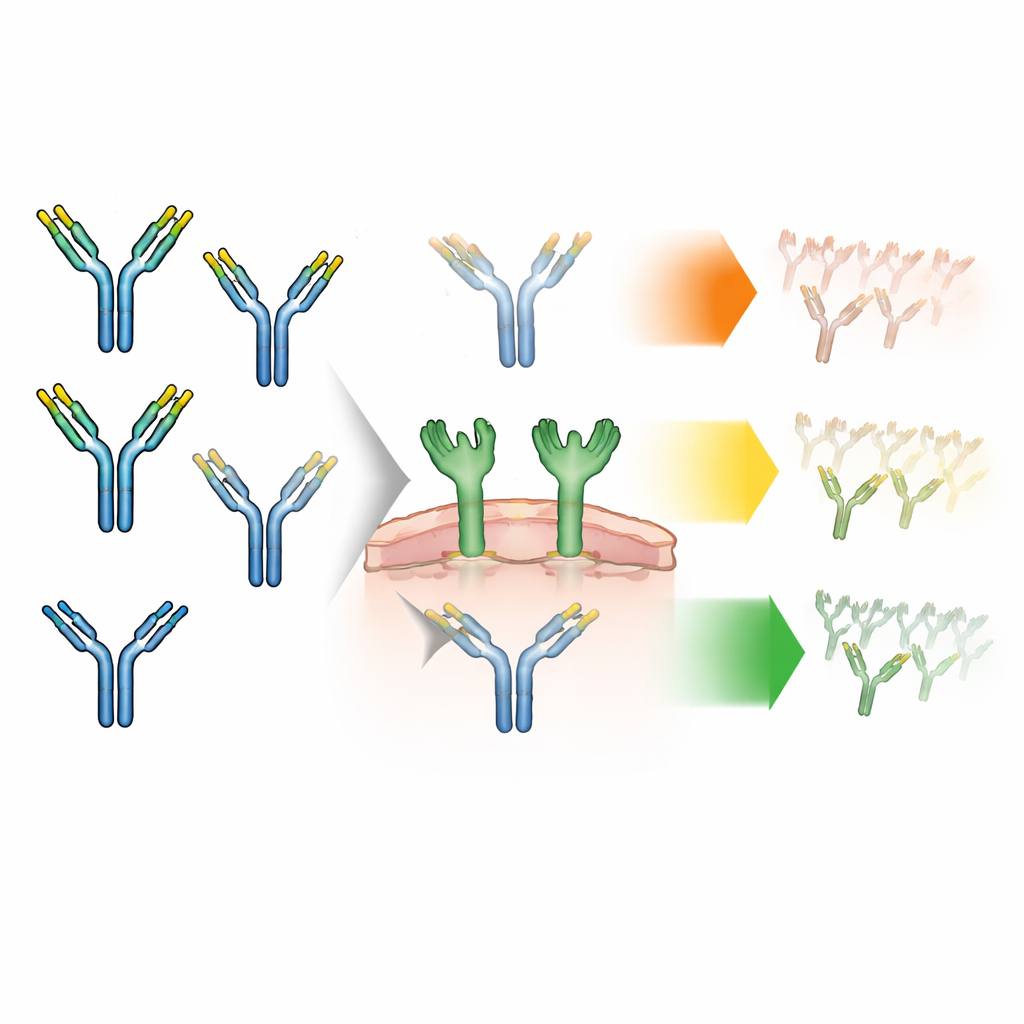
抗体天然在其主链上携带称为糖链的小型糖链。这些糖链有不同类型。大多数是“复杂型”构型,但少数是“高甘露糖型”,这是一种更简单的类型,以往研究将其与更快的血液清除相关联。每个抗体有两个作为一对的糖修饰位点,这两个位点可以相同(对称配对)或不同(非对称配对)。直到现在,药企通常只统计总体上每种糖型的含量,而不去考察同一抗体上两个糖是如何配对的。作者怀疑,这种配对模式可能改变抗体与免疫细胞上一个特殊糖识别蛋白——甘露糖受体——的相互作用强度,从而影响药物被清除的速度。
按糖对对抗体进行分拣
为此,研究团队工程化获得富含高甘露糖的抗体,然后将它们物理分离为三类主要组别:带有两个复杂型糖的抗体、一个复杂型和一个高甘露糖(非对称)以及两个高甘露糖(对称)。他们仔细验证了这些组在其他方面几乎一致:尺寸、形状、电荷和稳定性相同,并且与通常保护抗体免于降解的回收受体的结合也相似。由此,后来在细胞实验或动物实验中观察到的任何差异都可以追溯到糖配对本身,而非隐含的损伤或杂质。
观察细胞如何吞噬抗体
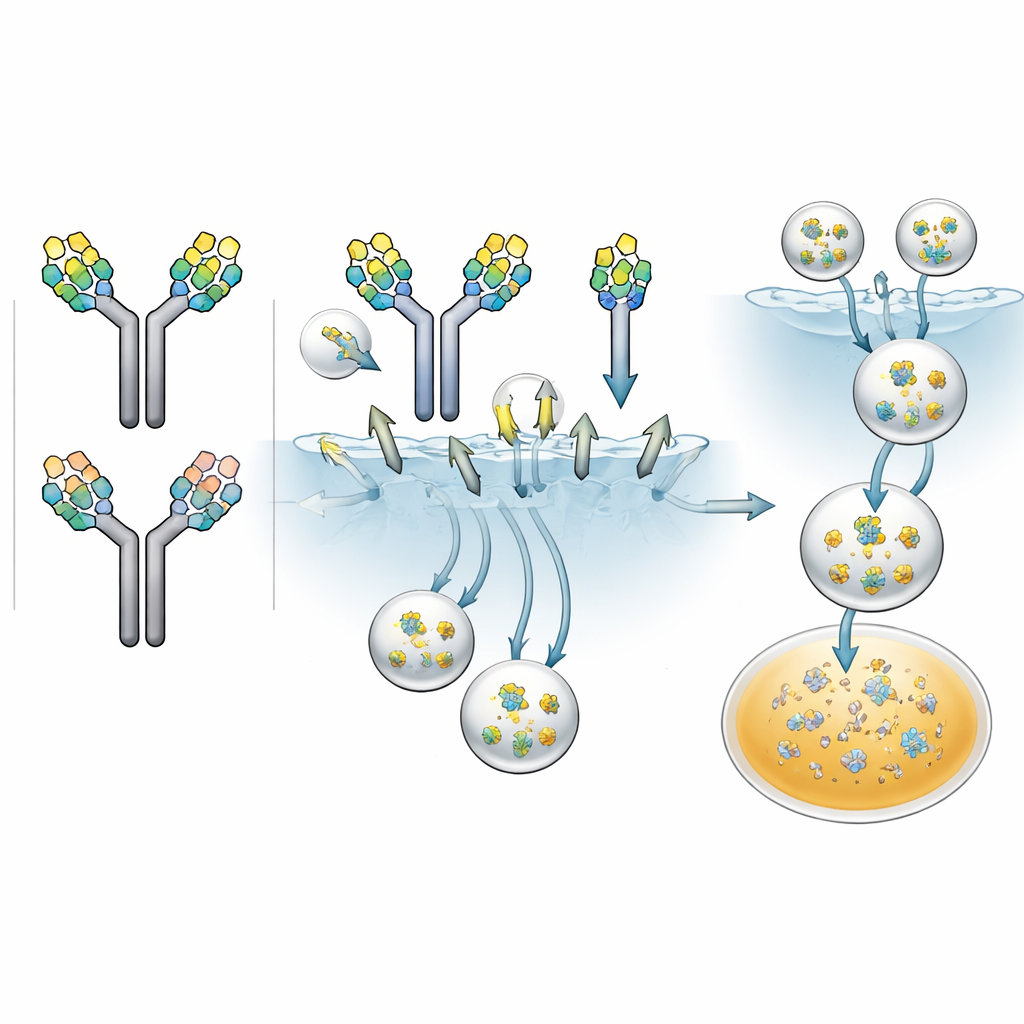
接着,研究人员询问每种糖模式使抗体被表达甘露糖受体的细胞吞噬的速度如何。他们用荧光标记不同的抗体组分,并与被工程化显示该受体的人源细胞共同孵育。近三天内,他们追踪细胞内部的荧光强度作为摄取量的指标。所有抗体都在一定程度上被摄取,但速度不同:两个高甘露糖的抗体被内化最快,带有一个高甘露糖的抗体居中,只有复杂型糖的抗体最慢。当团队加入甘露聚糖(天然糖,可与甘露糖受体竞争)时,高甘露糖抗体的摄取显著下降,这证实该受体对快速内化负有主要责任。
追踪带糖标记的抗体在活体中的去向
关键测试是这些细胞水平的差异是否会转化为真实药物行为。科学家将富含对称和非对称高甘露糖配对以及仅复杂型配对的药物配方注射到大鼠体内。利用灵敏的质谱方法,他们不仅能在两周内追踪总抗体水平,还能分别跟踪每种糖配对随时间的下降。结果令人惊讶:带有两个高甘露糖的抗体消失最快,半衰期约为2.4天;带一个高甘露糖的抗体持续时间更长,约为7.2天;而仅含复杂型糖的抗体则可存在约17.4天。随时间的暴露量——浓度曲线下面积——与仅复杂型配对相比,双高甘露糖配对下降到38%,混合配对下降到73%。本质上,每增加一个高甘露糖就像为甘露糖受体添加了一个额外的“请清除我”标志。
对更安全、更持久药物的意义
对患者而言,这些结果阐明了为什么两种在纸面上看似相似的抗体药物在体内可能表现不同。研究表明,不仅高甘露糖的存在,而且它们的配对方式都会强烈影响抗体被清除的速度,这很可能通过甘露糖受体介导的摄取和在免疫细胞内的降解实现。由于同一通路也可能将抗原输送到触发免疫反应的机制中,这些糖模式可能影响抗药抗体和过敏反应的风险。作者建议制造商在设计和测试抗体疗法时应监测并控制糖链配对——而不仅仅是总体糖组成。这样做有助于实现更可预测的给药方案、更持久的疗效以及更低的意外免疫反应风险。
引用: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
关键词: 单克隆抗体, 糖基化, 甘露糖受体, 药代动力学, 免疫原性