Clear Sky Science · zh
用于患者来源癌症类器官宽场光学氧化还原成像的自动化图像分析流程
这项癌症成像研究为何重要
为每位患者找到合适的抗癌药物仍然是一个缓慢且带有碰运气性质的过程。本研究通过将患者来源的微小培养肿瘤(称为类器官)与一种基于相机的快速方法相结合来观察加入药物后其能量利用如何变化,从而应对这一问题。作者展示了一个新的自动化计算流程如何处理大量显微镜图像、在数天内追踪数百个类器官,并揭示哪些处理有效——这一切比人工手工操作快得多且更可靠。
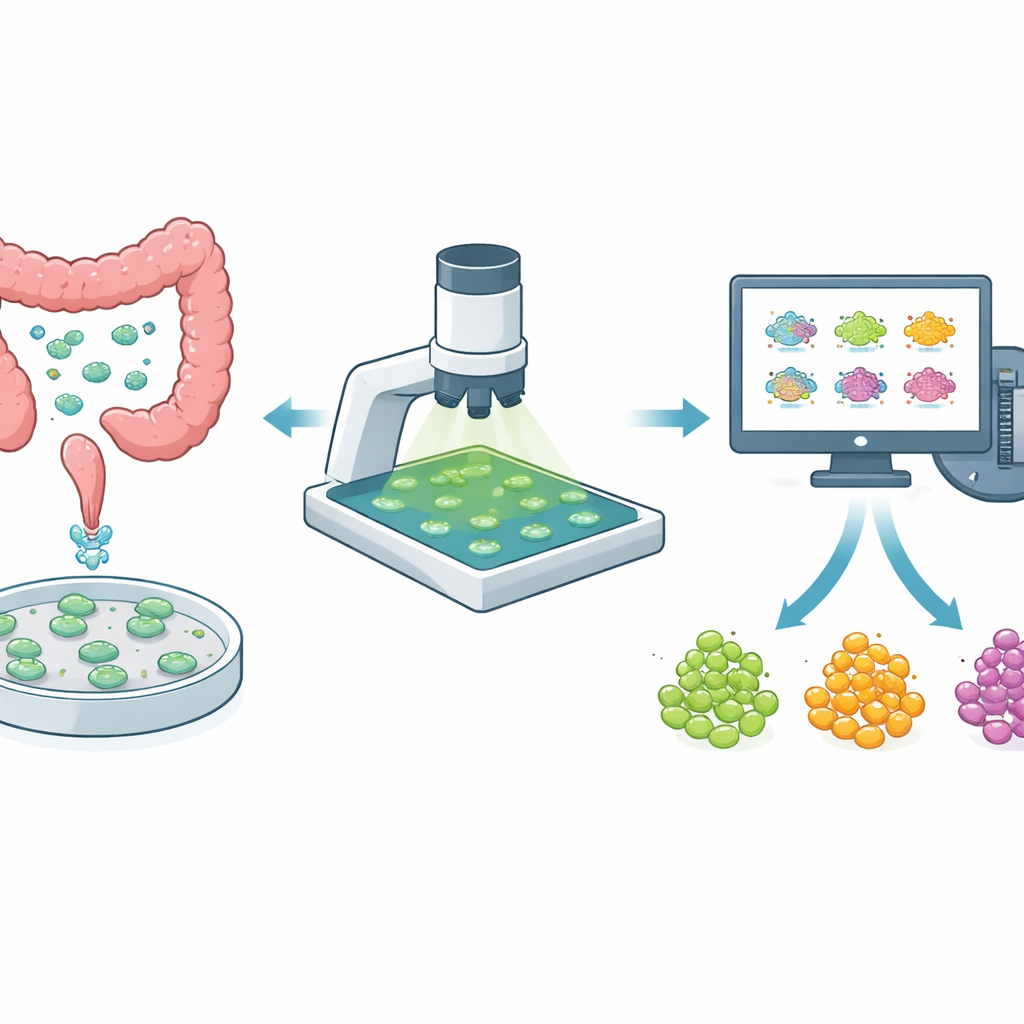
作为试验台的培养皿微型肿瘤
研究者现在常常使用直接从患者肿瘤制备的三维类器官,而非仅依赖平面培养的癌细胞。这样的微型肿瘤更好地保留了体内细胞类型的混合以及存在的耐药细胞隐匿区域。在结直肠癌中,肿瘤在不同患者之间乃至同一患者体内差异很大,类器官成为检测新药和既有药物疗效的强有力工具。但要用于指导治疗,类器官测试必须既温和——以便对同一个类器官进行长期观察——又要足够快速,以筛选大量药物及剂量。
用光观察肿瘤的“燃料使用”
团队使用一种称为光学氧化还原成像的技术,该方法依赖细胞内参与能量产生的分子微弱的天然荧光。通过照射特定波长的光并收集发射的荧光,一个简单的宽场显微镜就能捕捉到每个类器官的“氧化”或“还原”程度分布图——即其代谢状态的快照。与更复杂的高端显微镜不同,这一配置使用许多实验室已有的标准组件,因而相对容易推广。该氧化还原信号的变化常常比类器官大小或细胞死亡的变化更早出现,使其成为评估药物是否有效的早期警示信号。
将原始图像转化为可靠的数据
此前,分析这些图像需要人为在每个类器官周围画出轮廓、目测选择背景区域,然后尝试在多天中追踪哪个类器官对应哪个。这种缓慢且易出错的方法不适合大规模药物筛选。作者创建了一个端到端的自动化流程,完成三项艰巨任务:精确地将每个类器官与其周围环境区分开,为每个类器官在多天中分配一致的身份标识,以及以避免人为偏差的方式估算背景信号。他们对现有的人工智能工具(Cellpose)进行了微调,使其即使在类器官形状、大小和焦距变化时也能识别,然后构建了一个追踪算法,对齐不同天拍摄的图像并基于形状与位置重叠来匹配类器官。
放大关注最活跃的边缘
类器官具有不同分区:一个死或濒死的核心、一个较为静止的中间区,以及一个活跃的外缘——细胞在此繁殖活跃且通常对治疗最敏感。该流程会自动为每个类器官切出这层薄薄的外环——称为前沿区域——并计算其氧化还原值。通过在不同剂量的罗米地辛处理下,追踪同一类器官前沿区域三天的变化,软件能检测到代谢的细微转变。作者表明,相对于将所有类器官合并分析,逐个类器官追踪能减少变异性,提高统计检出能力,即使不同微型肿瘤的响应不一致,也能更清楚地看到药物效应。
更快、更稳健的药物反应见解
研究者在两种不同显微镜系统的图像上测试了他们的流程,发现自动勾画的轮廓与专家手绘的高度一致,追踪结果与人工追踪的吻合率超过94%。在比较整体药物反应度量时,自动方法在灵敏度上与人工方法相匹配,同时将分析时间缩短了百倍以上——从需要数小时的人力到仅需几分钟的计算处理。对于使用患者来源类器官的实验室,这意味着他们可以现实地分析大型图像集合并发现每个微型肿瘤对治疗的反应。从长远看,这类自动化分析有助于推动基于类器官的药物测试更接近临床,支持更个体化、更有效的癌症治疗。
引用: Hsu, A., Samimi, K., Gillette, A.A. et al. An automated image analysis pipeline for wide-field optical redox imaging of patient-derived cancer organoids. Sci Rep 16, 9757 (2026). https://doi.org/10.1038/s41598-026-40249-4
关键词: 结直肠癌, 患者来源类器官, 光学氧化还原成像, 自动化图像分析, 药物反应