Clear Sky Science · zh
体外膜肺氧合中流动诱发血栓形成与生长的多模态表征
为什么生命维持设备中的血栓很重要
体外膜肺氧合(ECMO)是一种心肺旁路方法,可在患者器官恢复期间维持危重患者的生命。但将血液通过泵和塑料管路循环,会使血液暴露于我们身体并非为之设计的强烈机械力下。这些力可触发回路内的危险血栓,进而增加中风、器官损伤或设备故障的风险。本研究旨在揭示血液通过 ECMO 泵的流动如何具体影响这些血栓的起始与生长,最终目标是使 ECMO 更加安全和有效。
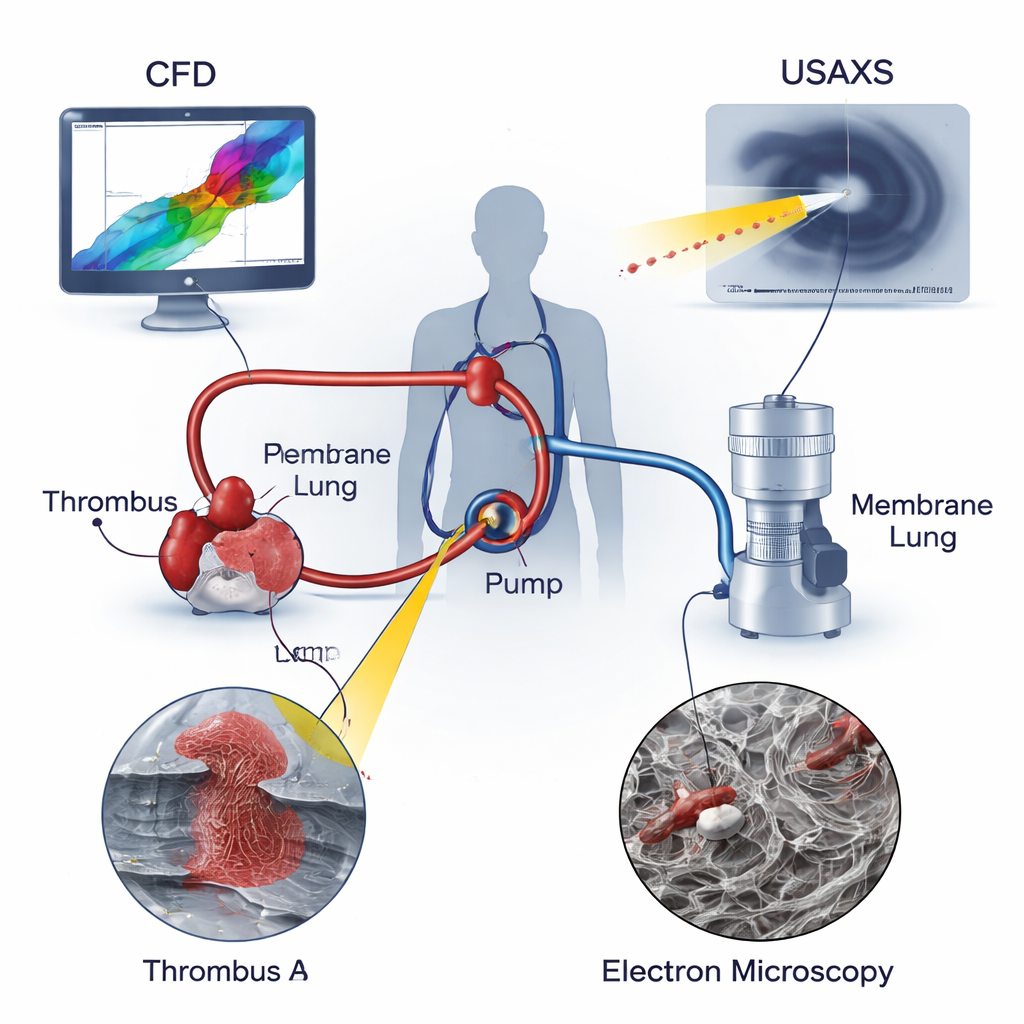
ECMO 如何维持患者生命
在 ECMO 中,血液从大静脉或动脉被抽出,经离心泵推动通过“膜肺”以补充氧气并移除二氧化碳,然后回输给患者。与在天然血管中平稳流动的血液不同,ECMO 回路内的流动存在极端情况:非常快速的流束、急剧的流向变化以及几乎停滞的滞留区。这些环境已知会损伤血细胞并刺激凝血。传统医学模型侧重于血管内的缓慢或阻塞流动,但并未完全考虑血液在旋转泵内所经历的强烈剪切和拉伸。作者认为,要真正理解 ECMO 中的血栓风险,必须同时研究设备内的机械力和形成血栓的显微结构。
从三种视角观察血栓
研究人员结合三种强有力的工具来分析取自儿童 ECMO 回路的两个真实血栓:位于泵入口处的血栓 A 和泵下游管路中的血栓 B。计算流体力学(CFD)模拟了血液在泵内的运动,揭示了回流和旋涡流动区域并定位了剪切与拉伸力的峰值。超小角 X 射线散射(USAXS)深入探测每个血栓,测量纤维蛋白支架——凝块结构的蛋白网格——在样本中的致密度与方向一致性。扫描电子显微镜(SEM)提供了凝块表面的高倍图像,显示红细胞、白细胞、血小板及周围纤维蛋白纤维的形态。通过叠加这三种视图,研究团队能够将局部流动条件与每个血栓的内部构架联系起来。
回流区形成致密且有取向的血栓
CFD 显示,血栓 A 形成的泵入口附近存在回流区:血液沿壳体向后并向上推进,然后重新汇入主流。该区域使血液成分滞留,同时在回流与来流的边界处经历明显的速度差异。USAXS 在血栓 A 内指示出高比例的纤维蛋白含量——至少 70%——以及纤维在首选方向上的强烈整体取向,表明这是一个致密而刚性的支架。SEM 图像证实了紧密交织的纤维蛋白网络,夹杂着形态异常的红细胞和血小板碎片。作者提出,长停留时间与强局部剪切的组合促进了一个能抵抗泵机械应力的紧凑、高度有序血栓的生长。
旋转出口塑造出更松散、扭曲的血栓
相比之下,取自泵后管路的血栓 B 在以旋转出流为主的区域生长。CFD 显示从泵出口出现旋转、螺旋状的流动结构,USAXS 数据表明纤维蛋白网络仍占主导但总体密度更低、取向性较弱。纤维蛋白主方向在血栓内逐渐变化,从一个倾斜角度过渡到另一个,呼应了扭曲的流动模式。SEM 图像显示不同粗细的纤维蛋白丝和大量被困的红白细胞,包括细胞损伤和炎症的证据。重要的是,模拟还识别出泵体积中小但显著的部分,拉伸力足以使冯·维尔布兰因子(von Willebrand factor)展开——这是一种在受力时会变得粘附并迅速招募血小板的关键血浆蛋白。这些区域集中在叶轮叶片和出口附近,使其成为导致血栓 B 初始激活事件的可能部位。
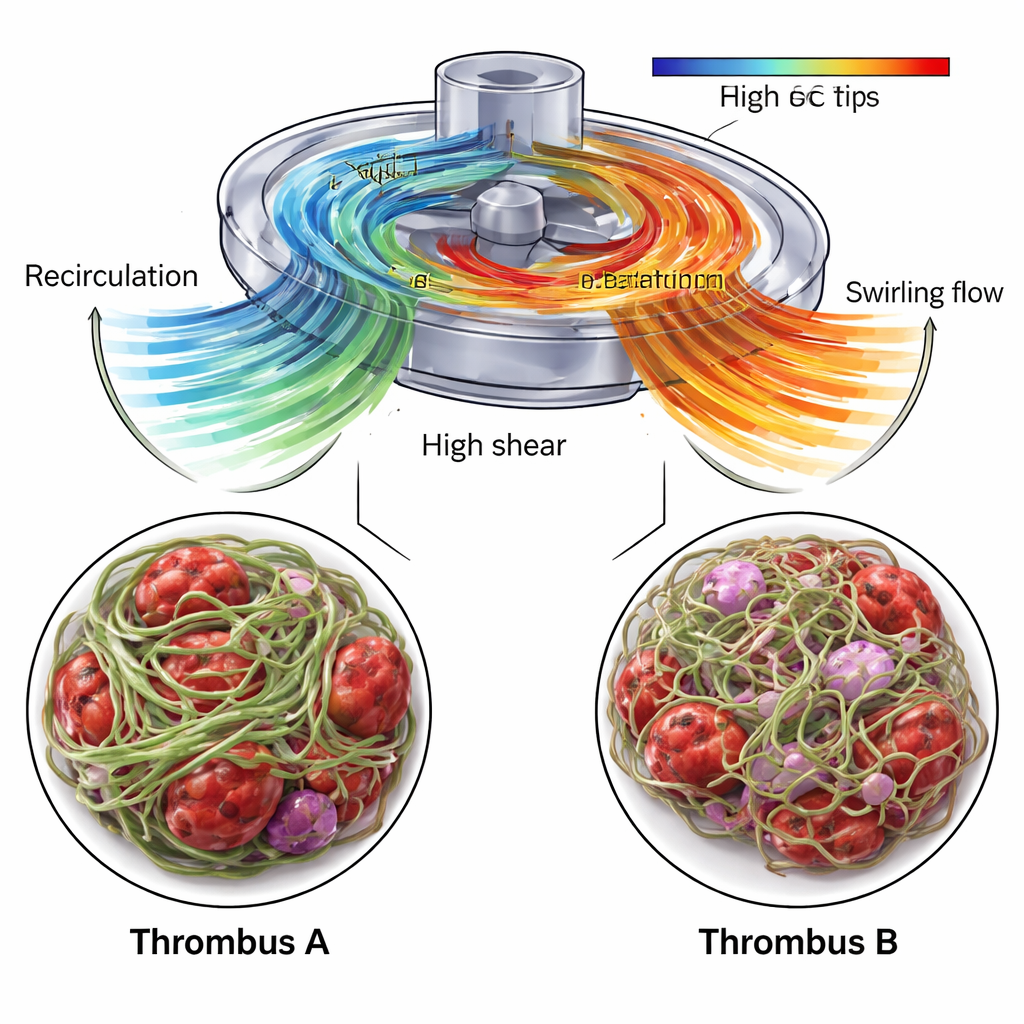
走向更安全的生命维持设备
通过将血流的详细模拟与对真实 ECMO 血栓的 X 射线和电子显微镜测量相结合,本研究表明凝块的内部“纹理”和密度反映了其形成时的机械环境。泵入口附近的回流流动与致密、高度取向的纤维蛋白支架相关,而旋转出流则与更扭曲、开放的网络相关,该网络仍能捕获大量血细胞与免疫细胞。这些见解突出了 ECMO 泵和管路中可通过结构改进或有针对性的抗凝调整最有效降低血栓风险的特定区域。从泵几何与流动模式到蛋白排列的多尺度映射,长期来看可指导更安全的设备设计,并帮助临床医生在救命的 ECMO 支持期间更好地平衡出血与血栓的双重风险。
引用: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
关键词: ECMO, 血液凝固, 剪切应力, 离心血泵, 纤维蛋白结构