Clear Sky Science · zh
西普洛福通过上调AMPK抑制铁死亡以减轻大鼠脑缺血–再灌注损伤
为何在卒中后保护大脑至关重要
当发生缺血性卒中时,医生会争分夺秒地重开被阻塞的血管,恢复大脑供血。具有讽刺意味的是,这一挽救生命的步骤本身可能造成额外损伤,这一现象称为再灌注损伤。大脑在经历一段缺血后突然被氧气和营养物质淹没,会触发一系列化学反应风暴,可能导致脆弱的神经细胞死亡。本研究探讨了西普洛福——一种已用于镇静的新型麻醉药——在血流恢复这一关键时刻,是否能通过抑制一些最有害的过程来保护大脑。
从血流阻断到脑损伤的过程
为模拟人类卒中发生的情况,研究者在大鼠中短暂阻断了一条主要脑动脉,然后恢复血流,造成所谓的脑缺血–再灌注损伤。有些大鼠仅接受该手术程序,另一些则在血流恢复后不久给予西普洛福。研究组随后评估了动物的运动和触觉反应能力,并检查其大脑中坏死组织范围以及神经细胞的结构损伤。接受西普洛福处理的大鼠表现出更小的脑损伤区域、形态更健康的神经细胞,以及比未处理动物更好的运动和感觉评分,提示该药减轻了损伤的严重后果。
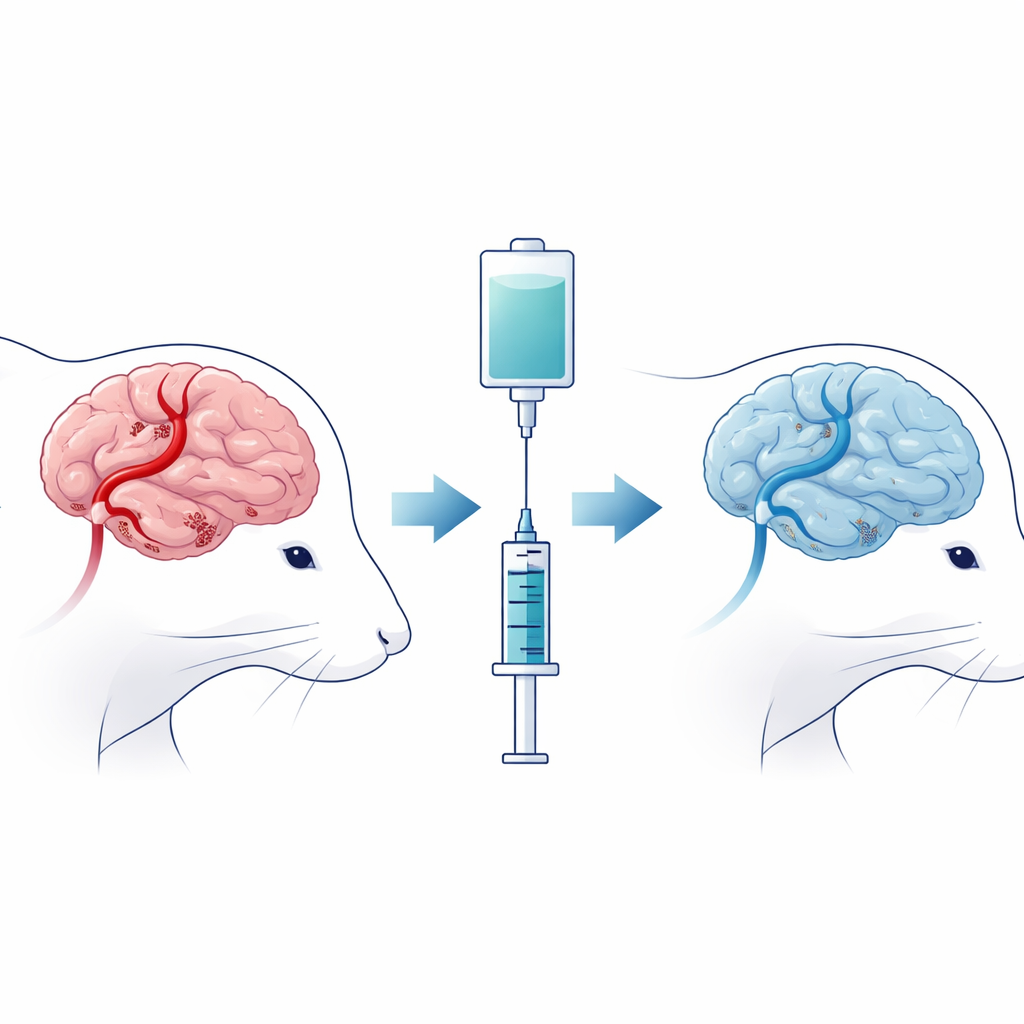
一种由铁驱动的隐性细胞死亡形式
除了可见的组织损伤外,作者还关注了一种新近被认识的细胞死亡类型——铁死亡,该过程由铁和失控的化学反应驱动,会攻击细胞膜的脂质成分。在未经处理的卒中模型大鼠中,损伤核心周围的易损区脑组织含铁量更高,脂质损伤副产物水平升高,电子显微镜下神经细胞线粒体表现为肿胀且结构破坏。分子检测显示,通常用于解毒有害脂质副产物的保护性蛋白减少,而促进该破坏过程的蛋白则增加。西普洛福在很大程度上逆转了这些变化:铁和脂质损伤下降,关键蛋白的平衡向保护方向转移,线粒体保持了更接近正常的形态和内部结构。
作为控制开关的细胞能量传感器
研究随后探讨了西普洛福如何产生这些保护作用。注意力集中在AMPK上——一种作为细胞能量传感器和应激应答器的蛋白。在未经处理的受伤大脑中,AMPK活性受到抑制。西普洛福提高了AMPK的活化形式,这与铁死亡相关损伤的减少同步出现。为检验这一能量传感器是否真正位于保护链条的上游,研究者使用了另一种药物Compound C来阻断AMPK。当动物同时接受西普洛福和该AMPK抑制剂时,西普洛福的益处部分丧失:与铁死亡相关的标志物回升至有害水平、铁蓄积恢复,且AMPK活性信号甚至低于未处理的卒中动物。这一模式支持了激活AMPK是西普洛福保护神经细胞关键步骤的观点。
抑制大脑炎性风暴
卒中相关损伤不仅是神经元内细胞死亡的问题;大脑的免疫反应也起到重要作用。研究组测量了几种在缺血–再灌注后通常激增的炎性信使分子。在未处理的动物中,这些信号显著升高,反映出强烈的炎性反应。西普洛福降低了所测的三种主要炎性标志物,表明它不仅抑制铁驱动的膜损伤,还缓和了随之而来的炎性风暴。当用Compound C阻断AMPK时,这些对炎症的抑制作用被削弱,再次将西普洛福的益处与这一中心能量感应通路联系起来。
这对未来护理可能意味着什么
综合来看,结果表明西普洛福不仅仅是一种镇静剂:在该大鼠模型中,它似乎通过激活AMPK来限制卒中相关的脑损伤,而AMPK进而抑制了铁驱动的细胞死亡并减弱炎症。由于西普洛福已在临床用于麻醉和操作性镇静,它作为脑保护剂的潜在附加价值尤为引人关注。不过,这项工作也存在重要局限性,包括仅依赖单一动物模型以及AMPK阻断药物本身可能具有副作用的可能性。还需要更多研究,包括在其他物种以及最终在人类患者中的研究,以确认西普洛福在卒中治疗期间及之后能否安全地帮助保护大脑。
引用: Zeng, H., Yu, X., Zheng, Z. et al. Ciprofol attenuates cerebral Ischemia‒reperfusion injury in rats by inhibiting ferroptosis through upregulating AMPK. Sci Rep 16, 9282 (2026). https://doi.org/10.1038/s41598-026-40104-6
关键词: 缺血性卒中, 再灌注损伤, 西普洛福, 铁死亡, 神经保护