Clear Sky Science · zh
MyoFuse 是一个完全基于人工智能的体外骨骼肌细胞融合自动定量工作流
为什么数肌细胞很重要
当我们锻炼、从损伤中恢复或患上如糖尿病等疾病时,骨骼肌会不断重塑。在实验室中,科学家通过在培养皿中培养肌细胞并观察单个细胞融合成长长的多核纤维来模拟这一过程。一个简单的数值——融合指数——可以告诉他们融合进行了得如何。但今天这个数值通常由人工在屏幕上手动计数成千上万微小细胞核得到——既费时又容易出现不一致和错误。本研究介绍了 MyoFuse,一个完全基于人工智能的工作流,用于自动化该计数任务,旨在使肌肉研究更快、更可靠且更少偏差。
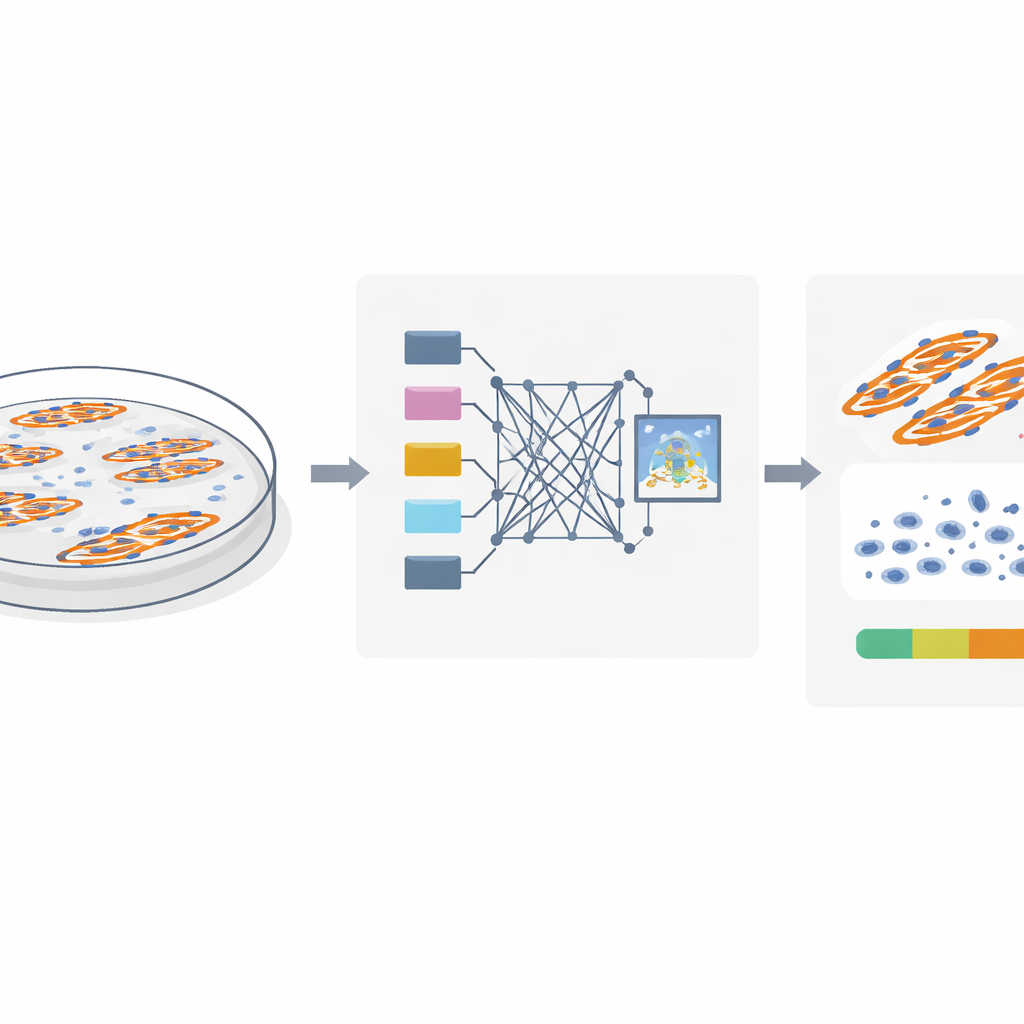
看清真实情况的挑战
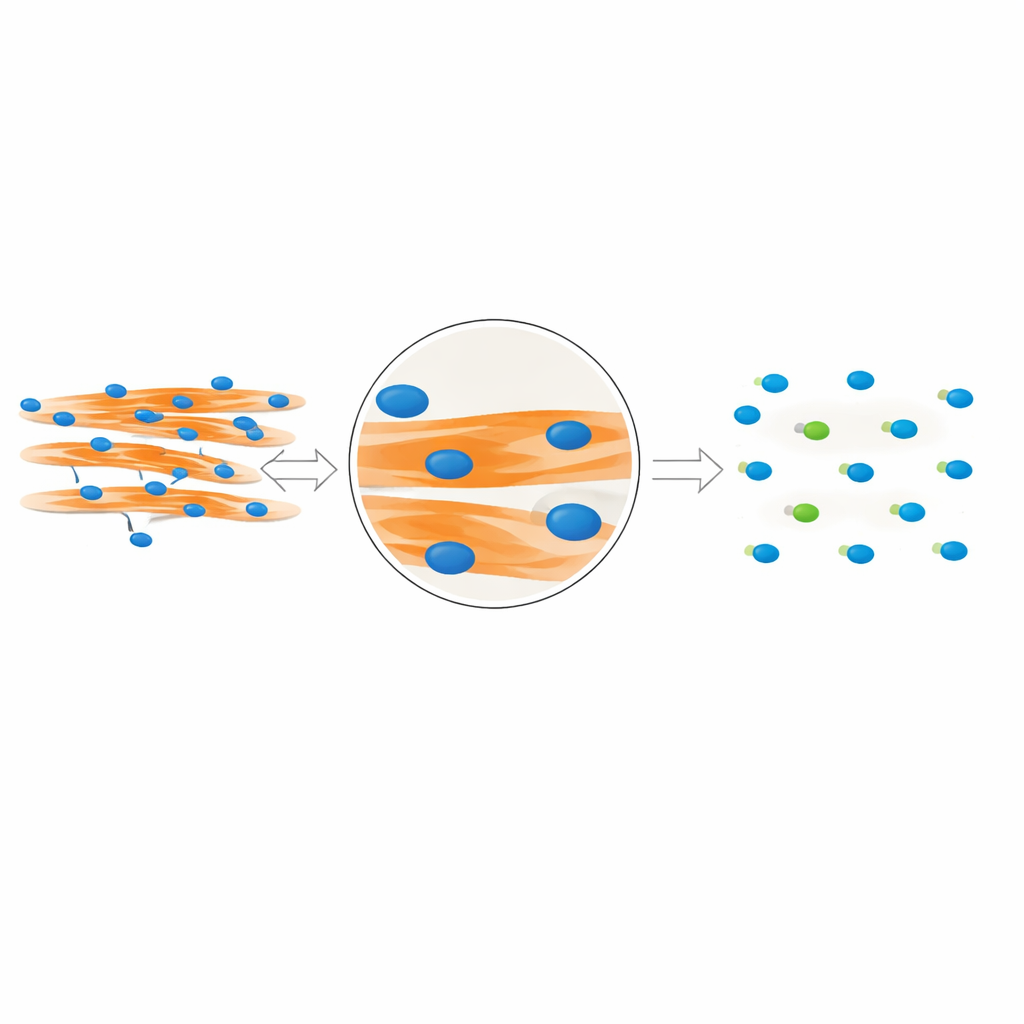
为了研究肌细胞融合,研究者用荧光染料标记细胞核和肌纤维并拍摄显微镜图像。关键问题是哪些细胞核确实位于融合的肌纤维内部,哪些则属于旁边未融合的细胞。传统方法假定如果在二维图像中细胞核与肌纤维重叠,那该细胞核必定在纤维内。然而,细胞是三维生长的:细胞核很容易位于纤维的上方或下方,在图像中仍然看起来像是重叠。作者使用小鼠和人类肌细胞的详细共聚焦成像表明,这种重叠的做法可能产生误导,导致许多邻近的细胞核被错误地计为融合纤维的一部分,从而抬高了融合指数。
更聪明地解读荧光图像
研究团队注意到真正“在纤维内”的细胞核会留下独特的视觉痕迹。由于这些细胞核实际占据纤维内的空间,它们会在标记肌肉蛋白 MyHC 的荧光信号中产生小的暗区。相比之下,位于纤维上方或下方的细胞核并不会破坏该信号。基于这一洞见,作者设计了 MyoFuse,一个两步的人工智能工作流。首先,采用一个专门的分割模型(改编自开源工具 Cellpose)精确描绘单个细胞核的轮廓,即便它们紧密聚集成簇也能识别。其次,一个轻量级神经网络分类器检查每个细胞核周围的 MyHC 信号,并仅根据这种局部模式而非简单的重叠来判断其是在纤维内还是在外部。
人工智能与人类专家的匹配程度
研究人员在小鼠 C2C12 肌细胞和来自不同肌肉的人原代肌细胞图像上严格测试了 MyoFuse。对于这两种物种,人工智能对总细胞核的计数及其计算出的融合指数与专家的细致人工标注高度一致,相关性近乎完美。在单个细胞核水平上,分类器在各数据集中能在超过 90% 的情况下正确区分纤维内外细胞核,其性能指标可与人类区分水平媲美。重要的是,MyoFuse 在一组从未用于训练的人类细胞图像上也表现良好,这表明该方法能推广到新的样本,而不仅仅是记忆训练图像。
揭示常用方法中的隐性偏差
除了准确性外,MyoFuse 还揭示了广泛使用的基于掩膜的方法的系统性问题,这些方法依赖于核与纤维信号的简单重叠。当作者将 MyoFuse 的融合指数与应用于相同图像的改进掩膜方法的结果比较时,掩膜方法在融合估计上持续高估,尤其是在肌纤维覆盖培养皿较大比例的区域。调整检测阈值会改变数值但并不能消除这种潜在偏差;表面上的改进常常来自互相抵消的错误而非更准确的生物学判断。团队还展示了同一孔的不同区域之间融合估计可能大幅波动,强调仅分析少量手工挑选的视野可能会扭曲对细胞融合程度的认识。
这对未来肌肉研究的意义
MyoFuse 为肌肉生物学家提供了一种既更快速又更忠实于培养皿真实情况的细胞融合测量方法。通过将自动显微成像与能够在几分钟内分割并分类数十万细胞核的人工智能相结合,该工作流减少了人力工作量,降低了关于选择观测区域和图像阈值的主观性,并避免将邻近细胞误计为融合肌纤维。作者承认极端成像条件或非常不同的染色协议可能需要重新训练,但该方法是公开可用并旨在易于适应。对于研究肌肉发育、衰老、再生或代谢疾病的实验室来说,MyoFuse 有望带来更稳健的融合测量——也因此带来对肌肉生长与变化更可信的结论。
引用: Lair, B., Cazorla, C., Lobeto, A. et al. MyoFuse is a fully AI-based workflow for automated quantification of skeletal muscle cell fusion in vitro. Sci Rep 16, 9387 (2026). https://doi.org/10.1038/s41598-026-40047-y
关键词: 骨骼肌, 细胞融合, 人工智能, 图像分析, 肌发生