Clear Sky Science · zh
Caldesmon-1 介导的肌动蛋白动力学对主动脉瓣间质细胞成骨分化至关重要
为什么心脏瓣膜变硬很重要
随着年龄增长,心脏的一个关键闸门——主动脉瓣——可能会逐渐变得僵硬甚至像石头一样硬。这个病症称为主动脉瓣狭窄,会迫使心脏更费力地泵血并可能导致心衰。到目前为止,唯一可靠的治疗手段是外科或导管置换瓣膜。这里总结的研究提出了一个基础但关键的问题:是什么让本来柔软、富有弹性的瓣膜组织逐步转变为类似骨骼的物质?通过发现这一过程中的一个关键分子参与者,研究指向未来有望减缓甚至阻止瓣膜钙化的药物策略,而不是仅仅替换受损瓣膜。
深入观察瓣膜中的隐秘“工人”
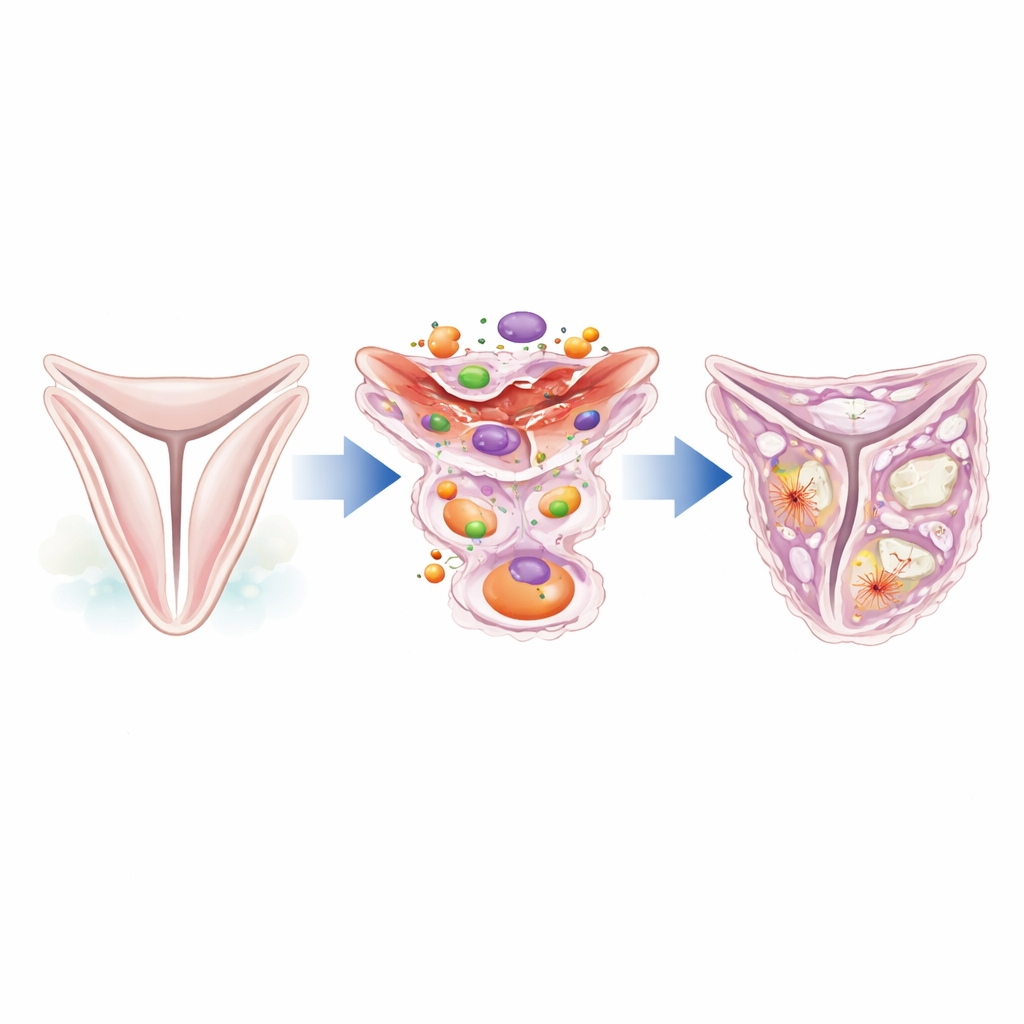
主动脉瓣叶由一层称为瓣膜间质细胞的专门支持细胞支撑。在健康瓣膜中,这些细胞保持静默,帮助维持组织结构。然而在压力或损伤下,它们会改变身份,开始表现为成瘢痕的细胞或甚至成骨细胞。作者关注一种称为 caldesmon-1 的蛋白,它有助于控制由肌动蛋白丝构成的细胞内部支架。通过挖掘已有的人类瓣膜单细胞 RNA 测序数据,他们发现与正常瓣膜相比,患有主动脉瓣狭窄的瓣膜中 caldesmon-1 明显升高,尤其是在增厚、纤维化区域的间质细胞中。
从柔软组织到纤维化与类骨斑块
对人类瓣膜样本的显微镜研究显示,caldesmon-1 蛋白在病变的瓣膜叶中大量存在,并与活化的收缩性细胞和产生胶原的成成纤维样细胞的标志物共线。这些富含 caldesmon-1 的细胞聚集在纤维化和早期钙化的区域周围,提示它们参与构建导致瓣膜增厚的额外基质。进一步分析表明,这些细胞表达平滑肌样和易成骨细胞类型的典型基因,并且大量合成 I 型胶原等结构蛋白。换言之,在瓣膜变硬和瘢痕化的地方,呈 caldesmon-1 阳性的间质细胞往往出现在现场。
一种控制形态的蛋白如何推动细胞走向骨化
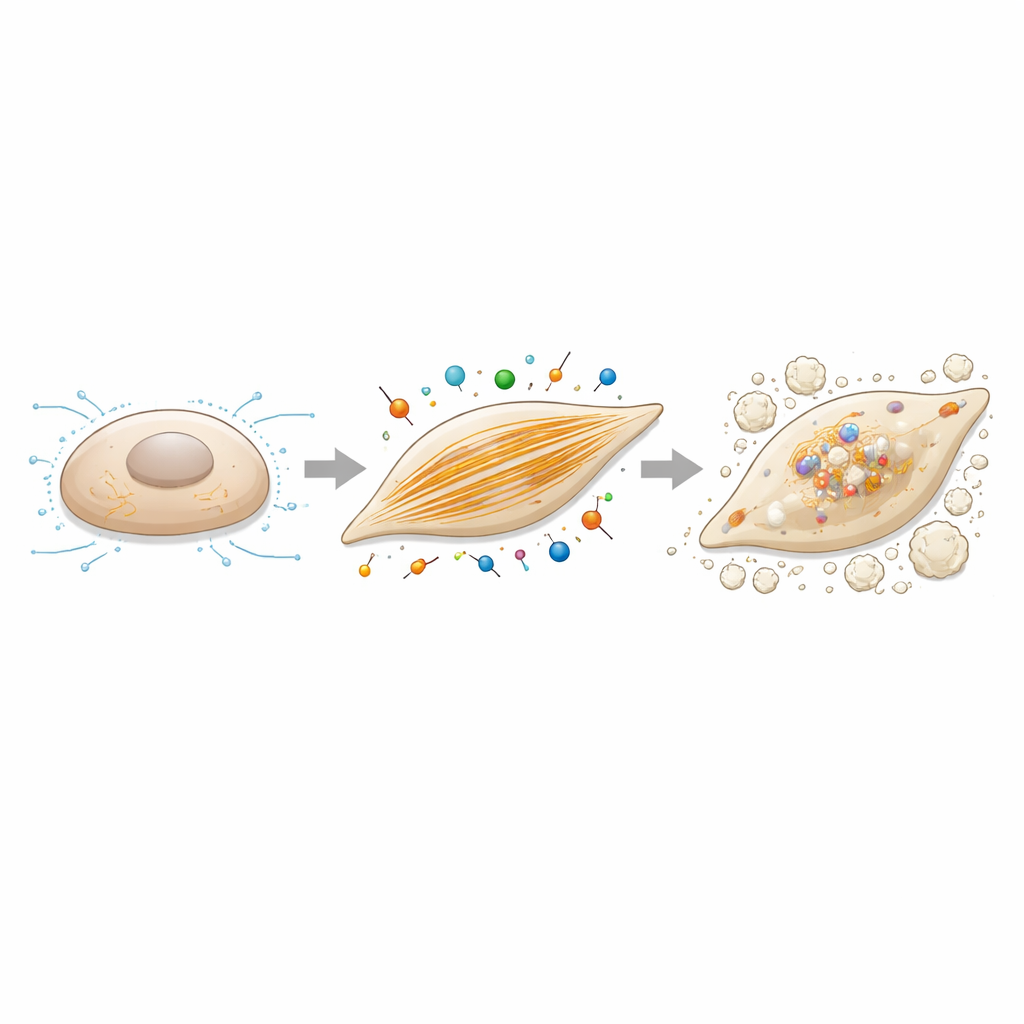
为弄清因果关系,研究团队分离了人类瓣膜间质细胞并使用小干扰 RNA 下调 caldesmon-1。缺失该蛋白后,细胞失去了伸长的纺锤形态,变得更为圆钝。其内部的肌动蛋白丝变得稀薄,细胞的增殖和定向迁移能力下降。当研究者将这些细胞置于成骨(促骨)培养基中时,正常细胞很容易形成钙沉积,而 caldesmon-1 缺失的细胞则显示出明显较少的矿化积累。大规模 RNA 测序证实,许多参与骨形成和组织重塑的基因(包括著名的成骨驱动因子如 RUNX2 和碱性磷酸酶)在成骨条件下被强烈激活,但在 caldesmon-1 被敲低时未能上调。
将肌动蛋白丝视为控制钙化的杠杆
由于 caldesmon-1 是肌动蛋白的调节因子,作者接着询问直接改变肌动蛋白组装是否会改变细胞的钙化倾向。他们在应用同样的促骨培养条件时,用环胞裂素 B(cytochalasin B,一种温和扰乱肌动蛋白丝生长的化合物)处理瓣膜间质细胞。在不会严重损害细胞存活的剂量下,该处理显著减少了钙沉积并降低了与骨化相关基因的表达,包括 caldesmon-1 和 RUNX2。与敲低实验结合,这些发现描绘出一个连贯图景:稳固的肌动蛋白丝网络及其支持的收缩力不仅仅是旁观者——它们积极地驱动了瓣膜中由静默支持细胞向成骨细胞的转变。
这对未来治疗意味着什么
对非专业读者而言,主要信息是主动脉瓣变硬是一个主动且受调控的过程,而非简单的“磨损”。本研究鉴定出 caldesmon-1 作为将细胞内骨架与制造类骨组织的基因程序连接起来的关键协调子。通过帮助瓣膜间质细胞获得收缩性、纤维化并最终成骨的身份,caldesmon-1 直接促成了狭窄瓣膜上硬质沉积的累积。尽管针对该蛋白或肌动蛋白动力学的任何疗法都需谨慎评估以避免对其他组织造成不良影响,但 caldesmon-1 介导的通路现在突出成为旨在在手术必要之前减缓或阻止瓣膜钙化的有前景的药物候选目标。
引用: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
关键词: 主动脉瓣钙化, caldesmon-1, 瓣膜间质细胞, 肌动蛋白细胞骨架, 成骨分化