Clear Sky Science · zh
RBP4通过抑制PI3K/AKT信号通路并促进巨噬细胞M1型极化干预舌鳞状细胞癌进展
为什么舌癌需要新思路
舌癌可能夺走人的说话、进食和味觉能力,即便采用手术、化疗和放疗,长期生存率仍常令人失望。这项研究探索了血液中一个意想不到的帮手——一种携带维生素A的蛋白RBP4,揭示它既能减缓舌肿瘤生长,又能召集机体自身的免疫防御。通过揭示该分子在癌细胞内及周围免疫细胞中的作用机制,研究指出了有望使治疗更有效且损伤更小的新策略。
舌肿瘤中的一种隐匿蛋白
研究者首先通过筛查大型癌症基因数据库,寻找哪些与免疫相关的基因可预测舌鳞状细胞癌患者的预后。在数百个候选基因中,RBP4——一种以在血液中运输维生素A而闻名的蛋白——显得尤为引人注目。当团队比较肿瘤样本与邻近的健康舌组织时,发现肿瘤中的RBP4水平持续显著偏低。这一模式在多个独立数据集中以及来自20名患者的组织样本中得到证实,提示RBP4的丧失可能是该疾病的常见特征。
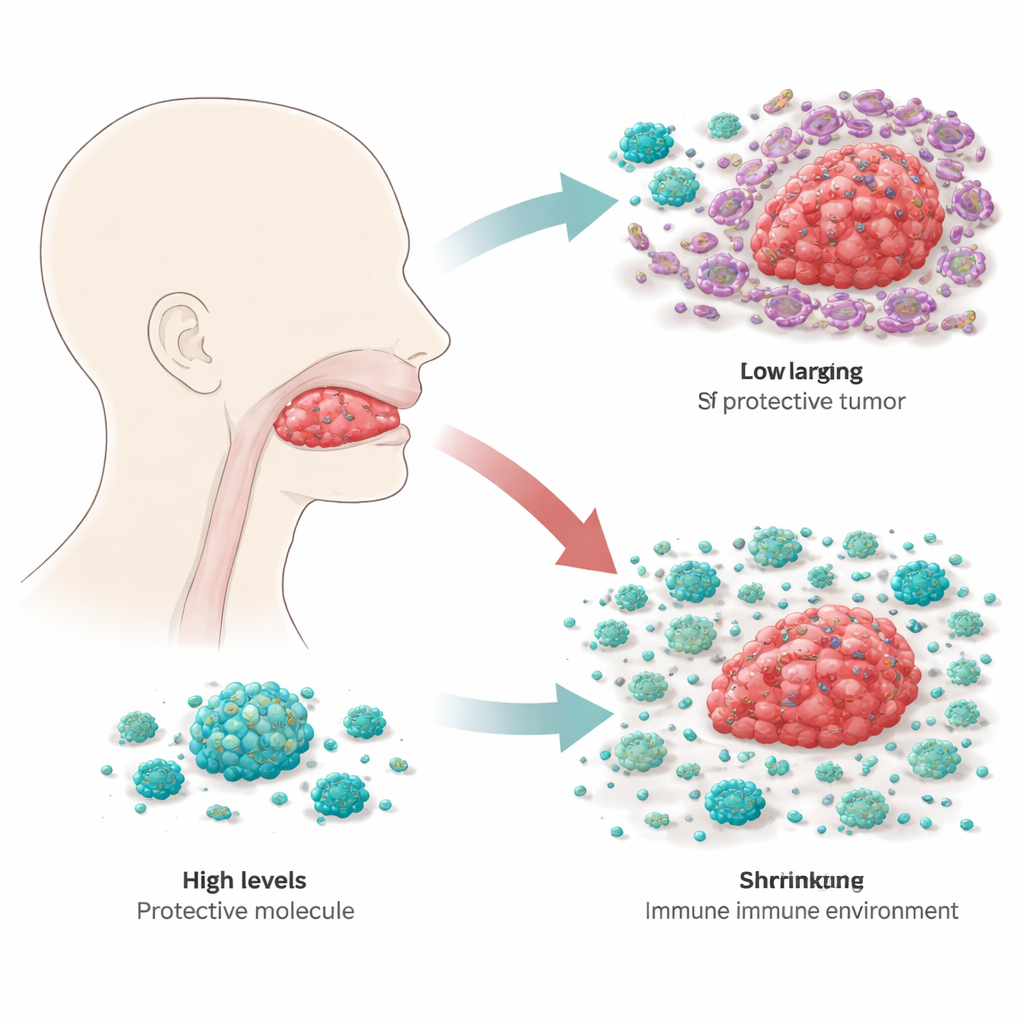
从内部减缓肿瘤生长
为了弄清RBP4在舌癌细胞中的实际功能,科学家们对肿瘤细胞系进行了工程改造,使其要么额外表达RBP4,要么大幅减少RBP4。在培养皿中,RBP4较高的细胞生长更缓慢,而RBP4减少的细胞增殖更快,并且在人工膜上的迁移和侵袭能力更强,这些行为与转移和复发有关。当将这些经过改造的细胞植入小鼠体内时,过表达RBP4的肿瘤保持较小,而RBP4降低的肿瘤生长更具攻击性。通过追踪细胞内关键的生长调控开关,团队表明RBP4抑制了一个主要的生长通路——PI3K–AKT–mTOR,该通路被许多癌症当作内部“油门”。当RBP4水平高时,该通路更为沉寂,肿瘤细胞不易获得有利于迁移的可塑、活动状态。
将免疫细胞转变为抗肿瘤战士
癌症并非孤立生长;它存在于由免疫细胞、血管和支持细胞组成的肿瘤微环境之中。在这里,巨噬细胞——能攻击或辅助肿瘤的大型免疫细胞——扮演核心角色。研究人员注意到,含有更多RBP4的肿瘤也往往富含“M1”型巨噬细胞,这一类型与炎症和抗肿瘤相关,而非常常支持肿瘤生长的“M2”型。在细胞培养中,当巨噬细胞暴露于纯化的RBP4或由工程化舌癌细胞分泌更多RBP4的环境时,它们会转向这种M1、抗肿瘤的状态。当癌细胞中的RBP4减少时,巨噬细胞则倾向于向更有利于肿瘤的表型滑落。
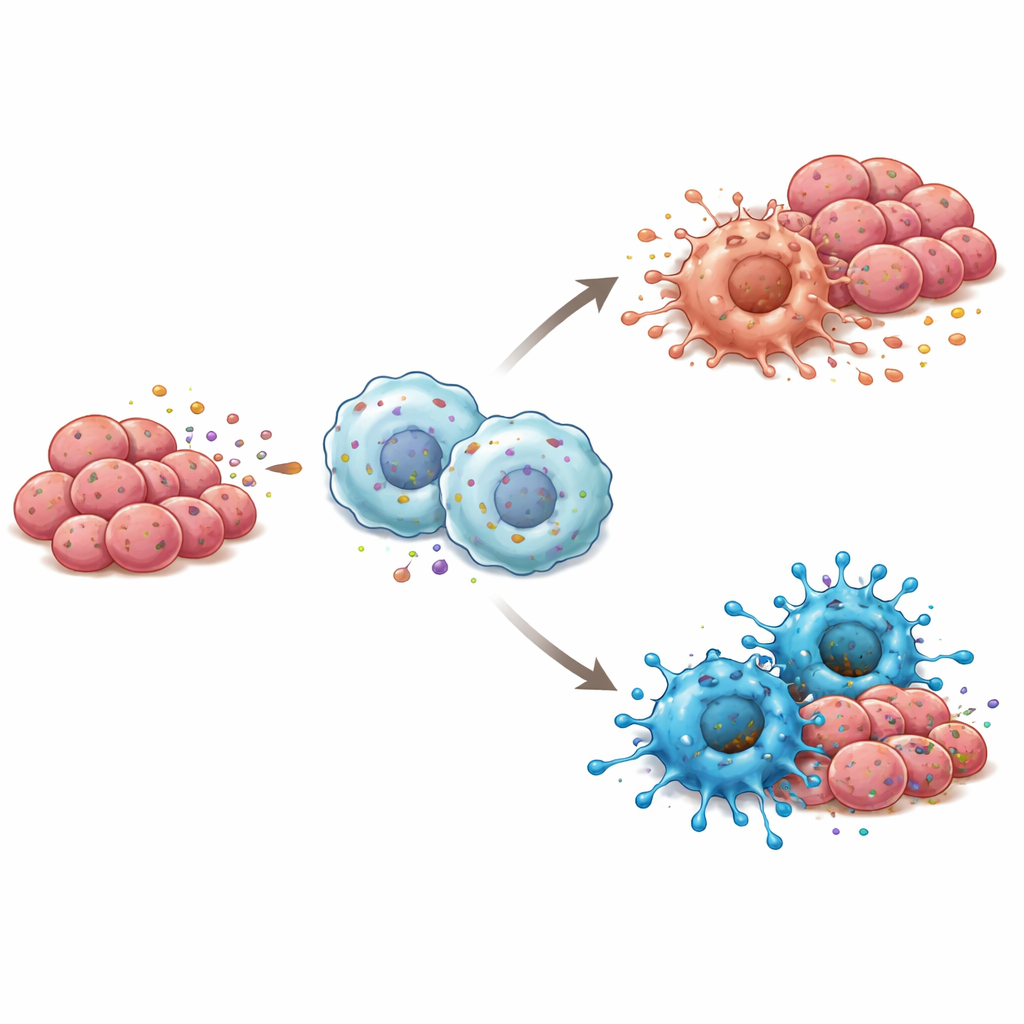
导致免疫转变的信号通路
为理解RBP4如何推动巨噬细胞对肿瘤采取更敌对的态度,研究者检查了这些免疫细胞中被激活的内部报警系统。他们发现RBP4刺激了巨噬细胞表面的一个感受器TLR4,并进而激活了NF-κB——驱动炎症反应的主开关。用化学抑制剂阻断TLR4可以关闭这一连锁反应,并阻止巨噬细胞在RBP4存在下转向M1状态。在小鼠实验中,由富含RBP4的舌癌细胞与巨噬细胞混合形成的肿瘤生长更慢,且含有更多M1型细胞,并伴随更强的TLR4和NF-κB活性,这进一步支持该通路对RBP4免疫效应的关键作用。
这对未来治疗意味着什么
综合来看,这项工作将RBP4描绘为对舌癌具有双向抑制作用的因子:在肿瘤细胞内部,它降低了过度活跃的生长回路;在肿瘤的“邻里”中,它有助于将巨噬细胞转化为更警觉的防御者。尽管仍有许多问题未解——例如RBP4如何确切与其靶点相互作用以及如何安全地提高其水平——该研究表明恢复或模拟RBP4的作用,既可减缓肿瘤扩张,又可增强机体对肿瘤的免疫压力。对患者而言,这提出了未来治疗的前景:不仅切除肿瘤,还通过重塑其内部线路和局部“生态系统”来防止复发。
引用: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
关键词: 舌癌, RBP4, 肿瘤微环境, 巨噬细胞, PI3K AKT通路