Clear Sky Science · zh
慢性炎症通过ADAM10介导的CX3CL1切割促进胃癌进展
为何长期胃部刺激至关重要
许多人因感染、饮食或其他健康问题多年承受持续的胃部刺激。这种持续的低度刺激被称为慢性炎症,是胃(胃癌)这一全球致死性较高的癌症的隐性风险因素。本文总结的研究提出了一个明确的问题:慢性炎症如何促使早期胃肿瘤更快生长并扩散?通过追踪一种特定的化学信号及激活它的酶,研究人员揭示了一个未来治疗可能针对的薄弱环节。
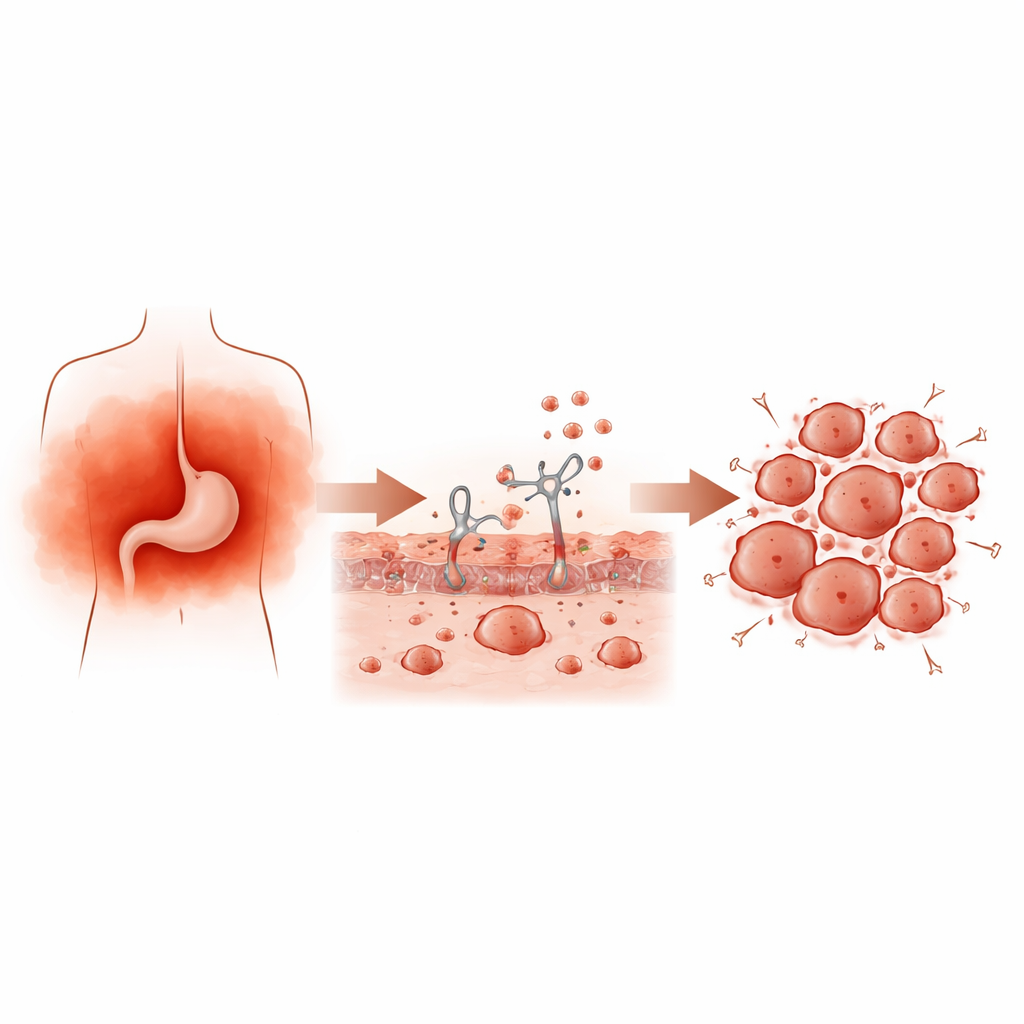
从刺激到更快生长的肿瘤
为了模拟长期炎症,研究团队反复用能触发免疫反应的物质处理小鼠,然后在皮下植入胃癌细胞。与对照动物相比,处于慢性炎症的小鼠长出了更大、更重、充满分裂细胞和免疫细胞浸润的肿瘤。在细胞培养实验中,从具有不同炎症水平的大鼠体内提取的血清使人类胃癌细胞更强烈地增殖并形成集落。这些结果共同表明,体内循环的炎性信号可以直接加速肿瘤生长。
寻找关键的致病信号
下一步是弄清哪些炎性信使分子最具危害性。研究人员使用广谱蛋白质阵列,比对了来自有炎症和无炎症小鼠肿瘤中的多种细胞因子,发现有九种明显升高。通过交叉检验公共患者数据集,他们锁定了一个突出候选分子:CX3CL1,一种帮助引导免疫细胞的趋化因子。CX3CL1在胃肿瘤中的水平高于正常胃组织,在更晚期的肿瘤中特别升高,并与患者更差的生存率相关。在小鼠肿瘤中的测量证实,慢性炎症在局部提升了CX3CL1水准,提示这一单一信号可能有助于解释炎症与不良预后之间的联系。
哪些细胞发送并接收该信号?
通过单细胞RNA测序,研究者在肿瘤内逐细胞绘制了基因活性图谱。他们发现CX3CL1主要由癌细胞自身产生,而非周围的免疫或支持细胞。其配对受体CX3CR1分布在几种细胞类型中,但在慢性炎症条件下在肿瘤细胞上的表达更为显著。一个在炎症肿瘤中扩增的特定肿瘤亚群表现出高CX3CL1表达以及增强的蛋白产出和生长特征。在体外实验中,向胃癌细胞直接添加纯化的CX3CL1可提高其存活、集落形成和迁移能力。阻断CX3CR1能削弱这些效应,表明癌细胞既发送也响应这一促进生长的信号。
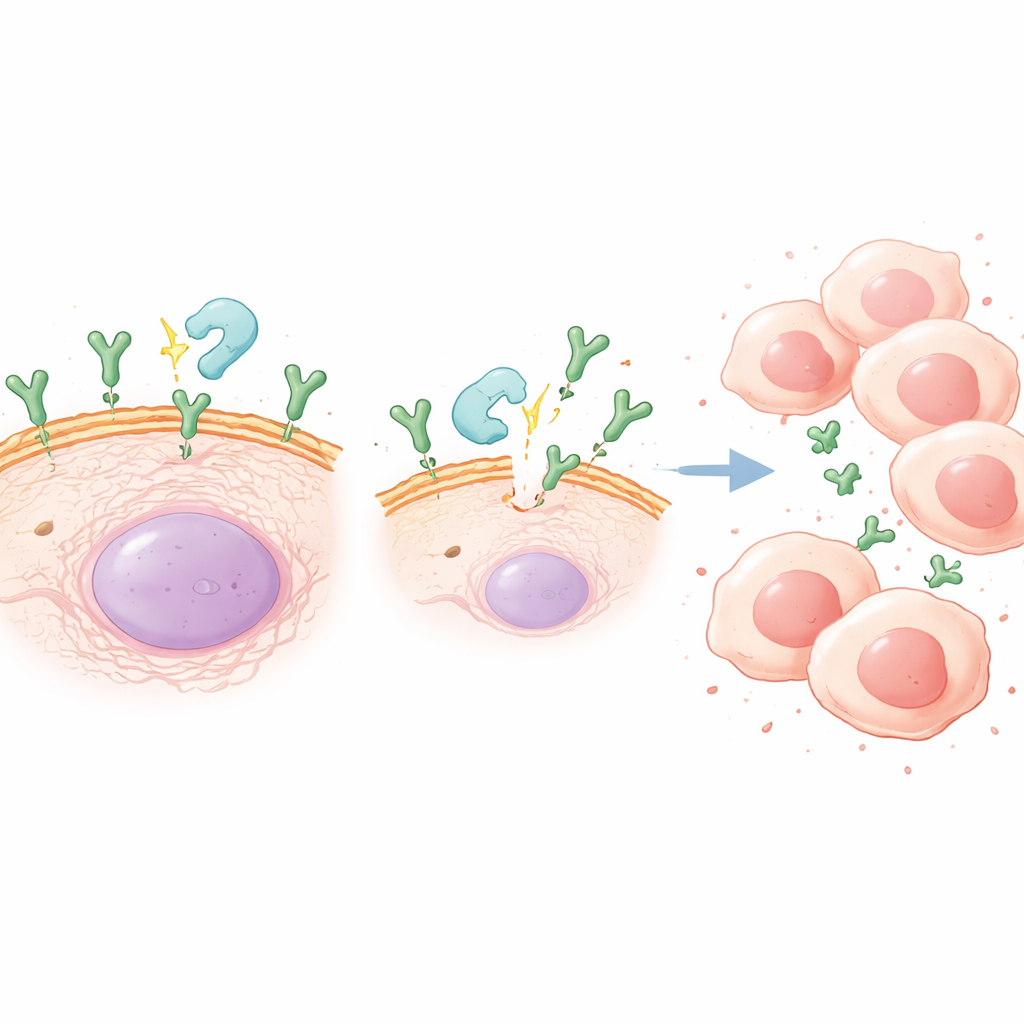
放大危险的酶
CX3CL1既有锚定在细胞膜上的形式,也有可在组织中扩散的可溶形式。可溶形式由一种名为ADAM10的酶切割膜结合型产生。研究发现,慢性炎症在小鼠肿瘤以及在实验室中暴露于炎性触发物的胃癌细胞中提高了ADAM10水平。当研究者用ADAM10抑制剂处理细胞时,周围液体中可溶CX3CL1的含量下降,且炎症驱动的癌细胞增殖和迁移的增加大体被逆转。在患有慢性炎症的小鼠中,阻断ADAM10减缓了肿瘤进展并降低了肿瘤中的CX3CL1水平,进一步支持了这一酶介导的“剪切”步骤是关键的观点。
这对有慢性胃部问题的患者意味着什么
综合来看,这项工作勾勒出一条清晰的事件链:胃及其周围的持续炎症激活了胃癌细胞中的ADAM10;随后ADAM10剪切产生更多可溶CX3CL1,而这些可溶因子又反馈作用于癌细胞,帮助其增殖和迁移。对普通读者而言,这类似于被刺激的环境教会肿瘤细胞既高声发送又接收一种促进生长的信息。因为ADAM10和CX3CL1都是可识别的分子并已有药物研究兴趣,新描述的“ADAM10/CX3CL1轴”为旨在减缓或预防炎症驱动胃癌进展的治疗提供了可行的靶点。
引用: Song, Z., Liu, Y., Wang, Z. et al. Chronic inflammation promotes gastric cancer progression via ADAM10-mediated cleavage of CX3CL1. Sci Rep 16, 9169 (2026). https://doi.org/10.1038/s41598-026-39743-6
关键词: 胃癌, 慢性炎症, 趋化因子, 肿瘤微环境, ADAM10