Clear Sky Science · zh
镉暴露通过抑制 hsa_circ_0075684/miR-363-3p/KLF4 信号通路诱导肾脏纤维化
为何这种隐蔽金属威胁重要
镉是一种有毒重金属,悄然通过食物、香烟烟雾和工业污染渗入我们的生活。一旦进入体内,它能在体内滞留数十年,尤其容易在肾脏中蓄积。本研究探讨长期镉暴露如何在肾组织中留下疤痕,并锁定了一个微小的分子回路,可能作为早期危险信号——这为预防慢性肾脏病,而不是事后治疗提供了希望。
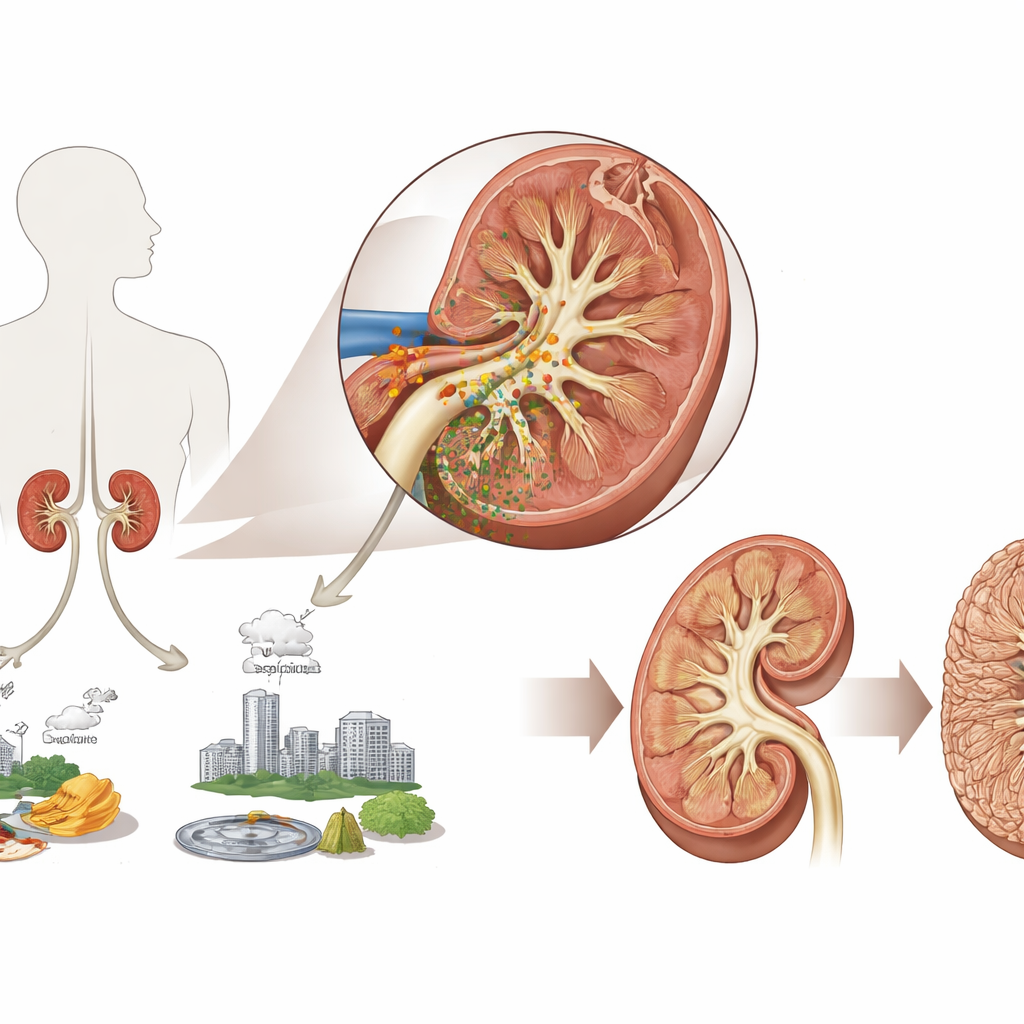
逐渐加剧的肾损伤
肾脏充当身体的过滤器,清除血液中的废物。然而,镉会在这些过滤器中多年累积,并且与慢性肾脏病密切相关。作者指出,全球慢性肾病病例在上升,一旦镉沉积在肾脏中目前没有有效的清除方法。他们认为,与其专注于清除镉,不如寻找检测并早期中断损伤的方法——尤其是纤维化过程,即健康组织被僵硬的瘢痕组织逐步取代,从而削弱肾功能。
微小的 RNA 信号与保护开关
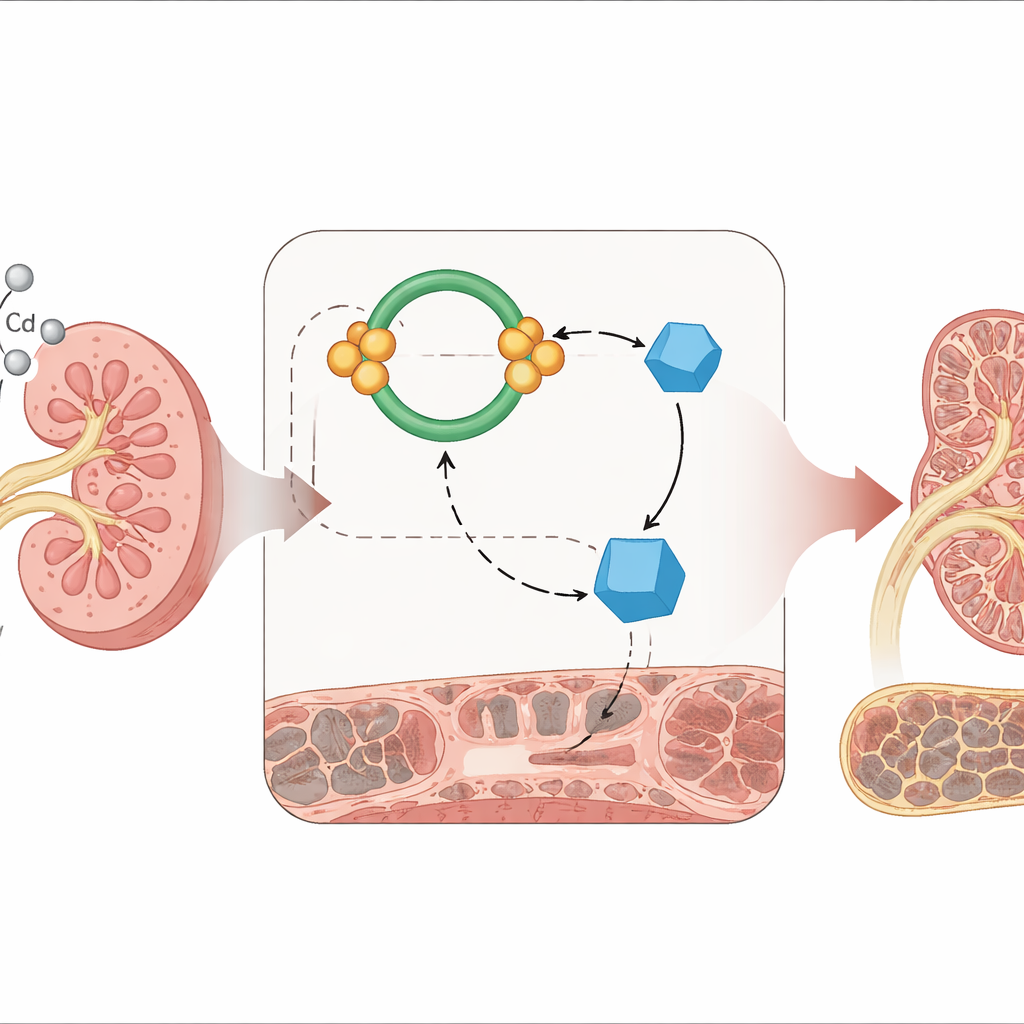
研究者聚焦于一种名为 miR-363-3p 的小型调控分子,它属于通过短小 RNA 片段微调基因活性的家族。作者早期的工作显示,这种 RNA 在长期镉中毒的工人中水平升高。利用大型公共基因数据库,他们在镉暴露的肾组织中寻找围绕 miR-363-3p 的更广泛调控回路。他们鉴定出一个三部分通路:一种可“吸收” miR-363-3p 的环状 RNA(hsa_circ_0075684)、miR-363-3p 本身,以及一种名为 KLF4 的蛋白,后者有助于保护肾细胞免受瘢痕形成。总体来看,这三者像一个分子开关,维持对纤维化的抑制。
从培养皿到实验小鼠
为检验这一假设,研究团队将人类肾小管细胞暴露于逐渐升高剂量的镉。随着镉水平上升,细胞出现了纤维化的典型特征:与瘢痕相关的蛋白升高,而帮助细胞粘附并维持正常结构的蛋白下降。与此同时,miR-363-3p 水平上升,KLF4 与该环状 RNA 水平下降。基因学实验显示,miR-363-3p 能直接结合 KLF4 并抑制其表达,而环状 RNA 通常能结合并“束缚”miR-363-3p,防止其沉默 KLF4。当研究者增强 miR-363-3p 时,瘢痕相关蛋白激增且 KLF4 下降;当他们阻断 miR-363-3p 或增加环状 RNA 时,即使存在镉,KLF4 也回升,纤维化标志物减轻。
在活体肾脏中证实损伤
研究者随后转向小鼠模型,以观察这一分子模式是否也在活体动物中出现。小鼠被口服给予镉三个月,剂量选取以模拟长期环境暴露。显微镜下,镉处理小鼠的肾脏显示出明显的纤维化变化——染成蓝色的胶原纤维充填在小管间隙。生化检测与细胞培养结果一致:瘢痕相关蛋白上升,保护性蛋白 KLF4 下降,肾脏中 miR-363-3p 水平增加,支持该通路在缓慢、真实世界的镉损伤过程中具有活性。
对保护肾脏意味着什么
综合来看,结果表明镉通过扰乱环状 RNA、微小 RNA 与保护性蛋白之间的微妙平衡来促进肾脏纤维化。当镉降低环状 RNA 与 KLF4 时,miR-363-3p 得以自由推动细胞走向纤维化。对非专业读者而言,关键讯息是,早期的分子变化——远在症状出现之前——或许有朝一日可作为血液或尿液检测的预警信号,用于监测有镉暴露风险的人群。尽管仍需更多临床研究,尤其是对人类患者的研究,这一新绘制的通路为将来检测并可能在不可逆瘢痕形成前削弱镉驱动的肾损伤指明了方向。
引用: Zhou, J., Huang, Y., Li, G. et al. Cadmium exposure induces renal fibrosis by inhibiting hsa_circ_0075684/miR-363-3p/KLF4 signaling pathway. Sci Rep 16, 8754 (2026). https://doi.org/10.1038/s41598-026-39715-w
关键词: 镉暴露, 肾脏纤维化, 微小RNA, 环境毒理学, 慢性肾脏病