Clear Sky Science · zh
外周血CD14+单核细胞在乳腺癌腔内亚型中的作用:初步研究与候选生物标志物蛋白概述
为何血细胞对乳腺癌重要
医生确诊乳腺癌时通常依赖来自肿瘤组织的样本。但如果一次简单的抽血也能提示患者的乳腺癌类型及疾病状态呢?本研究探讨了这一可能性,通过检测循环血中特定免疫细胞内的蛋白,考察这些细胞是否携带不同腔内型乳腺癌的分子“回声”。
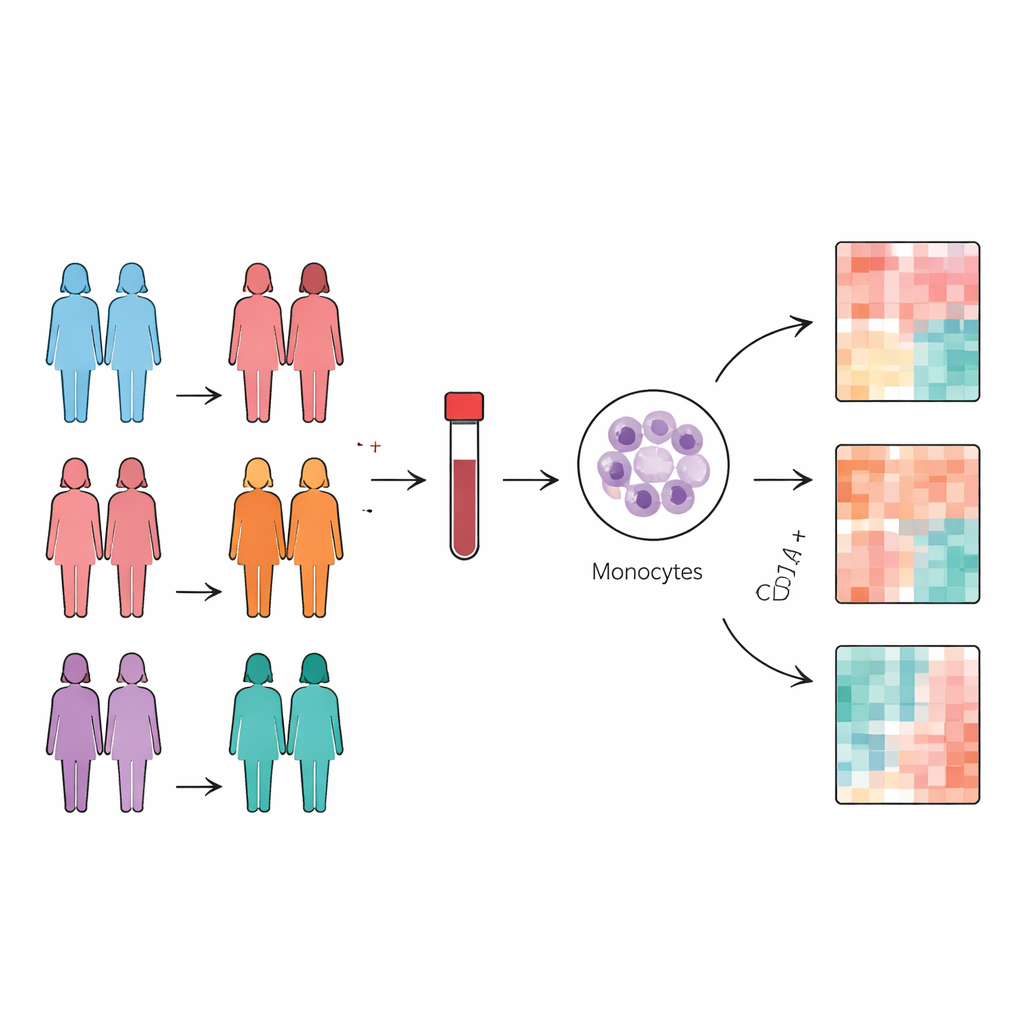
关注在体内巡逻的哨兵
研究者聚焦于CD14+单核细胞,这是一类在血流中巡逻并参与塑造肿瘤微环境的白细胞。他们从患有三种密切相关乳腺癌类型的女性——腔内A型、无HER2的腔内B型以及伴HER2的腔内B型——以及有良性乳腺疾病的女性和健康志愿者处采集血样。研究不是查看基因,而是采用高分辨率质谱对来自每位受试者的纯化单核细胞内数千种蛋白进行谱系分析,然后比较各组间蛋白水平的差异。
癌症亚型间的共同蛋白指纹
团队发现,相较于健康对照,多个蛋白在所有腔内乳腺癌组中一致改变。其中一些如SRSF1呈上调,已知可支持细胞生长与存活。另一些蛋白,包括CSTB以及某些角蛋白(KRT2 和 KRT5),则下调或在亚型间呈现相反的变化,暗示细胞结构和应激反应的改变。与脂质转运相关的蛋白(APOB、APOE)、血小板与凝血活动相关的蛋白(ITGA2B)以及参与酸碱调节的蛋白(HEL-S-11,一种碳酸酐酶)也发生变化。总体来看,这些变化表明患腔内乳腺癌女性的单核细胞呈现出一种独特的、与癌症相关的状态,可通过血液检测到。
每种肿瘤类型的不同内部机制迹象
除了个别蛋白外,研究者还考察了更广泛的细胞通路。在腔内A型病例中,单核细胞表现出激素相关信号、钙离子处理以及免疫细胞由血液向组织迁移等过程活性降低——这些过程与免疫细胞反应及肿瘤生长有关。在无HER2的腔内B型中,与蛋白合成工厂(核糖体)相关的通路更为活跃,而与细胞回收与降解的隔室(溶酶体)相关的通路则活性降低,提示细胞构建与分解成分方式的转变。在伴HER2的腔内B型中,模式则指向由转录因子MYC调控的基因,这与快速细胞增殖有关。这些通路特征强调每种腔内亚型都在循环免疫细胞上留下各自的分子印记。
从蛋白面板走向潜在的血液检测
若干改变的蛋白——尤其是APOB、APOE、CSTB、HEL-S-11、SRSF1和ITGA2B——在作为分类器评估时对区分腔内乳腺癌患者与健康对照表现出一定的判别能力。尽管没有单一蛋白能单独达到足够的准确性,但这些标志物的组合可能构成用于微创检测的面板。值得注意的是,角蛋白KRT2和KRT5在患有良性乳腺疾病的女性中也发生了变化,提示部分信号反映的是一般性乳腺病理而非仅是癌症,这凸显了在设计标志物面板时需要谨慎。
这项早期工作对患者的意义
该研究属于探索性初步工作,基于相对小且不均衡的患者群体,作者强调其发现为初步结果,需要在更大、独立的队列中验证。即便如此,研究表明循环中的免疫细胞携带与乳腺肿瘤及其亚型相关的丰富蛋白信息。如果未来研究证实并优化这些基于单核细胞的蛋白特征,它们最终可能支持血液检测工具,作为组织活检的补充,帮助更精确地分类腔内乳腺癌,并以更少侵入性的检测指导更个体化的治疗决策。
引用: Alexovič, M., Bober, P., Marcin, M. et al. Peripheral blood CD14 + monocytes in luminal breast carcinoma subtypes: in preliminary research and overview of candidate biomarker proteins. Sci Rep 16, 8090 (2026). https://doi.org/10.1038/s41598-026-39686-y
关键词: 腔内型乳腺癌, 血液生物标志物, 单核细胞, 蛋白质组学, 免疫反应