Clear Sky Science · zh
骨髓间充质干细胞外泌体通过 circRNA_43350/miR-342-5p 调控 COPD 中肺微血管内皮细胞凋亡
为何保护脆弱的肺小血管至关重要
慢性阻塞性肺疾病(COPD)会逐步剥夺患者的呼吸能力和独立性。香烟烟雾不仅刺激气道,还会损伤包绕气囊、负责将氧气输送到血液的小而脆弱的血管网络。在这项研究中,科学家们探讨骨髓干细胞释放的天然修复“包裹物”是否能保护这些易损的肺血管免受烟雾伤害,以及为何这种保护在 COPD 中显得减弱。他们的发现指出了一个微小的环状遗传环路,像分子海绵一样吸附有害信号,帮助肺血管细胞存活。
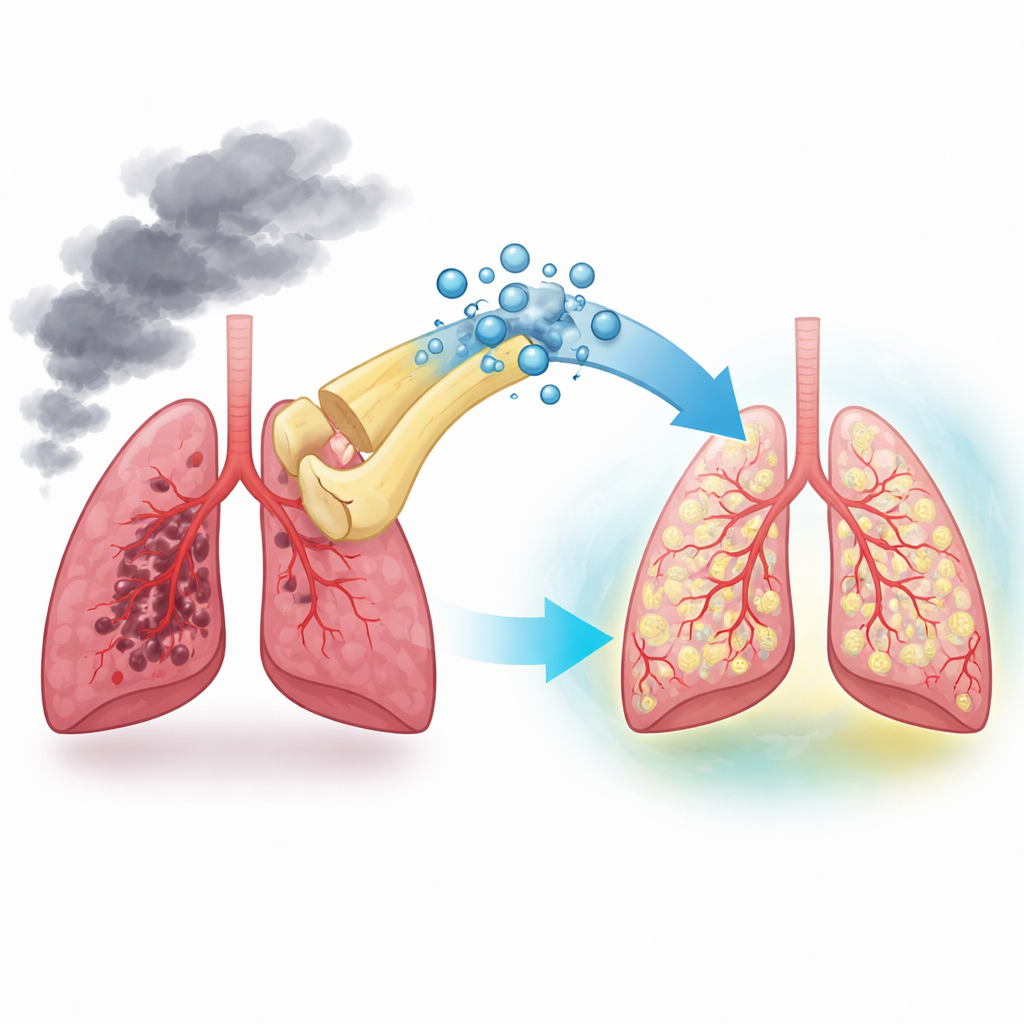
来自干细胞的小型修复包裹物
骨髓间充质干细胞以其抑制炎症和支持组织修复的能力著称,既可以分化成其他细胞类型,也会释放出称为外泌体的微小囊泡。这些外泌体携带蛋白质和遗传物质,能被其他细胞摄取,作为现成的指令。研究人员首先从小鼠骨髓干细胞中分离出外泌体,并确认其具有预期的形态和尺寸。随后他们证明,这些外泌体可以被肺微血管内皮细胞——即 COPD 中受损的肺小血管内膜细胞——有效吞噬。
外泌体减轻香烟烟雾对肺的损伤
为模拟吸烟相关的 COPD,研究团队用香烟烟雾提取物处理培养的肺血管细胞,并建立了烟雾诱导的肺气肿小鼠模型。在这两种系统中,烟雾都显著增加了血管内膜细胞的死亡,并导致肺泡扩大、结构破坏。当加入来自健康干细胞的外泌体时,关键存活蛋白的平衡朝有利于细胞存活的方向转变,较少的内皮细胞进入程序性死亡,且小鼠肺部的类似肺气肿的损伤部分被逆转。这些结果表明,健康干细胞外泌体携带的因子可以直接保护肺小血管并减轻结构性肺损伤。
保护作用核心的环状遗传环路
接着,科学家在外泌体货物中搜索健康与 COPD 条件下的差异,重点关注环状 RNA——一种新发现的稳定、闭合的遗传分子。在近 1.4 万种检测到的环状 RNA 中,有一种称为 circRNA_43350 的分子格外显著:它在健康小鼠的外泌体和肺组织中丰度较高,而在 COPD 中显著减少。在受烟雾处理的血管细胞中人工提升 circRNA_43350 水平可降低细胞死亡率并恢复更健康的存活蛋白谱。在 COPD 小鼠中,将额外的 circRNA_43350 送入气道可以减轻类似肺气肿的病变并降低肺内膜细胞死亡,指向该环状 RNA 的关键保护作用。
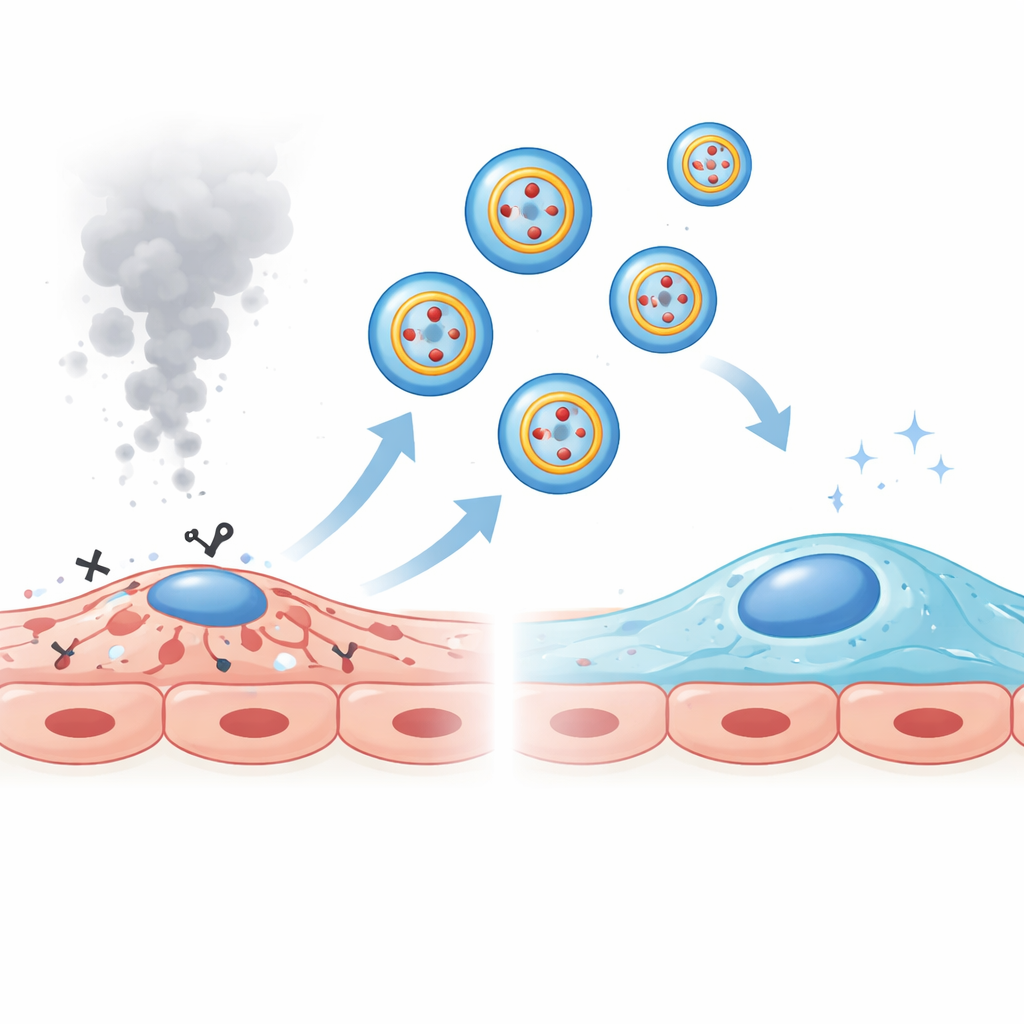
像海绵一样吸附有害信号的分子
环状 RNA 常通过结合小型调控 RNA(即微小 RNA)来发挥作用,阻止它们沉默靶基因。借助预测工具和分子报告实验,研究团队发现 circRNA_43350 能直接结合一种名为 miR-342-5p 的微小 RNA。在患者、COPD 小鼠以及烟雾处理的血管细胞中,miR-342-5p 水平均高于正常,阻断该微小 RNA 可减少内皮细胞死亡。研究者证明 circRNA_43350 与 miR-342-5p 互相制约:增加 circRNA_43350 会降低 miR-342-5p 并保护细胞,而增加 miR-342-5p 则削弱 circRNA_43350 的保护作用并促进细胞死亡。这种拉锯表明,当 COPD 的外泌体中失去 circRNA_43350 时,miR-342-5p 得以自由发挥,推动脆弱的肺血管细胞走向损伤。
对未来 COPD 治疗的意义
总体而言,这些发现描绘了这样一幅图景:健康的骨髓干细胞将富含 circRNA_43350 的保护性外泌体运送到肺部,该环状 RNA 吸附过量的 miR-342-5p,帮助肺小血管在香烟烟雾压力下存活。而在 COPD 中,外泌体中 circRNA_43350 含量减少,削弱了这一防护,使损伤和肺气肿更易发生。通过锁定这一显微修复环路,该研究为治疗提供了新思路:设计工程化外泌体或其他能恢复 circRNA_43350 或抑制 miR-342-5p 的疗法,未来或可帮助保护 COPD 患者的肺结构和呼吸功能。
引用: Zeng, Y., Song, Q., Yang, L. et al. BMSCs exosomes regulate pulmonary microvascular endothelial apoptosis via circRNA_43350/miR-342-5p in COPD. Sci Rep 16, 8183 (2026). https://doi.org/10.1038/s41598-026-39678-y
关键词: COPD, 肺内皮细胞, 间充质干细胞外泌体, 环状 RNA, 微小 RNA