Clear Sky Science · zh
使用小鼠CD25特异性重组免疫毒素在非人灵长类大脑中靶向特定神经元类型
这项脑研究为何重要
理解特定神经细胞群如何控制运动、情绪和行为,是治疗帕金森病和自闭症等疾病的关键。但大脑如同一片交织密集的森林,大多数工具往往同时砍倒许多树木。该研究提出了一种只移除猴子大脑中所选神经元类型且对周围组织损伤最小的方法,为更精确地研究特定回路如何塑造行为和疾病打开了大门。
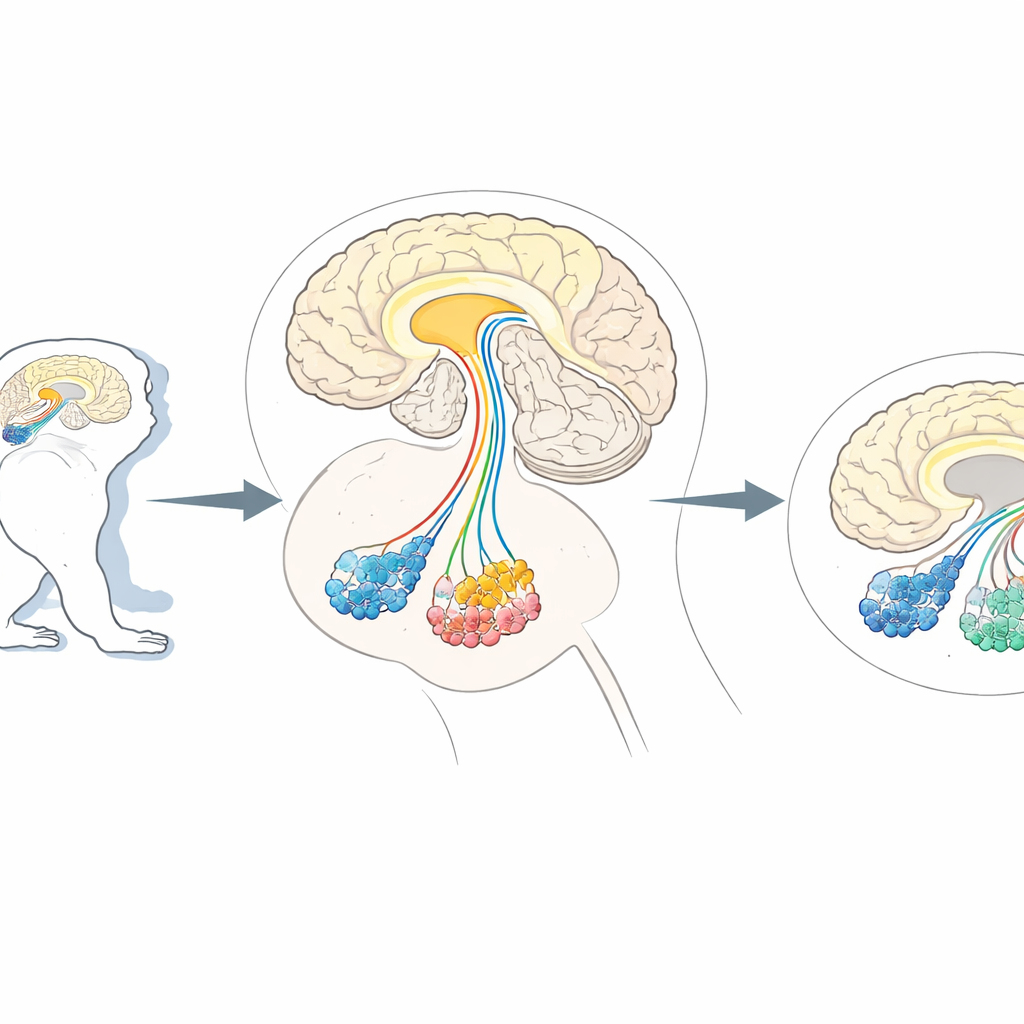
对精确“大脑细胞修剪”的需求
研究人员常用非人灵长类动物,如绒猴和猕猴,因为它们的大脑组织方式与人类相似。这些动物是研究影响高级脑功能的疾病(从帕金森样运动障碍到类似自闭症的社交行为变化)的重要模型。现有方法可以沉默或刺激特定通路,但在这些复杂的大脑中真正仅移除某一类型神经元而不伤及他者仍然困难。早期在小鼠中的工作使用了一种技巧:让被选中的神经元表达一种称为CD25的人源细胞表面标记,该标记可被设计毒素识别并仅杀死这些带标记的细胞。然而,这一相同的标记在灵长类免疫细胞乃至可能在脑细胞中自然存在,增加了毒素在猴子体内攻击错误目标的风险。
设计更安全的分子手术刀
作者着手构建一种为灵长类使用而定制的新型分子手术刀。他们没有针对人源CD25,而是聚焦于小鼠版本,因为它与猴子天然CD25的相似性要低得多。他们首先用小鼠CD25蛋白免疫兔子,并采用芯片方法筛选出那些能强烈结合小鼠CD25但不结合人源形式的单个兔源细胞。从中鉴定出一株表现突出的抗体,命名为RMAb-52,具有很高的亲和力。随后,他们将该抗体的关键部分与铜绿假单胞菌(Pseudomonas)来源的毒性片段拼接,构建出单一的工程“免疫毒素”蛋白,命名为anti-mCD25-PE38。
检验该工具的性能
在试管实验中,新型免疫毒素对小鼠CD25的结合远强于对人源CD25,证实了其选择性。当该毒素作用于被工程化携带小鼠CD25的培养细胞时,在极低剂量下即大幅降低了这些细胞的存活率,而携带人源CD25的细胞则不受影响。接着,团队将研究推进到活体绒猴。利用一种沿神经纤维逆行传播的特殊病毒载体,他们把小鼠CD25基因导入从黑质(substantia nigra)向纹状体投射的多巴胺产生神经元——这一通路对运动控制至关重要。在给病毒足够时间使这些神经元表达标记后,他们将anti-mCD25-PE38蛋白直接注入目标的中脑区域。
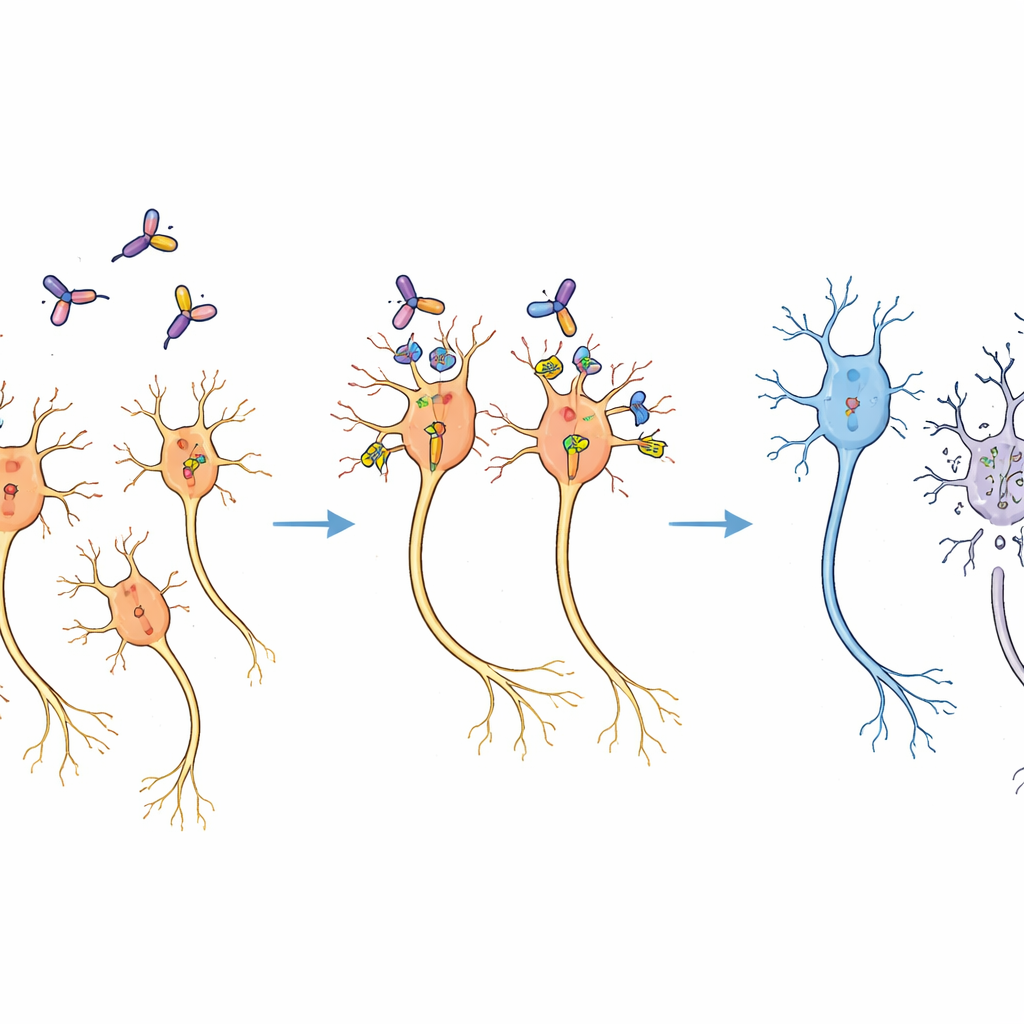
选择性丧失而无广泛损伤
治疗两周后,来自绒猴的大脑切片显示了清晰的结果。在接受免疫毒素的一侧,多巴胺神经元数量(以合成多巴胺的酶染色为标记)降至未处理侧的约三分之二。然而显微镜下周围脑组织外观正常,其他也接受病毒载体的脑区未见明显细胞丧失。先导实验已确定了避免非特异组织损伤的剂量范围,而所选剂量明显落在这一安全窗口内。细胞丧失的分布模式与病毒和毒素的预期扩散一致,表明神经元被消除是因为它们被工程化表达了小鼠CD25,而不是毒素对细胞进行非特异性伤害。
这对未来脑研究的意义
对非专业读者而言,关键信息是研究者已构建出一种在灵长类大脑中高度选择性删除特定神经元群的“删除按钮”。通过将逆行病毒递送系统与小鼠特异性免疫毒素结合,他们可以移除明确的通路——例如与帕金森病相关的多巴胺回路——同时保护邻近细胞。该策略避免了与动物自身CD25发生危险交叉反应,尤其适用于该天然受体存在或在疾病中升高的情况。长期来看,这种方法将有助于科学家绘制单一路径在大脑连线中如何影响运动、决策和精神病理症状的图谱,使我们更接近能针对性调整故障回路而非广泛影响整个大脑的治疗方案。
引用: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
关键词: 非人灵长类神经科学, 免疫毒素靶向, 多巴胺神经元, 绒猴大脑回路, 帕金森病模型