Clear Sky Science · zh
缺氧诱导因子1α通过TIMP3介导的血管生成和侵袭调控在膀胱癌进展中发挥双重作用
为何缺氧肿瘤重要
癌细胞常常生长过快,以至于超过了血液供应,使肿瘤的部分区域处于缺氧状态。这种低氧环境迫使细胞启动生存程序,可能使癌症更难治疗。在膀胱癌——一种常见的泌尿系统肿瘤中——科学家长期怀疑由名为HIF-1α的蛋白控制的氧感应程序主要有助于肿瘤生长和转移。本研究对其进行了更细致的探查,发现了一个令人惊讶的转折:在某些条件下,降低HIF-1α反而会使膀胱癌细胞更具侵袭性,而另一个蛋白TIMP3正处于这一悖论的核心。
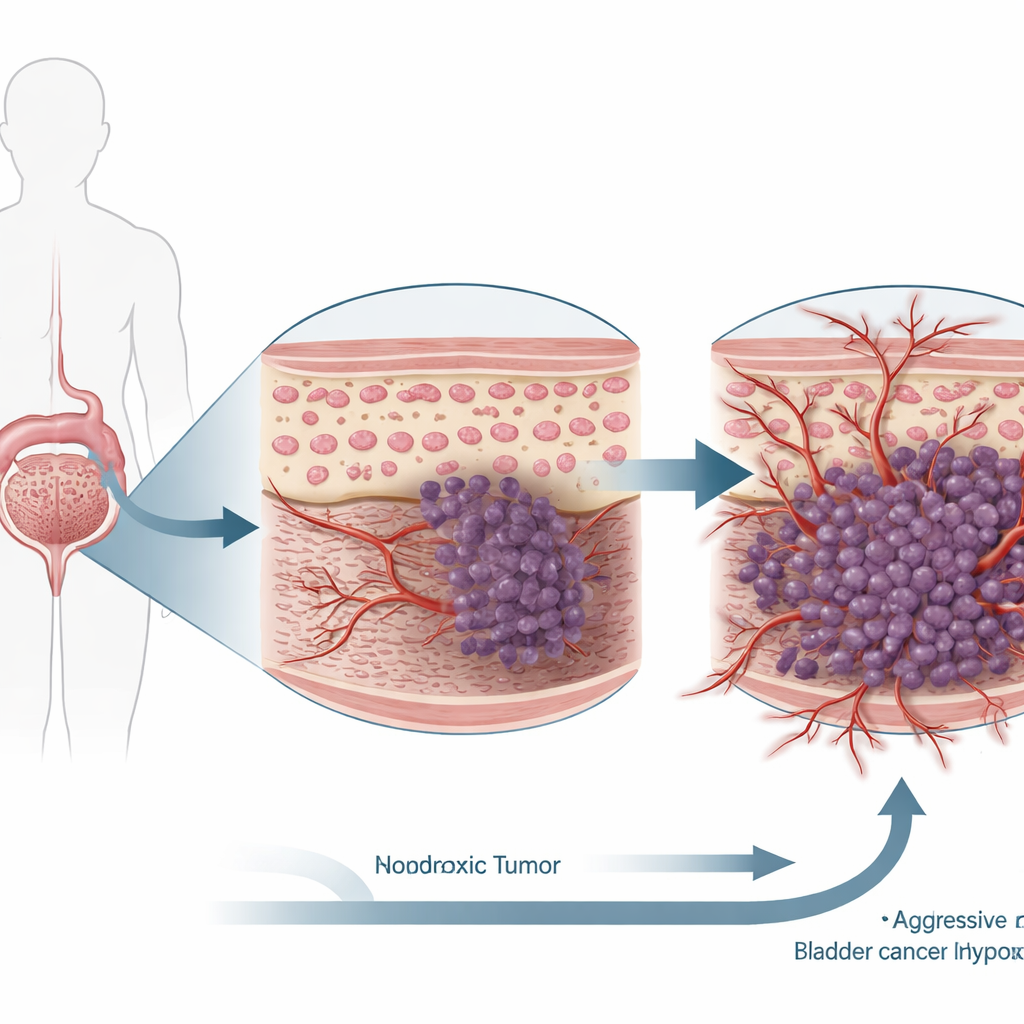
对膀胱癌细胞的深入观察
研究人员使用了两种公认的人类膀胱癌细胞系,并将它们置于常氧或模拟肿瘤内氧气匮乏的缺氧环境中。随后他们利用基因学工具下调这些细胞中的HIF-1α,并测量此变化如何影响癌症的基本行为:细胞增殖速度、凋亡倾向以及迁移、穿越屏障侵袭和促进新血管形成的能力。同时,他们还检查了患者的膀胱肿瘤样本,以比较肿瘤组织与邻近正常膀胱组织中HIF-1α和TIMP3的水平。
低氧下的意外角色反转
患者样本证实,膀胱肿瘤中HIF-1α确实高于正常组织,与其作为促进肿瘤因子的名声一致。然而,在缺氧条件下的细胞实验中,下调HIF-1α却产生了与多数预期相反的效果。当HIF-1α被敲低且氧气稀缺时,癌细胞随时间表现出更快的生长、较低的程序性细胞死亡率,并在迁移和穿越模型屏障的侵袭能力上增强。它们还释放出促使血管细胞形成更为致密、范围更广管状网络的信号,这是血供增加的标志。总之,在低氧情境中减少HIF-1α使膀胱癌细胞表现得更具恶性。
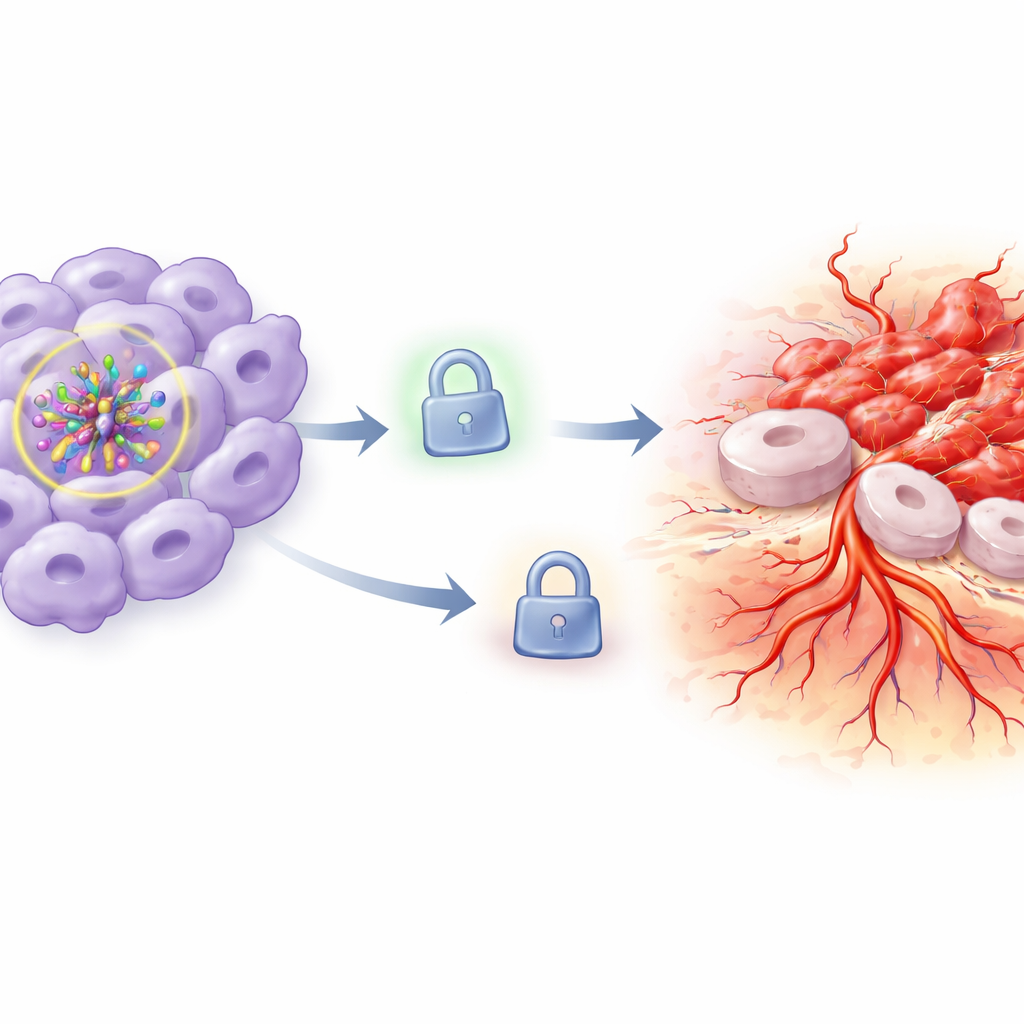
肿瘤扩散失去的刹车
为了解这一现象的原因,团队将注意力集中在TIMP3上——一种通常通过阻断分解周围基质的酶来抑制组织降解和新血管生成的蛋白。在维持常氧的HIF-1α降低细胞中,TIMP3水平相对保持较高。但当氧气水平下降时,TIMP3蛋白急剧降低。这一TIMP3的丧失与观察到的侵袭和血管形成增加相吻合:当刹车变弱,癌细胞更容易重塑周围环境并扩展。研究者随后在缺氧且HIF-1α被敲低的情况下,强制让细胞表达额外的TIMP3。恢复TIMP3部分或几乎完全逆转了这种侵袭性行为:细胞生长减少、凋亡增加、迁移与侵袭下降,并且诱导的血管样管道更少且更短。
对未来治疗的意义
这些发现表明,HIF-1α在膀胱癌中具有双重性。一方面,它在肿瘤中的总体水平较高并推动已知的有利于肿瘤的程序;另一方面,在严重缺氧时似乎有助于维持TIMP3的保护性存在。在那种情况下去除HIF-1α可能无意中降低TIMP3,从而释放出更多侵袭性和促血管生成的行为。就治疗而言,这意味着单纯阻断HIF-1α可能产生适得其反的效果,除非同时有办法维持TIMP3或其他类似的“刹车”。这项工作强调了理解不仅是单一靶点,而是塑造肿瘤对其严酷低氧环境反应的更广泛制衡网络的重要性。
引用: Wang, X., Guo, J., Zhang, R. et al. Hypoxia-inducible factor 1α exerts dual roles in bladder cancer progression through TIMP3-mediated regulation of angiogenesis and invasion. Sci Rep 16, 8425 (2026). https://doi.org/10.1038/s41598-026-39635-9
关键词: 膀胱癌, 肿瘤缺氧, HIF-1α, TIMP3, 血管生成