Clear Sky Science · zh
保加利亚乳杆菌(Lactobacillus delbrueckii subsp. bulgaricus)2038 与嗜热链球菌(Streptococcus thermophilus)1131 抑制聚苯乙烯纳米塑料通过肠上皮细胞的跨细胞通透和内吞
为什么微小塑料和酸奶细菌很重要
塑料废弃物不会凭空消失;随着时间推移,它会崩解成我们肉眼看不见的微小颗粒。这些纳米塑料如今出现在我们的食物、水源乃至体内。科学家担心这些颗粒可能穿过肠道上皮进入血液,从而在细胞内引发应激和损伤。本研究提出了一个充满希望的问题:常见的酸奶细菌能否帮助阻挡这些看不见的入侵者穿越肠壁并在体内扩散?
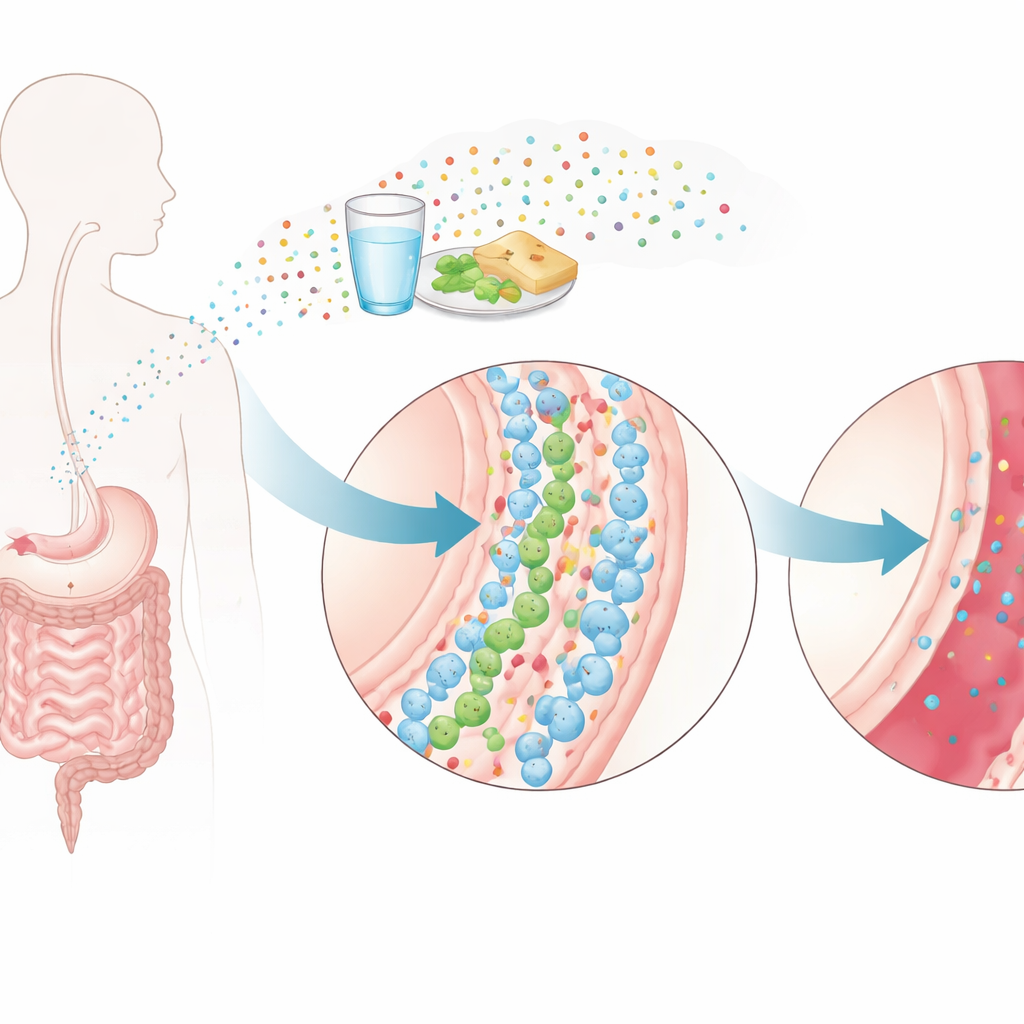
微小塑料的移动方式
研究者聚焦于聚苯乙烯纳米塑料,将其作为日常物品如食品包装和泡沫容器分解后所形成颗粒的代表。先前的研究表明,这些微粒可被吞入并被小肠上皮细胞摄取。进入细胞后,它们可能扰乱细胞机制,削弱肠与血液之间的屏障,并进一步转移到器官中。然而直到现在,还没有在肠壁层面上提出可行的办法来减缓或阻止这种内吞过程。
检验一种基于酸奶的防护
团队研究了两株广泛用于制作酸奶的乳酸菌:Lactobacillus delbrueckii subsp. bulgaricus 2038 和 Streptococcus thermophilus 1131。利用成熟的人小肠体外模型(Caco‑2 细胞单层),他们将细胞暴露于带荧光的聚苯乙烯纳米塑料,分别单独处理或与这些细菌共同作用。通过流式细胞术和高分辨率显微镜追踪荧光,他们测量了进入细胞的颗粒数量以及随后穿过细胞层到“血液侧”下方的数量。他们还测试了经热灭活的细菌,以判断是否需要活菌生长才能产生效果。
肠细胞的反应
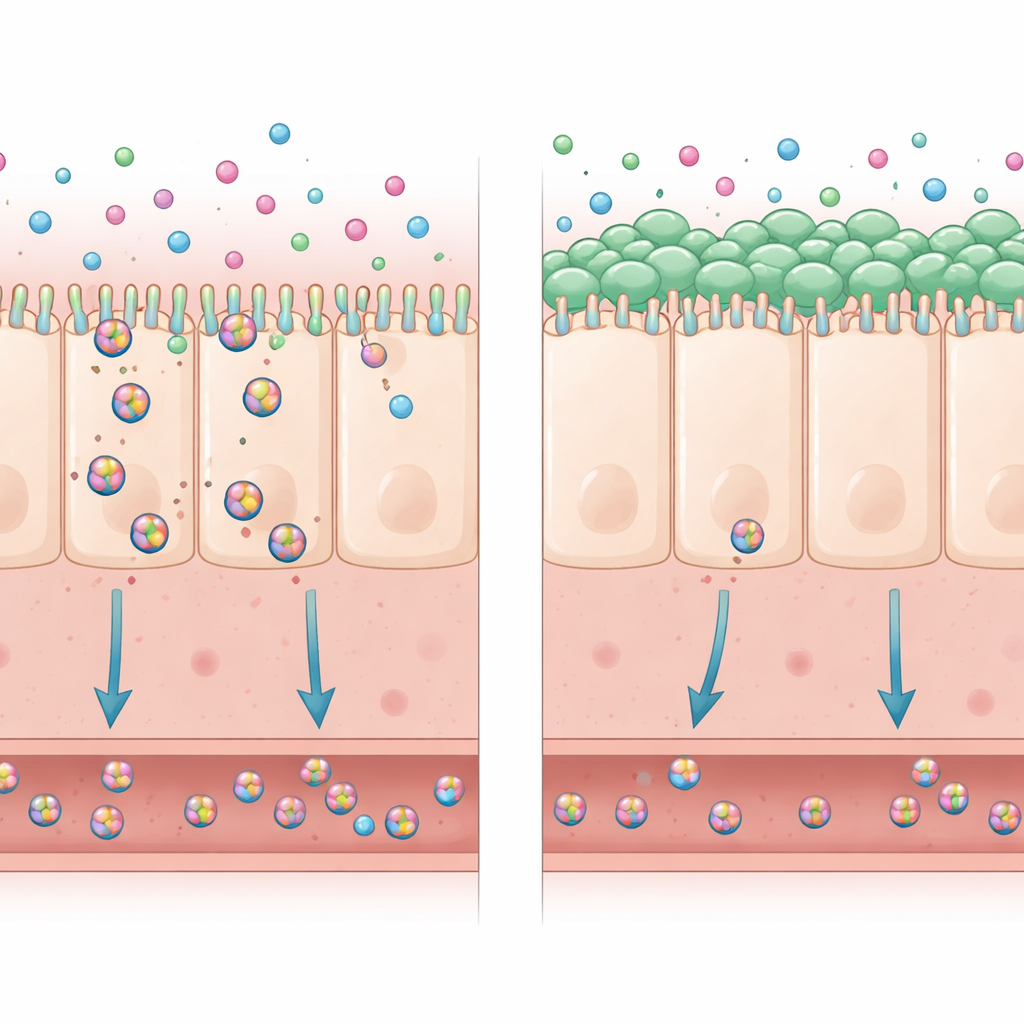
纳米塑料容易被肠道细胞吸收,主要通过细胞膜内陷并囊泡化的小体吞(主动摄取)途径。当这种情况发生时,基因表达模式发生了变化,表现出与氧化应激和降低的 DNA 修复能力一致的特征。研究者接着考察酸奶菌株如何改变这一过程。两种细菌——无论是活的还是热处理的——都显著减少了细胞内的纳米塑料量,并降低了穿过细胞层到达远侧的颗粒数量。重要的是,细菌并非通过与塑料发生聚集或简单地物理阻挡来发挥作用;即便在细胞预先处理细菌后再洗去,保护效应仍然存在。
关于保护机制的线索
由于细菌不需存活,作者得出结论认为它们细胞壁中稳定的成分很可能向肠细胞发出信号,从而降低塑料的摄取。先前与相关细菌的研究表明,它们可能通过作用于细胞表面的免疫感受器来调整细胞处理肠道物质的方式。在基因表达分析中,单独的纳米塑料削弱了一个关键的化学加工途径——葡糖醛酸化(glucuronidation),而该途径通常有助于肠细胞处理有益的植物性化合物。酸奶菌株部分防止了该途径的下降,这提示除了阻止塑料进入,它们还可能保护肠道处理益生营养物质的能力。
为何这两株尤为突出
并非所有酸奶细菌的表现都相同。当团队比较同两种物种中的若干菌株时,每一种都显示出降低纳米塑料进入的某种能力,但最初的酸奶起始株——L. bulgaricus 2038 和 S. thermophilus 1131——效果最为显著。这表明存在菌株特异性的性状,可通过筛选更多候选菌株来选择并优化,或许能获得更强的保护性。该研究在培养细胞中进行,因此尚不能证明食用酸奶会在真人体内阻挡纳米塑料,但它为未来的动物和人体试验提供了可检验的策略。
对日常健康的可能意义
简而言之,这项工作表明某些酸奶细菌可能有助于在肠道表面形成一层无形的防护,使纳米塑料更难侵入我们的体内并转移到易感器官。通过减少纳米塑料进入肠细胞的摄取以及它们穿过肠壁的通透,这些菌株或能降低与长期塑料暴露相关的细胞应激和炎症。尽管还有许多问题未解——例如在真实饮食条件下效果有多强、对其他类型塑料是否同样有效——这项研究指出了一个出人意料的简单盟友:一勺酸奶中的微生物。
引用: Kobayashi, K., Ogawa, M., Mochizuki, J. et al. Lactobacillus delbrueckii subsp. bulgaricus 2038 and Streptococcus thermophilus 1131 suppress polystyrene nanoplastic transcellular permeability and internalization by intestinal epithelial cells. Sci Rep 16, 9109 (2026). https://doi.org/10.1038/s41598-026-39631-z
关键词: 纳米塑料, 酸奶细菌, 肠屏障, 益生菌, 塑料污染