Clear Sky Science · zh
解决在质子治疗中使用金纳米颗粒时模拟与实验结果矛盾的问题
为什么微小的金颗粒对癌症治疗重要
质子治疗是一种前沿的放射治疗方式,能够精确瞄准肿瘤,同时尽量保护周围健康组织。近年来,科学家尝试将质子治疗与微小的金颗粒(称为金纳米颗粒)结合,以期使治疗对癌细胞更具致命性。实验证明,这种组合通常比单独使用质子能杀死更多肿瘤细胞——但计算机模拟一直难以解释其原因。本文着手解决这一长期未解之谜,并指出了一个与许多研究者预期不同的主要作用机制。
旧说法:归咎于快速电子
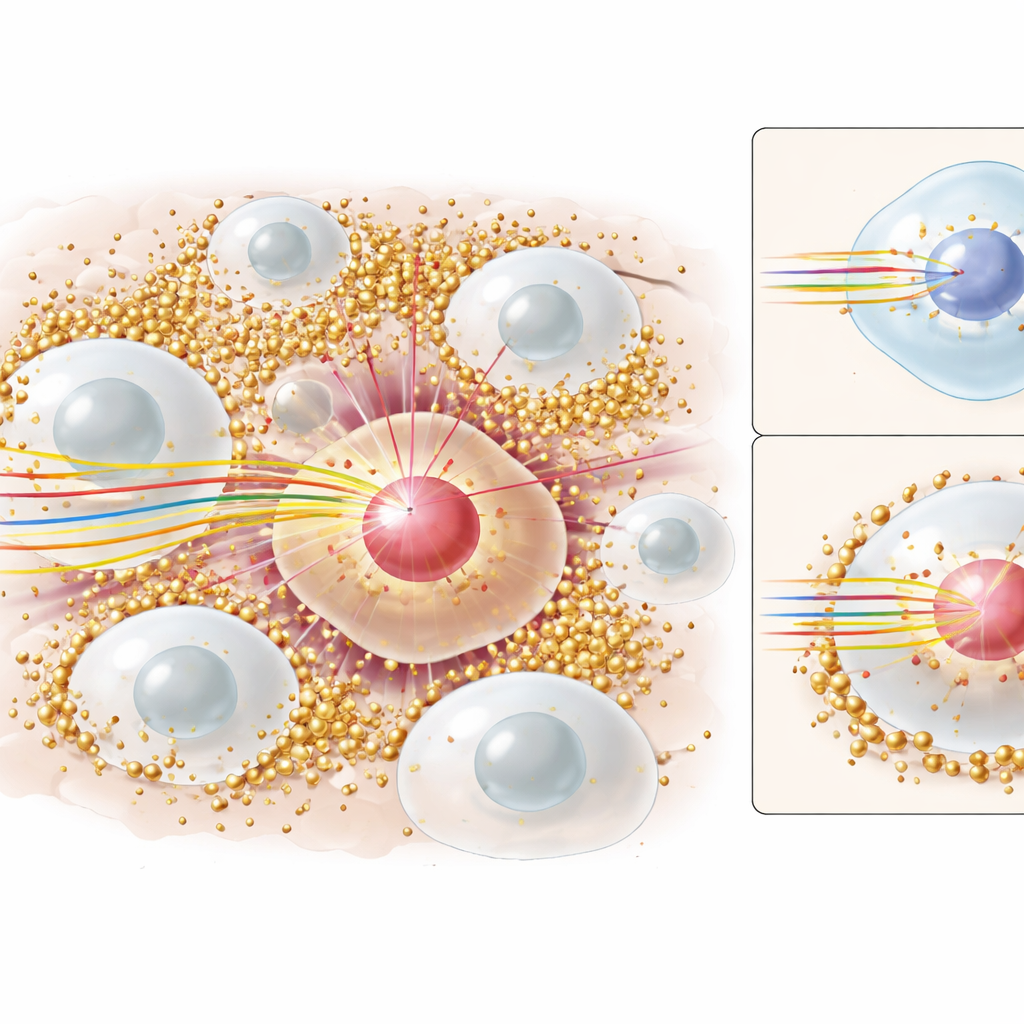
金纳米颗粒在X射线和γ射线治疗中已经广为人知,它们主要通过释放大量能量较高的电子来增强损伤。这些电子传播距离短,会破坏邻近细胞的DNA。多年来,许多人假定质子治疗中也适用同样的基本机制:质子撞击金属,额外的电子飞出,癌细胞因此受损。但问题在于,精细的计算模型(即本研究中使用的那类逐粒子能量跟踪模型)连续预测出细胞核中这些电子带来的额外剂量极少,特别是因为大多数纳米颗粒位于细胞的外部区域,而非DNA所在的细胞核。同时,体外细胞实验却清楚地显示在存在金属时细胞死亡率和治疗效果增加。两者的数值根本对不上。
新图景:质子本身被减速
本研究提出并检验了另一种主要机制:金纳米颗粒不是主要作为电子发射源,而更像质子的微小减速带。当质子穿过分布着高密度、高原子序数金属(如金或铁)的区域时,会与这些重原子发生许多小碰撞。每次碰撞比在普通组织中损失更多能量,因此质子减速更快,其单位路径能量损失——物理学中称为线性能量转移(LET)——增加。高LET通路对DNA的破坏尤为严重,因为它们产生密集的断裂簇,细胞难以修复。通过使用Geant4工具包进行详尽的蒙特卡洛模拟,作者表明金及其他重金属纳米颗粒显著增加了到达细胞核的慢速、高LET质子的数量,尽管总体路径长度在微米尺度,远超传统上被归咎的低能电子的作用范围。
将模拟与真实细胞实验对齐
为了检验这一新图景是否成立,研究重现了若干已发表的细胞实验,这些实验使用质子束并加入了不同大小和浓度的各种纳米颗粒(金、铁和铂)。在每种情况下,模拟计算细胞核所受的额外剂量——以剂量增强比表示——然后代入标准放射生物学公式,该公式将所给剂量与细胞存活率联系起来。这种方法修改了通常描述给定辐射剂量后细胞存活或死亡的曲线。对于所检视的大多数实验,预测的带有纳米颗粒的存活曲线与测量数据紧密吻合,误差通常约为百分之一左右。与此同时,模拟显示当加入纳米颗粒时,细胞核内的电子剂量几乎没有变化,而慢速且更具破坏性的质子的通量明显上升。仍有少数不匹配现象,作者将其归因于某些实验设置或报告的不确定性,但整体趋势强烈支持质子减速的解释。
限制、例外与金最有用的情况
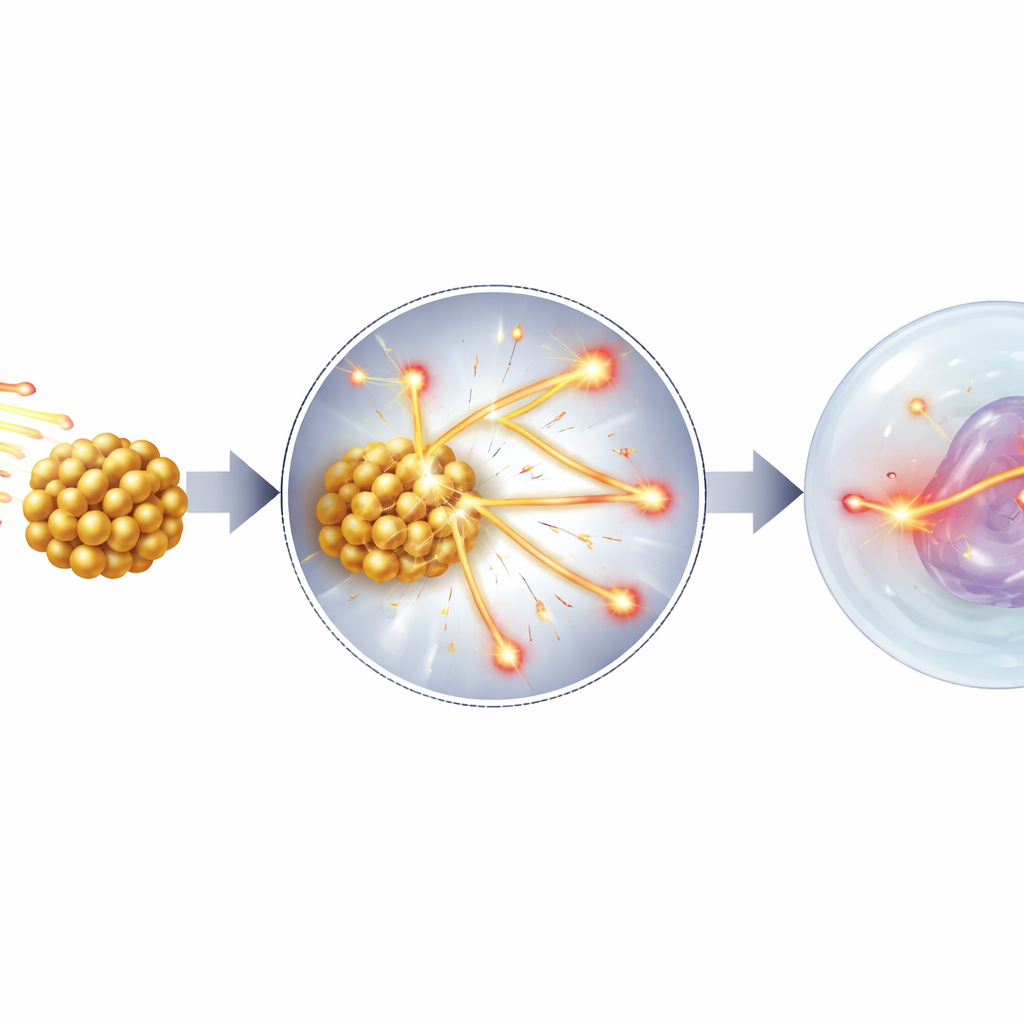
论文还探讨了纳米颗粒似乎不起明显作用的情形。对于在仅几层细胞内就停下的极低能质子束,质子没有足够的距离遇到大量纳米颗粒并发生显著减速,因此看不到明显的效能提升。同样,一些复杂的纳米颗粒形状或实验几何结构描述不充分,难以在模拟中重现,这可能解释了少数模型与测量不一致的离群点。作者指出,如果极小的颗粒实际进入细胞核,则电子发射和与细胞分子的化学反应可能会增加效应。尽管如此,在许多现实的治疗条件下,主导模式是一致的:在富含金属的区域对质子的更多减速会导致细胞核内更集中的损伤。
这对未来癌症治疗意味着什么
对非专业读者来说,核心结论是:质子治疗中的金纳米颗粒更像是看不见的刹车,而不是微小的电子枪——它们把快速、相对温和的质子变成在关键部位(即肿瘤细胞DNA处)更慢、更具杀伤力的“重击手”。通过澄清这一机制并证明它能准确再现真实的细胞存活数据,这项研究有助于解决理论与实验之间长期存在的冲突。这一见解可以指导更聪明的纳米颗粒治疗设计,例如选择材料、尺寸和浓度,以最大化在肿瘤细胞核附近对质子的减速同时最小化副作用。从长远看,这可能使质子治疗更精确、更强效,为难治性癌症患者带来更好的疗效。
引用: Tabbakh, F. Resolving the contradiction between simulation and experimental results of using gold nanoparticles in proton therapy. Sci Rep 16, 8012 (2026). https://doi.org/10.1038/s41598-026-39621-1
关键词: 质子治疗, 金纳米颗粒, 放射增敏, 癌症放疗, 纳米医学