Clear Sky Science · zh
人类节段性内毒素挑战后支气管肺泡灌洗液的蛋白组学描绘——一种潜在的加重模型
为何短暂的肺部炎症很重要
像慢性阻塞性肺疾病(COPD)这样的慢性肺病常在气道发生急性炎症时突然加重,通常由感染引发。这类被称为加重的事件会导致大量患者入院,并可能永久恶化呼吸功能。在患者身上直接研究这些事件既困难又存在风险。本研究在健康志愿者中采用可控的、短暂的肺部刺激来模拟这些加重的一些特征,随后在肺液中测量数百种蛋白,观察哪些信号被激活。研究结果有助于科研人员理解肺部炎症的化学过程,并可加速新疗法的开发。
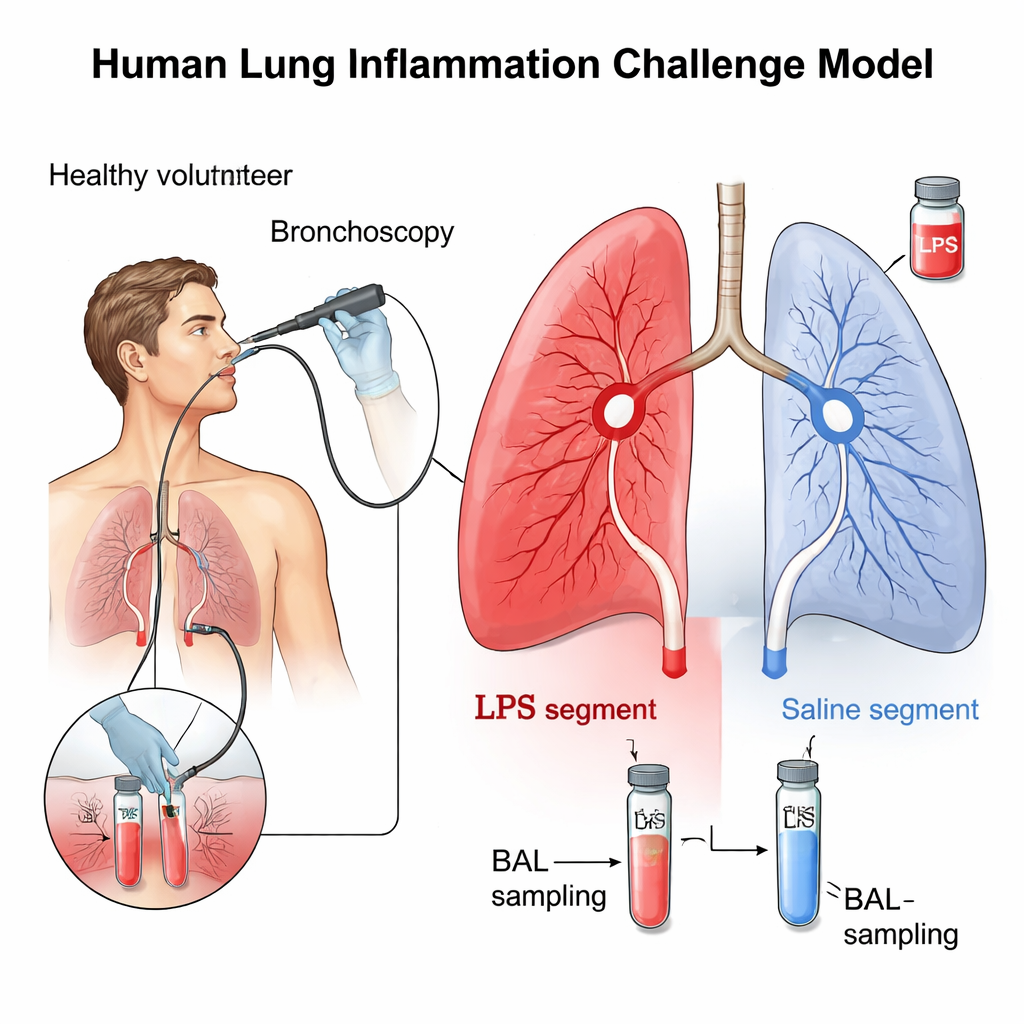
构建一个安全的“微型肺部加重”
研究者使用了一种成熟技术,短暂且局部地刺激肺部的小区域。十名健康、不吸烟的成人接受了支气管镜检查,一根细长柔性管被引导进入气道。通过该管,研究团队在一侧肺节段内注入微量细菌内毒素(即脂多糖,LPS),而在对侧相应节段注入生理盐水作为对照。LPS 是某些细菌的天然成分,可强烈激活机体防御反应。24小时后,对相同区域进行盐水冲洗——即支气管肺泡灌洗(BAL)——以采集来自肺深处的液体和细胞进行细致分析。
在肺液中进行蛋白普查
研究团队没有只看少数熟悉的标志物,而是使用高通量技术(SomaScan 平台)在 BAL 液中同时测量约1500种不同蛋白。他们比较了挑战前、仅盐水处理后和 LPS 处理后的样本。如预期,挑战前与盐水样本非常相似,证实程序本身并未引发炎症。相反,LPS 处理的节段发生了显著变化:599种蛋白显著上调,仅有4种下调。许多上升的蛋白是已知的炎症介质,包括 IL‑6 和 IL‑8、诸如髓过氧化物酶(MPO)和基质金属蛋白酶9(MMP9)等酶类,以及急性期蛋白如C反应蛋白(CRP)和凝血因子 von Willebrand 因子(VWF)。主成分和聚类分析显示 LPS 样本形成了明显独立的一组,强调了这种局部挑战对肺环境的强烈改变。
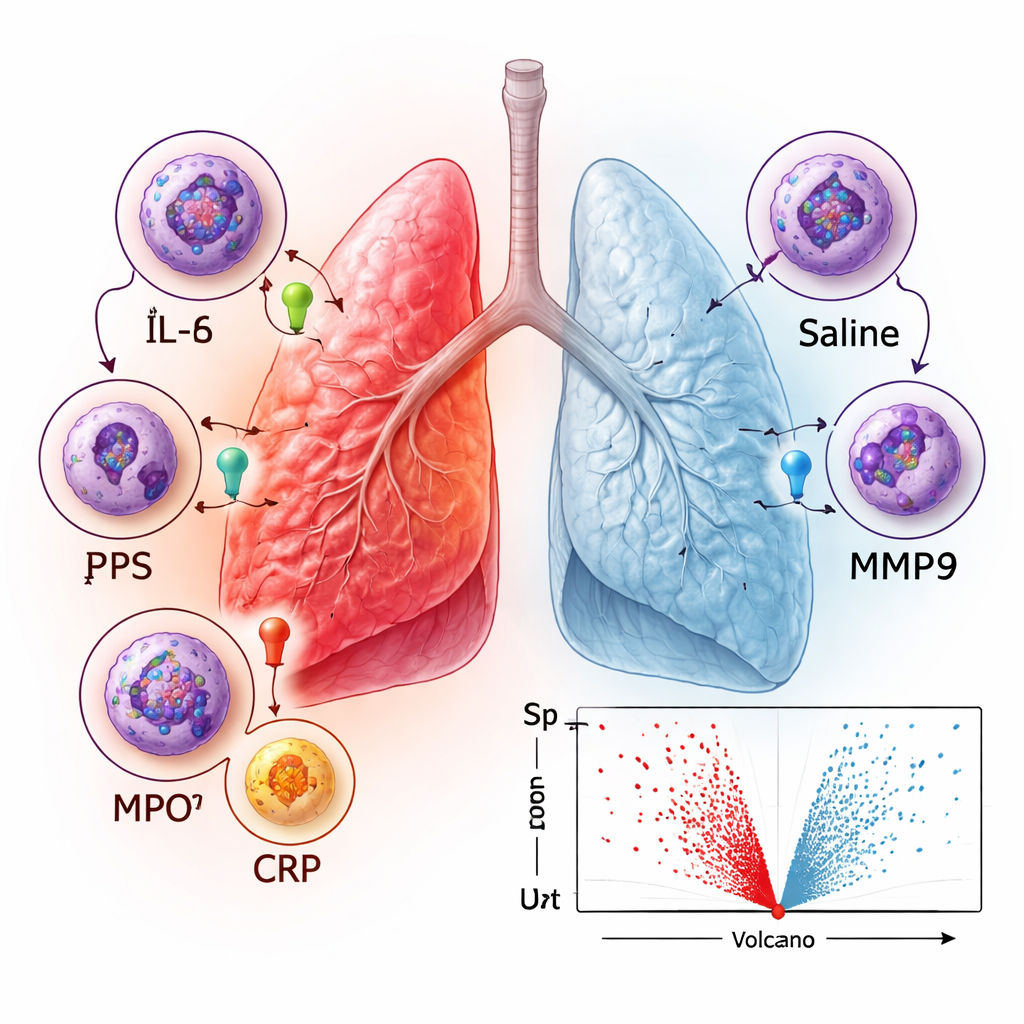
蛋白模式揭示的肺部防御机制
为超越单一标志物分析,研究团队考察了哪些生物学过程在 LPS 后上调的蛋白中最为富集。最强的信号涉及普遍的免疫活性和对外界或化学刺激的反应,以及与细胞迁移和程序性细胞死亡相关的过程。蛋白互作的网络分析突出了趋化因子(吸引免疫细胞的分子)、称为基质金属蛋白酶的组织改建酶、以及免疫蛋白体成分的簇状分布——免疫蛋白体是帮助处理外源蛋白以供免疫识别的细胞机器。这些模式与肺部应对感染的已知机制一致:嗜中性粒细胞等免疫细胞被吸引到气道,致病微生物遭到攻击,周围组织被重塑并在必要时修复。
将该模型与真实的 COPD 加重联系起来
作者接着探讨这一短期 LPS 模型与现实世界中 COPD 加重的相似性。他们将肺液数据与已发表的、在 COPD 加重时升高的血液生物标志物清单进行比较。在可评估的17种标志物中,有16种——包括 IL‑6、IL‑8、CRP、纤维蛋白原及若干趋化因子——在 LPS 后的 BAL 中也呈升高。仅有一种(sTREM‑1)未发生变化,这与此前关于其有效性的混合结果一致。这一高度重合表明,当健康肺短暂受到 LPS 挑战与易感的 COPD 肺经历严重加重时,许多相同的炎症通路被激活。与此同时,作者也指出 LPS 反应是短暂的,不能完全复制长期疾病中出现的慢性结构性损伤。
这对未来治疗意味着什么
简而言之,本研究表明,在健康志愿者局部可控且短暂地刺激肺部某一部分,能够诱发一种化学风暴,其特征与 COPD 加重期间发生的变化高度相似。通过绘制在该反应中上调或下调的数百种蛋白,研究人员获得了关于哪些信号和通路可能是重要靶点的详细图谱。由于该模型安全、可重复且已在早期药物试验中使用,它为新型抗炎药物的测试以及更精确生物标志物的识别提供了强有力的试验场,这些标志物未来可能帮助医生预测、发现并更好地治疗慢性肺病的急性加重。
引用: Gress, C., Müller, M. & Hohlfeld, J.M. Proteomic profiling of bronchoalveolar lavage following human segmental endotoxin challenge—a potential exacerbation model. Sci Rep 16, 6145 (2026). https://doi.org/10.1038/s41598-026-39528-x
关键词: 肺部炎症, COPD 急性加重, 支气管肺泡灌洗, 内毒素挑战, 蛋白质组学