Clear Sky Science · zh
将深度学习与基于物理的建模结合实现高精度抗体-抗原界面预测
这对未来药物意味着什么
抗体是我们免疫系统以及许多现代药物的制导导弹。要设计更好的抗体,科学家需要精确知道抗体如何抓住其目标分子(即抗原)。用实验手段测定这些结构既缓慢又昂贵。这项研究表明,将深度学习与传统的物理风格建模相结合,可以显著提升计算预测抗体与抗原接触位置的精度,从而有望加速抗体设计与筛选。
找到握手区域
抗体通过其末端的小而灵活的环状结构识别目标,这些环被称为结合区,它们共同形成一个接触斑块。这些环可以弯曲和扭转,而抗原上的匹配区域往往分散且浅平,而不是形成深腔。正是这种柔性和微妙性使得对接问题——确定两者如何契合——对计算机来说极其困难。传统的对接程序通过尝试两种蛋白质的多种相对位置并用诸如静电吸引和水分位移等物理规则对其评分,但在缺乏生物学线索时,它们常常停留在错误的配对上。
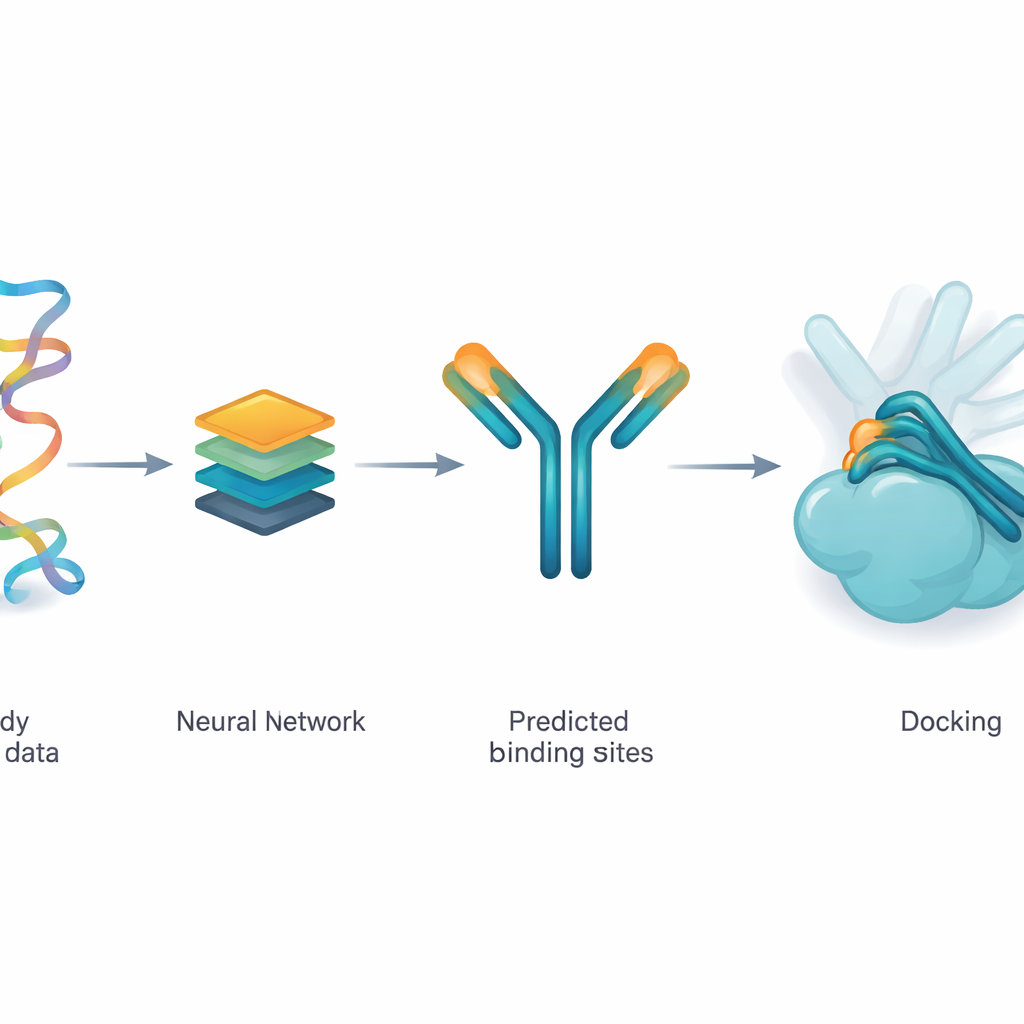
教网络提出可能的接触点
作者使用一种名为 ParaDeep 的深度学习模型来猜测抗体上哪些氨基酸最有可能接触抗原。ParaDeep 仅基于抗体的序列——即其构件的排列顺序——而不需要完整的三维结构。它将重链和轻链序列一起读取,编码它们的化学与位置特征,并使用注意力机制突出看起来像是结合候选的残基。每个位置都会得到一个概率评分;高于阈值的残基被视为预测的接触区,并可以映射回抗体结构上。
引导物理引擎而非替代它
研究团队并未用深度学习直接从零生成完整的抗体–抗原复合体,而是将 ParaDeep 预测的接触残基作为输入馈入现有的基于物理的对接引擎 PyDockWEB。该对接程序会采样成千上万种抗体与抗原可能的相遇方式,并用能量函数对其评分。在新的框架中,预测的接触残基充当软约束:它们偏置搜索,使许多采样的构象将这些残基带到靠近抗原表面的位置。重要的是,底层的物理评分和刚体处理保持不变,使过程透明且运行相对轻量。
预测到底提升了多少?
研究人员在来自经整理数据库的 50 个已知抗体–抗原复合体上测试了他们的混合方法。对每个案例,他们比较了标准的“盲”对接与由 ParaDeep 约束引导的对接。他们测量了局部界面精度(预测接触区与真实情况的接近程度)、整体形状相似性以及一种广泛用于评价对接模型的综合质量得分。在这一数据集上,受引导的方法大幅降低了结合位点的错误,将整体结构推向更接近真实复合体的方向,并使许多预测从明显错误转为中等或高质量类别。受引导模型中几乎一半落入高质量范围,而盲对接约为四分之一。
为何有些匹配更容易
团队还研究了为何有些复合体受益更多。他们发现仅仅预测更多接触残基并不能保证成功;关键在于将约束放在正确的区域,而不是数量。更亲水并且含有更多柔性无规则卷曲段的界面往往对接效果更好,这很可能是因为这些界面与 PyDockWEB 强调静电相互作用的评分策略相吻合,而且在不需大幅形变的情况下更容易对齐。当研究者用直接从实验结构提取的“理想”接触信息重复一些失败案例时,大多数情况都有改善,这证实了准确定位接触斑块是关键因素——但在需要大幅形状调整的情况下,刚体对接仍存在局限。
对未来的意义
通俗地说,这项工作表明,给基于物理的对接程序一个关于抗体可能抓住目标位置的聪明提示,可以在很大程度上提升其命中率,同时不将过程变成一个不透明的黑箱。ParaDeep–PyDockWEB 的组合流程并不取代更高级的柔性或生成方法,但提供了一种实用手段:利用序列层面的深度学习信号来引导熟悉且可解释的对接工具。随着抗体发现与工程产生越来越大的序列库,这类混合方法可帮助研究者快速筛选出在结构上与目标一致的候选者,从而使从序列到可用抗体的路径更快且信息更充分。
引用: Kodchakorn, K., Udomwong, P., Pamonsupornwichit, T. et al. Integrating deep learning with physics based modeling enables high precision antibody antigen interface prediction. Sci Rep 16, 8134 (2026). https://doi.org/10.1038/s41598-026-39466-8
关键词: 抗体对接, 深度学习, 结合位点预测, 蛋白质–蛋白质相互作用, 抗体设计