Clear Sky Science · zh
新辅助化疗对脂肪来源间充质基质细胞功能及其对肿瘤患者成纤维细胞调节作用的影响
这对癌症幸存者为何重要
许多接受过癌症治疗的人随后会面临愈合缓慢的伤口和术后并发症。与此同时,医生们越来越多地探索利用患者自身脂肪中来源的修复细胞来促进组织恢复的方法。本研究提出了一个实际且迫切的问题:在化疗之后,这些修复细胞仍然可用吗?如果不可用,哪些细胞受影响最严重?
体内隐秘的修复助力
我们的脂肪组织不仅仅是能量储存。它包含一类多功能的修复细胞,称为脂肪来源的间充质基质细胞(AD‑MSCs)。这些细胞并非静止存在;它们分泌一系列信号分子,能够抑制炎症、刺激新血管形成,并促使邻近细胞生长与重建受损组织。在脂肪之上的皮肤中生活着成纤维细胞——这些“工蜂”细胞会迁移到伤口处并沉积胶原蛋白,胶原是为新组织提供强度的蛋白质支架。AD‑MSCs 与成纤维细胞共同决定皮肤在受伤或手术后恢复的质量。
在治疗前后检测脂肪修复细胞
研究者从66例接受手术的患者中采集了小块皮肤和脂肪样本,其中部分患者在手术前接受过化疗,部分则没有。从脂肪中分离出AD‑MSCs,并确认这些细胞在形态和功能上仍具有典型修复细胞特征:它们呈现预期的表面标志,并能在体外分化为类骨、类软骨和类脂肪细胞。从皮肤中分离得到成纤维细胞。随后研究团队比较了接受与未接受化疗患者的AD‑MSCs和成纤维细胞在生长、细胞周期、分泌信号分子以及与伤口愈合和再生相关基因表达方面的差异。
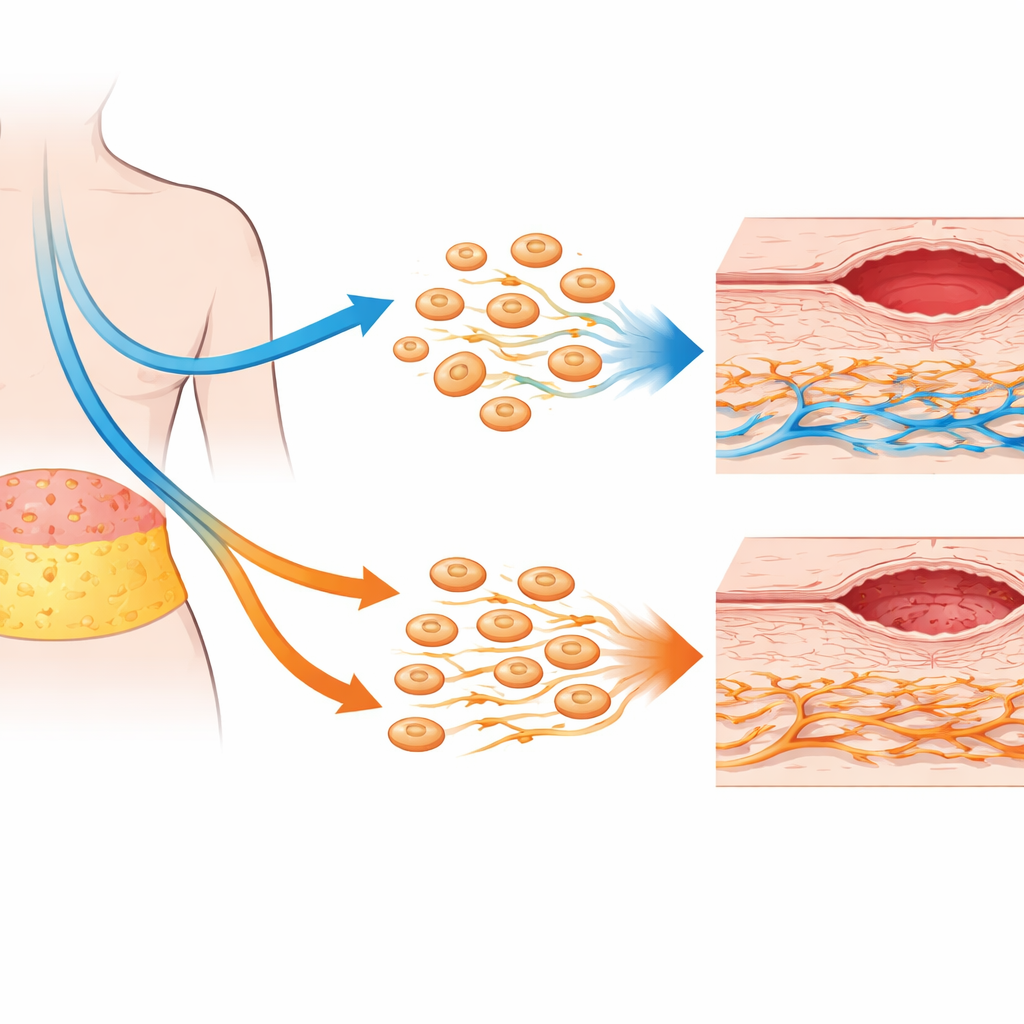
脂肪修复细胞出人意料地坚韧
与担心化疗可能削弱AD‑MSCs功能的预期相反,研究发现这些脂肪来源的修复细胞表现出明显的韧性。它们的基本身份标志、生长模式和分泌的信号蛋白谱在很大程度上未被既往化疗改变。与生长、自我更新和伤口修复相关的基因活性只有微小、无临床意义的波动。实际上,来自化疗患者的AD‑MSCs显示出略高的线粒体活性,提示代谢更为活跃而非受损。在共培养实验中(AD‑MSCs 与成纤维细胞共享培养基但不直接接触),AD‑MSCs 仍能增强某些成纤维细胞行为,例如朝向修复信号的定向迁移,尤其在来自未接受化疗患者的样本中更为明显。
皮肤“建筑者”承受化疗冲击
成纤维细胞的情况则截然不同。取自化疗患者皮肤的细胞表现出明显的生物活力下降:它们在培养皿上迁移填充类“划痕”伤口的能力显著受损,胶原蛋白的产生倾向于降低。它们分泌的信号分子谱向更具炎症性、再生性较差的方向转变,许多与生长信号、受体及再生潜能相关的基因表达被下调。即便在与同源AD‑MSCs 共培养时,这些成纤维细胞的大多数功能——迁移、胶原产生以及有利的基因活性——相比未接受化疗的成纤维细胞仍然受抑。
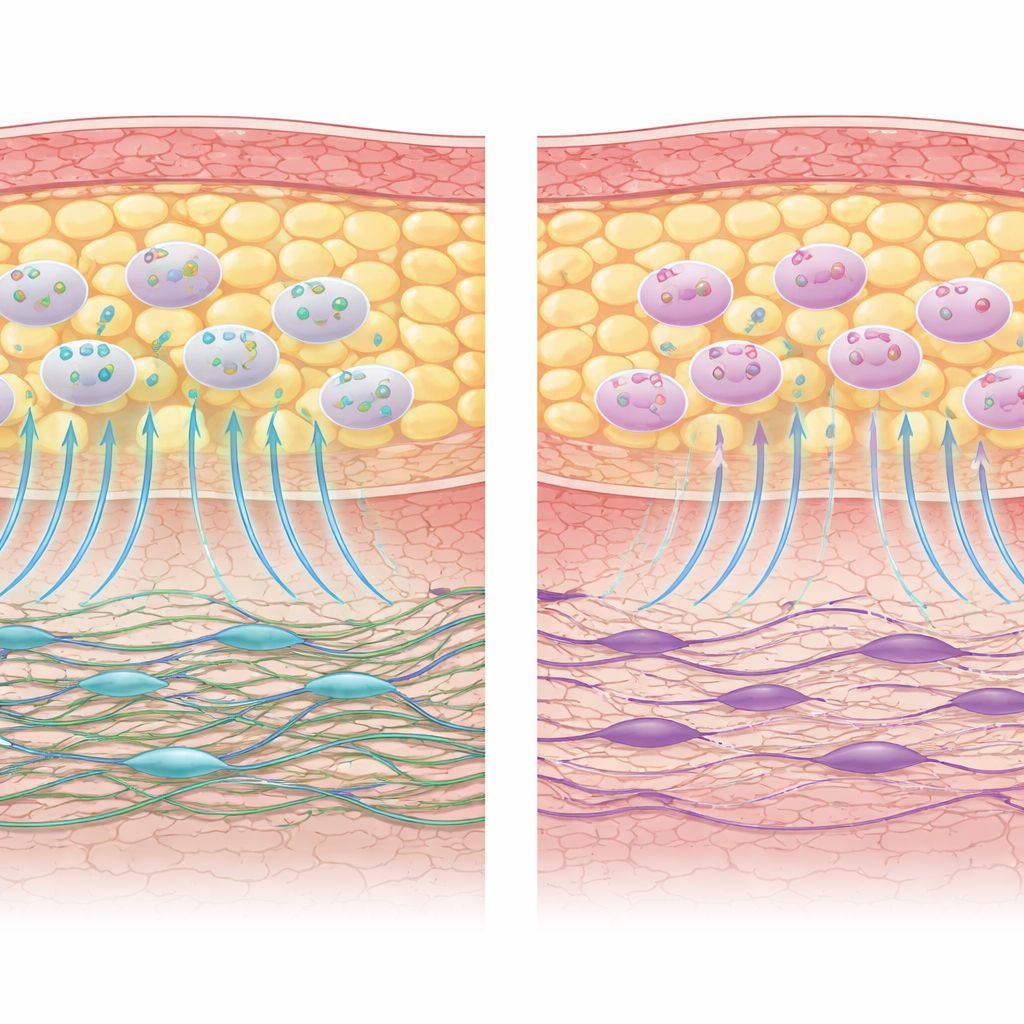
对未来修复疗法的意义
对普通读者而言,该研究传递的信息是:化疗似乎并未摧毁体内基于脂肪的修复细胞库,但确实使皮肤的一线“建筑者”——成纤维细胞——在快速进入伤口并重建坚固组织方面能力下降。由于AD‑MSCs 在功能上仍相对完整,它们仍是用于重建手术、伤口护理和术后脂肪移植等的有前景候选者。然而,成纤维细胞受损的状态可能限制这些类干细胞单独所能带来的益处。作者建议,未来的疗法可能需要同时支持修复伙伴的双方:在利用稳健的AD‑MSCs 的同时,保护或恢复成纤维细胞的健康,最好在更复杂、更接近体内的模型中评估,以更真实地反映癌症幸存者的愈合环境。
引用: Skoniecka, A., Słonimska, P., Tymińska, A. et al. Impact of neoadjuvant chemotherapy on the functionality of adipose-derived mesenchymal stromal cells and their modulatory effects on fibroblasts in oncology patients. Sci Rep 16, 8614 (2026). https://doi.org/10.1038/s41598-026-39457-9
关键词: 化疗, 伤口愈合, 脂肪来源干细胞, 成纤维细胞, 再生医学