Clear Sky Science · zh
白色念珠菌感染抑制脂多糖或铜绿假单胞菌刺激的小鼠骨髓来源巨噬细胞(BMDM)反应
当“友好”真菌变得复杂
大多数情况下,酵母白色念珠菌悄然栖息在我们的皮肤和黏膜表面。但在合适(或更确切地说,不利)的条件下,它会引发严重乃至致命的感染,尤其是在免疫功能受损的人群中。本研究探讨了一个不太明显的风险:当白色念珠菌与细菌同时出现时,它如何悄然干扰我们的免疫防御,从而可能以常规实验和治疗易被忽视的方式改变混合感染的进展。
为何这种常见酵母很重要
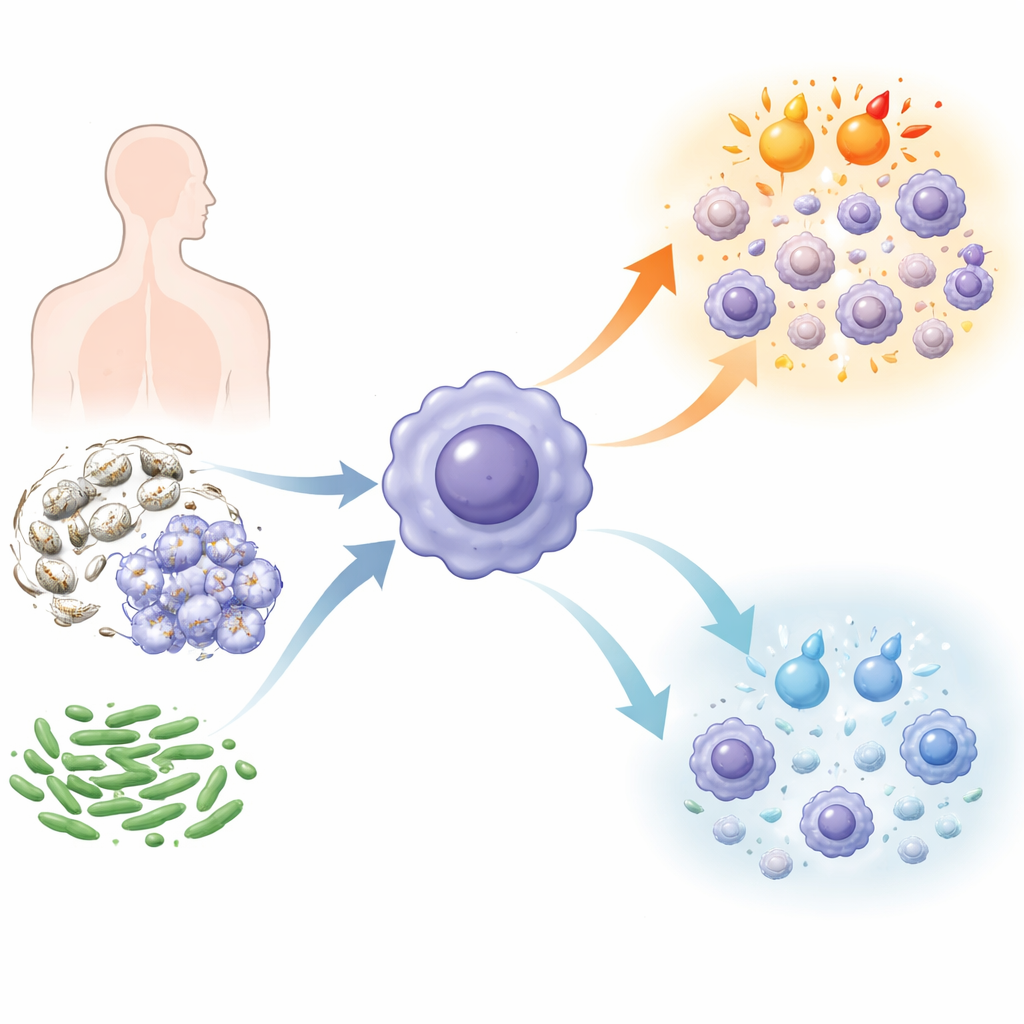
白色念珠菌最为人所知的是引起如鹅口疮等局部感染,但它也能进入血流并播散全身,此时治疗非常困难且常致命。同时,针对有限几类抗真菌药物的耐药性正在上升。我们的身体在识别并吞噬白色念珠菌以及通过释放称为细胞因子的信号蛋白招募增援方面,很大程度上依赖于称为巨噬细胞的免疫细胞。然而在现实中,白色念珠菌很少单独出现:它常与细菌共存,例如囊性纤维化患者肺部的病原体铜绿假单胞菌。此类混合感染常与更差的临床结局相关,但我们对单个免疫细胞在同时面对真菌和细菌时的行为知之甚少。
在免疫细胞内进行全蛋白组水平的观察
研究者以小鼠骨髓来源巨噬细胞为模型,用活的白色念珠菌、细菌分子如脂多糖(LPS),或直接用铜绿假单胞菌感染这些细胞。随后他们应用一种称为数据独立采集(data‑independent acquisition)的高分辨率蛋白质组学方法,对每个细胞内的数千种蛋白进行清点。通过比较受感染和未感染细胞,研究者得以观察巨噬细胞在不同条件下如何重塑其内部机制及哪些免疫通路被激活或抑制。
对白色念珠菌单独暴露时的出乎意料的低调反应
当巨噬细胞仅遇到活的白色念珠菌时,确实发生了反应,但远不及对LPS或铜绿假单胞菌的反应强烈。白色念珠菌触发了一些经典的警报通路并引起了诸如肿瘤坏死因子(TNF)等炎性蛋白的适度产生,但细胞蛋白组整体的重塑相对较温和。数据表明,白色念珠菌可能隐藏了许多免疫受体用于识别的表面特征,从而削弱了巨噬细胞的警报反应。尽管如此,一小组但一致的免疫相关蛋白和调控因子发生了变化,暗示白色念珠菌在更微妙的层面上悄然使细胞处于某种预备状态。
白色念珠菌如何削弱对细菌的警报
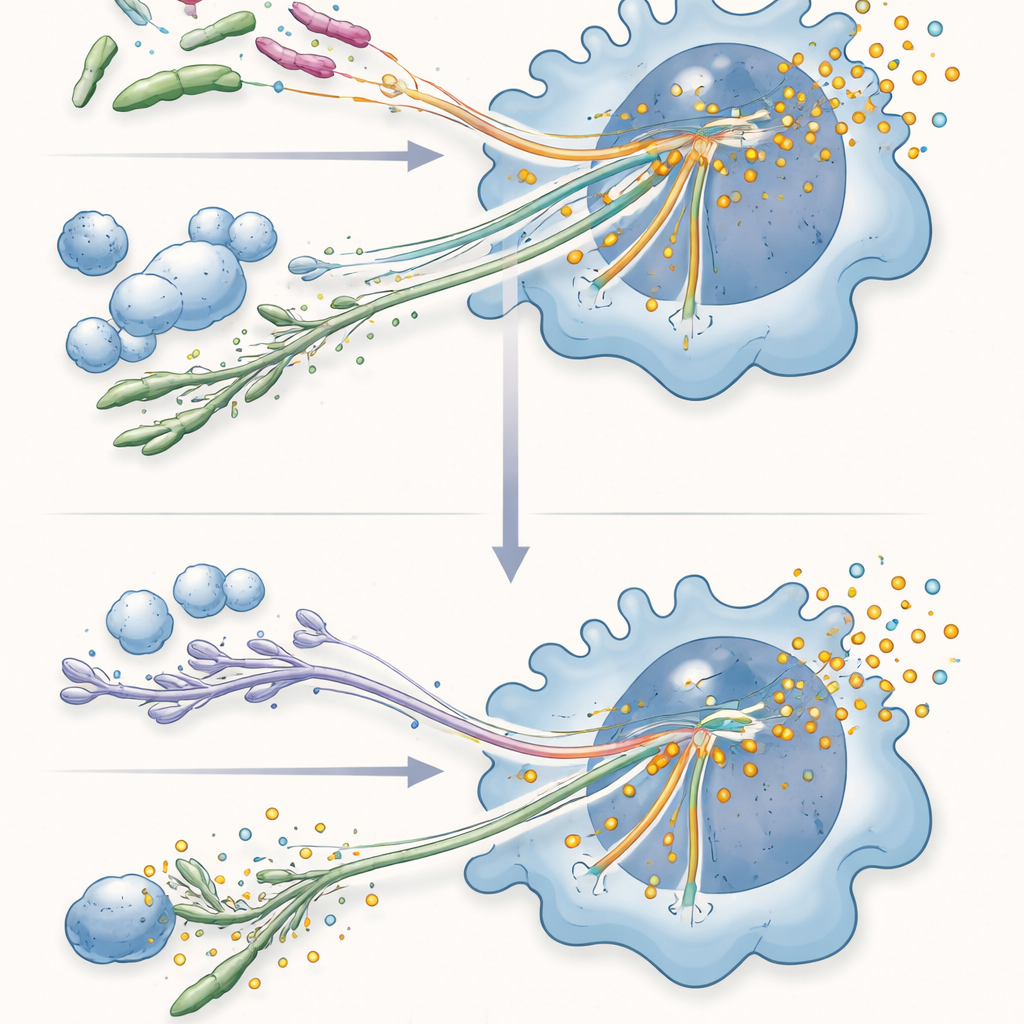
最显著的发现出现在白色念珠菌与细菌刺激共同存在时。在混合暴露条件下,白色念珠菌持续削弱巨噬细胞对LPS和活铜绿假单胞菌的反应,显著减少某些关键细胞因子的产生,尤其是IL‑6和IL‑12p40,而像TNF和IL‑10等其它因子则大多保持不变或甚至增加。蛋白质组分析显示,白色念珠菌广泛抑制了LPS或铜绿假单胞菌通常上调的一大类蛋白,但对白这些刺激下被下调的蛋白影响甚微。这种抑制效应需要活的白色念珠菌与巨噬细胞直接接触,且能够转变为长丝状菌丝体的菌株比被锁定在圆形酵母形态的突变株更能抑制反应,提示真菌形态驱动的细胞内应激可能发挥作用。
这对现实世界中的感染意味着什么
对非专业读者来说,关键结论是:白色念珠菌不仅仅引起本身的感染;它还可能作为免疫系统对细菌反应的隐性破坏者。在混合感染期间通过选择性地降低巨噬细胞内某些炎性信号,白色念珠菌可能改变机体同时控制真菌和细菌的能力。这项工作表明,医生和研究人员在考虑严重感染与潜在治疗时,应当把微生物的联合行为纳入考量,而不仅仅关注单一病原体。弄清白色念珠菌如何在分子水平上对免疫细胞施加这种“刹车”,最终或可为恢复平衡反应而不会加剧炎症的策略提供新的思路。
引用: Baker, C.P., Laba, S., Warner, J. et al. Candida albicans infection suppresses lipopolysaccharide or Pseudomonas aeruginosa stimulated murine bone marrow derived macrophage (BMDM) responses. Sci Rep 16, 8751 (2026). https://doi.org/10.1038/s41598-026-39429-z
关键词: 白色念珠菌, 巨噬细胞, 共感染, 先天免疫, 铜绿假单胞菌