Clear Sky Science · zh
机械应力丧失通过不同的滑膜细胞亚群诱发滑膜炎、纤维化与关节软骨退变
为何休息关节也有风险
我们许多人都听说过过度使用关节会导致损耗,但这项研究显示使用过少同样会对关节造成伤害。研究人员用小鼠模型探讨在数周内显著减少运动和承重(类似长期打石膏、瘫痪或长期卧床)时膝关节内发生的变化。通过逐细胞追踪显微组织变化与基因活性,他们揭示了机械应力丧失如何在关节滑膜中引发连锁反应,最终损害维持无痛运动所需的光滑软骨。
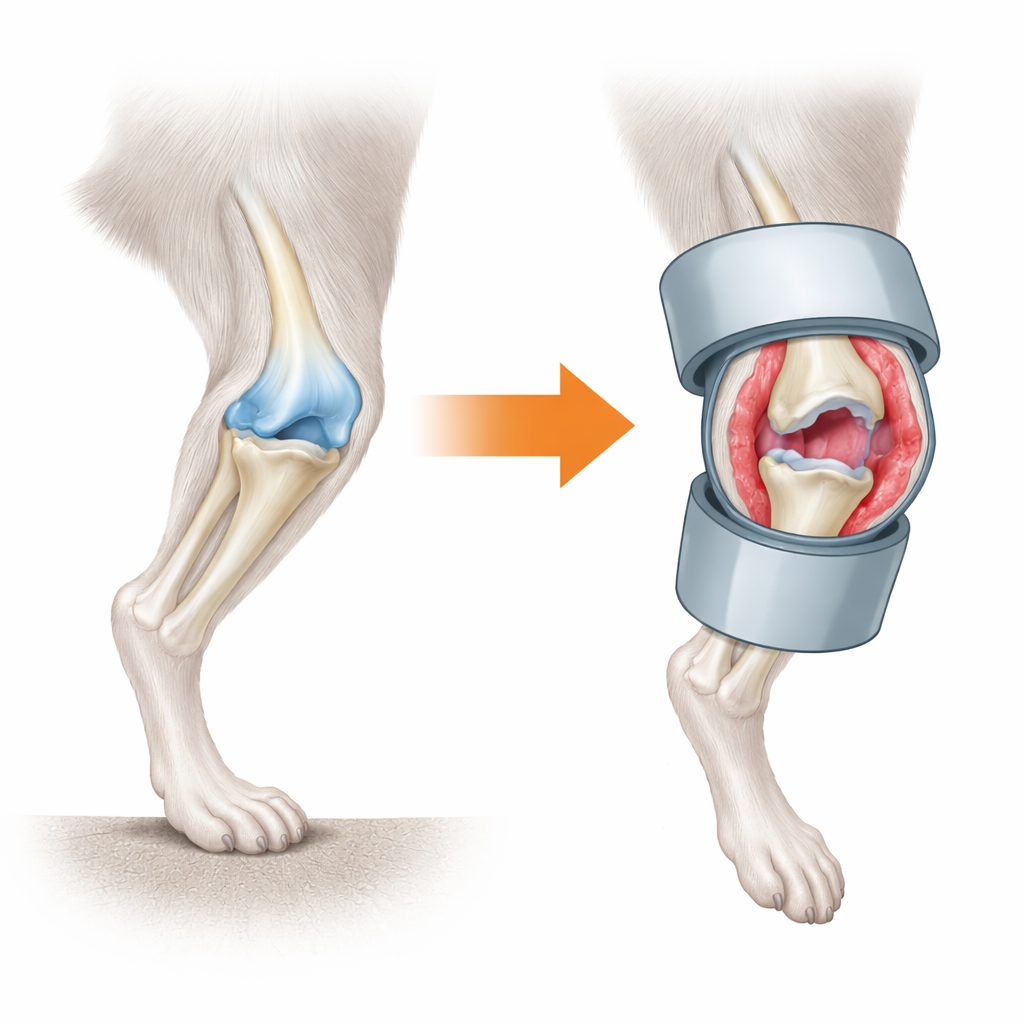
膝关节停止活动时发生了什么
研究团队建立了“最小化机械应力”模型:用小型塑料筒固定小鼠膝关节,同时抬高尾部使后肢不承重。仅仅三天内,称为滑膜的关节内膜就出现了炎症:细胞层增厚,新血管出现,免疫细胞聚集。接下来的两周内,该内膜发展出纤维化的瘢痕样组织,关节变得僵硬。覆盖骨端的滑润软骨并没有立即崩解;相反,只有在滑膜改变明显进行时,软骨才开始出现粗糙与表面物质的丧失,这种损伤在六周内持续加重。
运动与压力作为关节良方
研究者接着问这些变化是否可逆。在两周的固定与卸载后,一些小鼠恢复了关节活动但仍不承重,另一些则同时恢复了活动与负重。两组的滑膜炎症都减轻,内膜回薄趋于正常,表明单纯运动对滑膜健康有强烈影响。然而,软骨在既恢复活动又恢复负重时恢复最好。在分子层面,参与健康软骨构建的基因在不活动期间明显下调,但在关节重新允许运动与承重后大多回升。这提示软骨维持结构依赖于滑动运动与适度压力的组合。
滑膜细胞如何驱动软骨损伤
深入研究时,科学家检测到随着损伤进展滑膜中哪些基因被激活。他们发现与纤维化、组织重塑以及可分解软骨的酶相关的基因活性上升。许多信号来自免疫相关的介导分子,如炎性细胞因子与生长因子,它们能影响邻近的软骨细胞。单细胞RNA测序显示,不活动改变了滑膜内的细胞构成。两类异常细胞在固定的关节中扩增:一种类肌成纤维细胞,专门产生纤维基质;另一类为表达高水平炎性分子和软骨降解酶的巨噬细胞亚群。这些细胞共同在关节周围形成了一个独特的促进损伤的微环境。
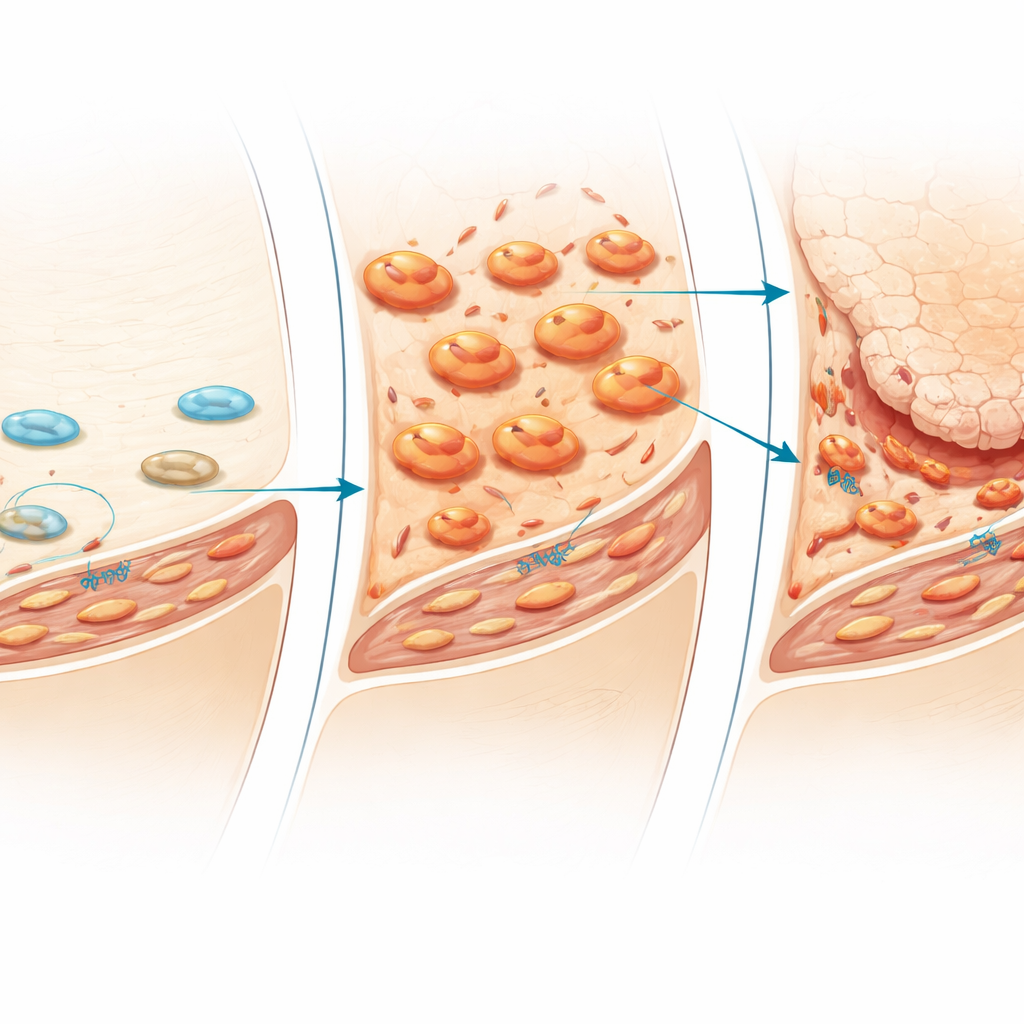
免疫细胞的早期作用
时间顺序证明至关重要。在不同阶段取材的组织切片中,巨噬细胞在移除机械应力后数日内首先在薄滑膜层迅速增多,随后向组织更深处扩散。随后才是成纤维细胞增殖和致密纤维组织的出现。当团队通过注射能消除巨噬细胞的脂质体选择性耗竭滑膜巨噬细胞时,这一级联反应发生了显著改变:关节内膜的炎症与纤维化明显减少,软骨退变显著减轻。类肌成纤维细胞亚群的标志也随之下降。这些发现将巨噬细胞指认为不活动所致有害反应的早期组织者,激活成纤维细胞并为随后软骨崩解奠定基础。
对保护关节的启示
总体而言,该研究表明关节依赖规律的运动和适当的机械负荷来维持滑膜与软骨的平衡。当这种机械输入消失时,滑膜中专门的免疫细胞和成纤维细胞转入炎性、纤维化状态,逐步侵蚀软骨。重要的是,恢复活动与承重可以扭转这一过程,尤其在损伤尚未严重时更有效。对于因打石膏、瘫痪或长期卧床而面临长期不活动的人群,这些结果强调了早期、规范的关节活动和安全负重的重要性,同时也提示未来可能通过针对巨噬细胞—成纤维细胞轴的药物来预防持久性关节损伤的潜力。
引用: Ishikura, H., Okada, H., Kin, Y. et al. Loss of mechanical stress induces synovitis, fibrosis and articular cartilage degeneration via distinct synovial cell subsets. Sci Rep 16, 8007 (2026). https://doi.org/10.1038/s41598-026-39416-4
关键词: 关节不活动, 滑膜炎, 软骨退变, 机械负荷, 巨噬细胞