Clear Sky Science · zh
利用CD32a信号吞噬优化THP-1-CAR单核细胞以实现抗原特异性T细胞激活
教免疫系统学会新把戏
现代细胞疗法已经能重新编程免疫细胞去追踪并清除癌症,但多数依赖T细胞,而T细胞在实体瘤的恶劣微环境中常常力不从心。本研究转而关注另一类强大的防御者——巨噬细胞,人体的“专业吞噬者”,探讨如何重线它们,使其不仅更高效地吞噬有害细胞或病毒,还能招募T细胞,从而实现更持久、靶向的攻击。研究揭示了构建更佳嵌合抗原受体(CAR)巨噬细胞的设计规则,这些规则可应用于如COVID-19等感染以及难治的实体瘤。
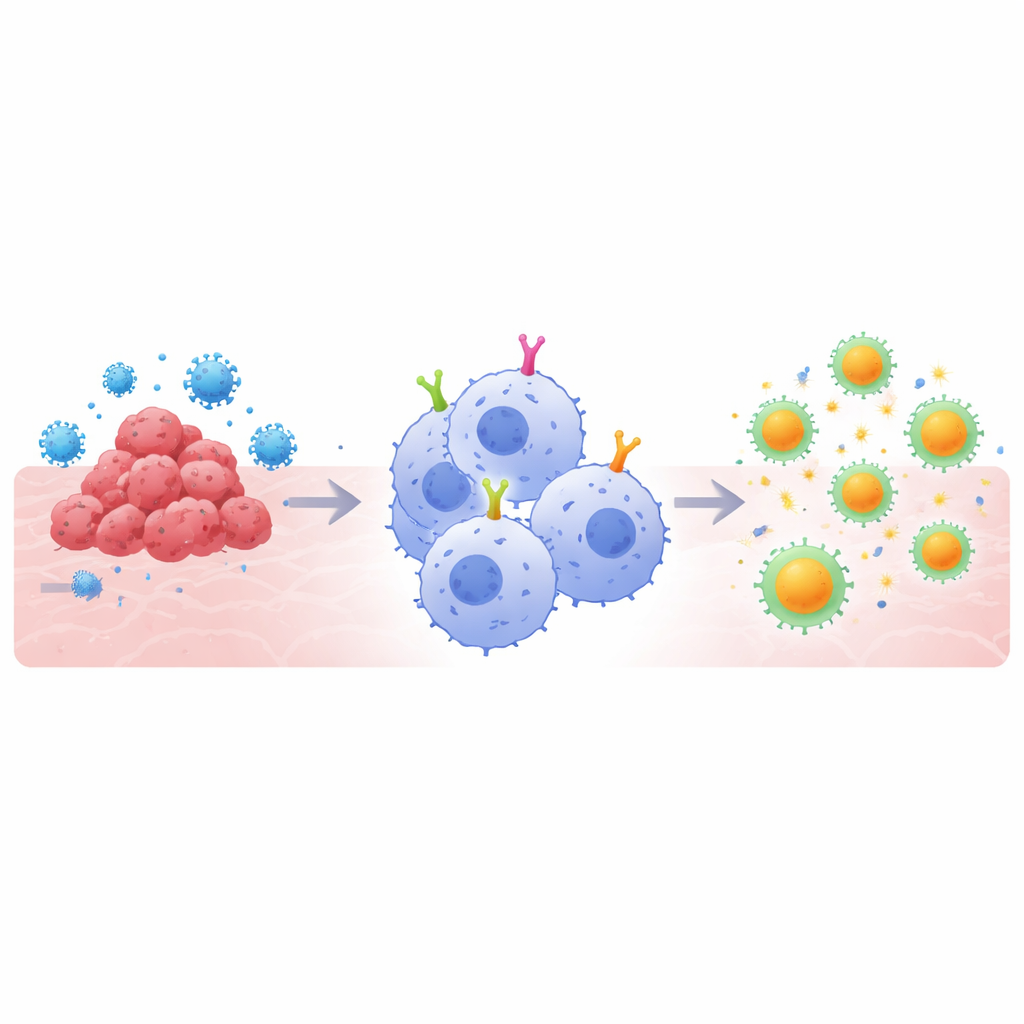
为何“超级吞噬细胞”重要
基于CAR的疗法通过为免疫细胞配备定制的表面受体来识别特定靶点(如肿瘤蛋白或病毒刺突蛋白)。T细胞版本已改变了某些血液癌症的治疗,但在对抗实体瘤和某些感染时面临障碍。巨噬细胞提供了不同的途径:它们天生能吞噬威胁并将其分解成可供T细胞展示的片段,连接了免疫的先天与获得两臂。然而,大多数CAR设计最初是为T细胞构建的,而非巨噬细胞。作者推断,为了充分利用巨噬细胞的优势,CAR的内部信号结构——即在识别靶点后告诉细胞如何响应的那部分——需要针对这些吞噬细胞进行专门调整。
寻找最佳内部线路
研究团队系统比较了几种内置信号域,这些信号域被引入可诱导为巨噬细胞的人类单核细胞系(THP‑1)中。他们关注来源于通常驱动吞噬和炎症的受体的域:CD3ζ(经典的T细胞模块)、CD32a(结合被抗体包裹靶点的受体)、补体受体成分CR3的CD11b和CD18(关键补体受体)以及TLR4(微生物危险感受器)。使用包被SARS‑CoV‑2刺突蛋白的微球和假病毒,他们测量了每种CAR设计使细胞吞噬靶点、产生炎性分子以及随后激活先前接触过该病毒的人类CD8 T细胞的能力。随后,他们将最有前景的设计转为靶向在多种实体瘤中过度表达的蛋白质间皮素的CAR,以评估在癌症环境中这些规则是否同样适用。
构建更强的吞噬者与信号放大器
结果呈现出明确的模式:基于CD32a的CAR在驱动吞噬方面持续表现出比采用传统CD3ζ域更强更快速的能力,尽管CD3ζ携带更多常见的激活基序。换言之,信号与巨噬细胞机械之间的“契合度”比单纯的信号强度更重要。在大多数条件下,在CD32a基础上叠加CR3衍生片段(CD11b或CD18)并未进一步提升吞噬能力,但确实提高了如TNF‑α和IL‑1β等关键炎性细胞因子的水平。含有TLR4的组合在增强炎性信号和表面标志CD86(与刺激T细胞能力相关)方面效果更显著,尽管这也带来了权衡:细胞表面的CAR表达水平降低以及吞噬能力有所下降。
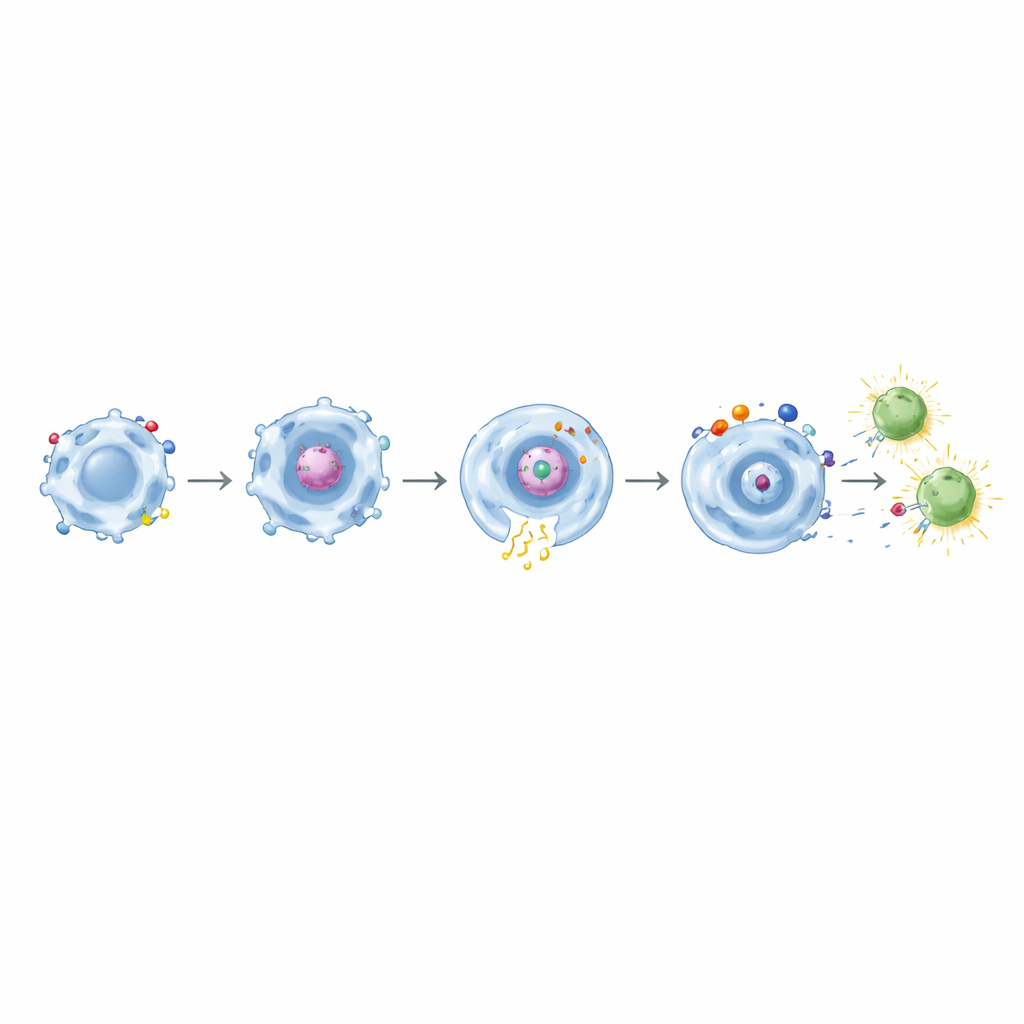
从吞噬到教育T细胞
关键的是,携带CD32a基CAR的巨噬细胞在吞噬刺突蛋白后,能够激活来自先前接种COVID‑19疫苗的人的记忆CD8 T细胞。这些T细胞开启早期激活标志并产生效应分子如干扰素‑γ和TNF‑α。将CD32a与CD11b、CD18或TLR4配对的双域CAR使这一效应更为强烈。当将类似靶向间皮素的设计用于工程化肿瘤细胞时,它们再次表现出精确的、依赖靶点的吞噬以及增强的炎性信号。在这些组合中,CD32a+TLR4组合作为一种强效的“组织警报”尤为突出,最有效地提升了细胞因子分泌和CD86表达,同时仍保持特异性的肿瘤吞噬能力。
这对未来治疗可能意味着什么
对非专业读者而言,这项研究表明对巨噬细胞进行工程改造并非一刀切的问题。通过替换和组合内部信号模块,科学家可以塑造出要么专注于高效清除病变细胞、要么更像免疫放大器、改变肿瘤抑制性环境并招募T细胞的细胞。基于CD32a的CAR成为这些设计的坚实基础,在巨噬细胞中优于传统的T细胞模块,并在病毒与肿瘤靶点中均显示作用。尽管这些结论来自实验室模型,仍需在原代人类细胞和动物中加以验证,但它们为下一代CAR巨噬细胞疗法提供了蓝图,可能通过将快速吞噬与精确的T细胞激活结合起来,更有效地应对实体瘤和持续性感染。
引用: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
关键词: CAR巨噬细胞, CD32a信号传导, 吞噬作用, 实体瘤免疫治疗, T细胞激活