Clear Sky Science · zh
通过使用深度学习技术的整合-微分方程框架进行癌症检测
为什么更聪明的扫描很重要
早期发现癌症可以挽救生命,但解读像钼靶这样的医学影像既困难又耗时,并且容易出现人为错误。医生必须在有限时间内将微弱的病变信号与正常组织和影像噪声区分开来。本文提出了一种新的辅助方法:将复杂的乳腺影像转化为更简单的一维信号,然后结合数学模型和人工智能来判断是否可能存在癌变。目标不是替代医生,而是为每次扫描提供更清晰、更可靠的线索。
将图像转为信号
作者首先重新思考了医学影像的表示方式。他们不是将钼靶视为一个巨大的像素网格,而是将其转换为一条汇总乳腺亮度变化的一维线状信号。首先对图像进行预处理:转换为灰度、去噪并进行强度平衡,使暗区与亮区可比。使用标准滤波器强调边缘和纹理,并以频域方式分析整体明暗模式(类似于将音频分为低频和高频)。随后逐行或逐列对像素值取平均,得到一条平滑的一维曲线。曲线中的峰值反映致密组织或可疑区域;谷值反映较为空旷的区域。尽管会丢失一些细节,但得到的是一种紧凑的信号,保留了诊断最相关的整体结构。 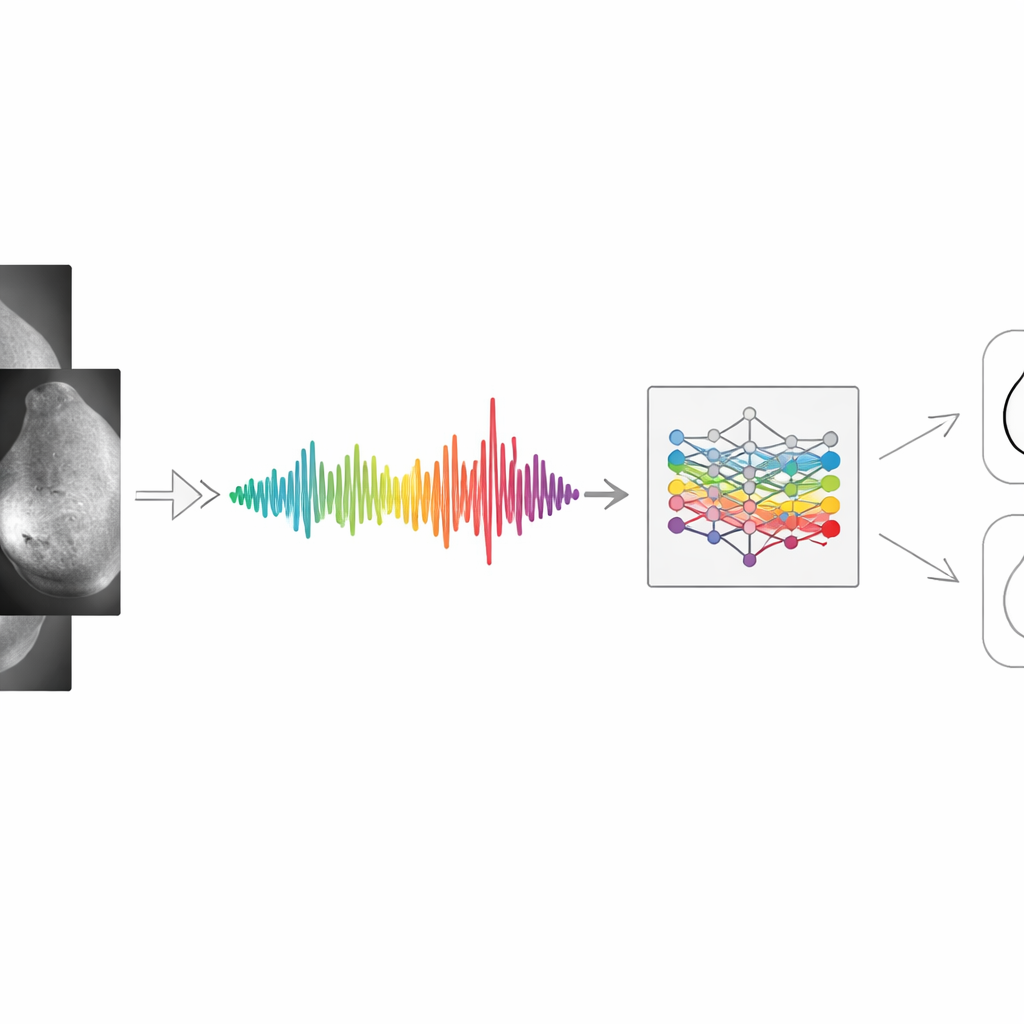
以方程为生物学增加一层解释
许多现有的深度学习系统直接在图像上工作,常被批评为“黑箱”,难以揭示肿瘤的实际行为。为了解决这一问题,作者在信号处理流程中嵌入了肿瘤生长的数学模型。他们使用积分-微分方程——既描述随时间变化又记忆过去状态的方程——来模拟癌细胞如何增殖、扩散并争夺血供。这些方程包含生长速率、拥挤限制、细胞运动和新血管形成等项。通过模拟肿瘤如何演化并影响钼靶中的亮度分布,框架产生了基于已知生物学而非单纯模式识别的额外特征。这些富化的信号旨在使最终预测对临床医生更具可解释性。
训练紧凑的神经网络来做出判断
在图像被转化为数学增强的信号后,一个精简的一维卷积神经网络(CNN)执行实际的分类。该网络沿着信号滑动小滤波器以检测关键形状——陡然跃变、平滑斜坡或重复波纹——这些都可能暗示异常组织。模型在公开的乳腺钼靶数据集(INbreast 和 MIAS)上进行训练,数据被划分为训练、验证和测试集以避免过拟合。作者通过信号增强和仔细调整模型参数来提高鲁棒性。为进一步打开黑箱,他们还应用了可解释性工具,突出显示对决策影响最大的信号部分,并将其关联回原始乳腺图像中组织密度或边界异常变化的区域。 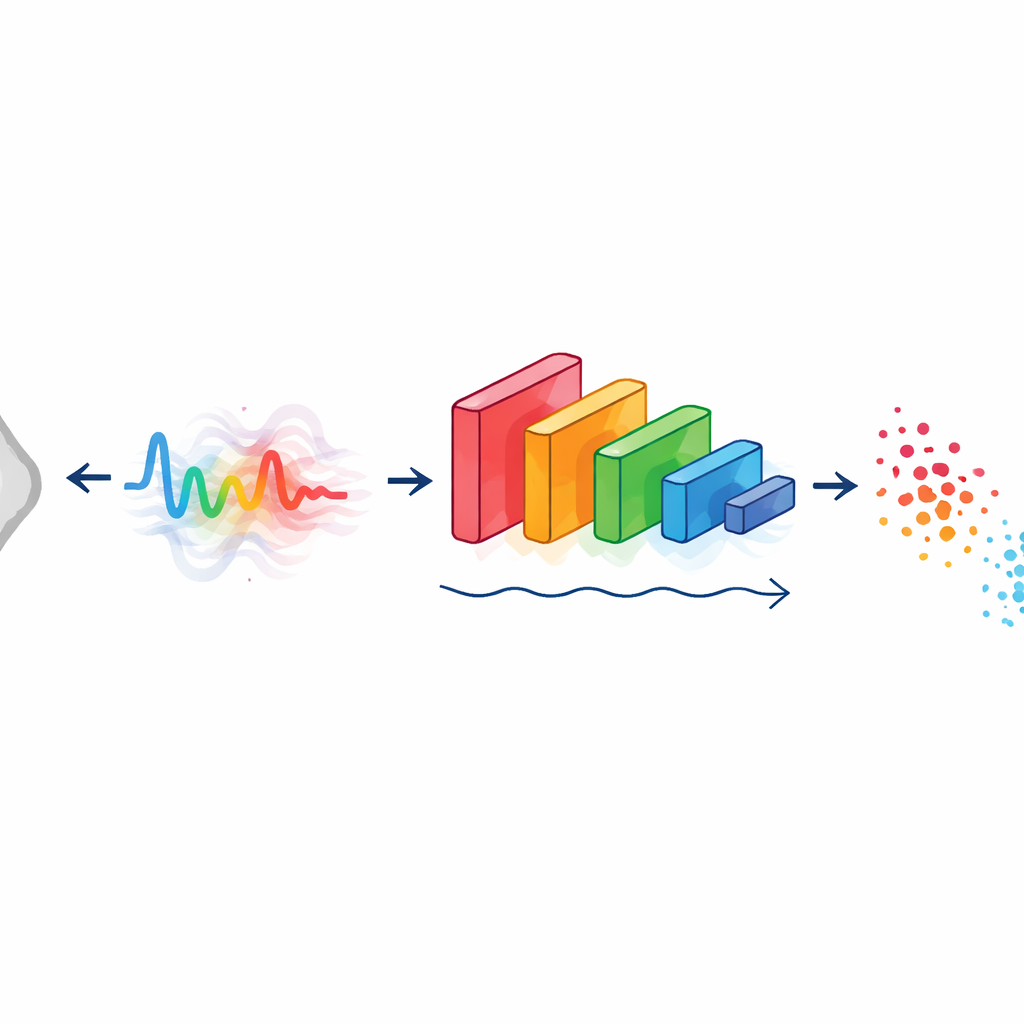
实际表现如何
在这些真实世界的钼靶集合上的测试中,该整合框架约96.4% 地正确区分了有癌与无癌病例,优于标准CNN、支持向量机、决策树及若干现代深度学习基线模型。它同时表现出高灵敏度(大多数癌症被成功检测)和高特异性(健康患者被误报的概率较低)。由于系统针对的是一维信号而非完整图像,它需要更少内存并能比许多大型基于图像的网络更快地给出预测,这对繁忙的门诊或算力有限的设备尤为重要。加入的数学建模似乎使关键特征更加清晰,在不显著增加计算代价的情况下提高了准确性。
未来可能的方向
作者总结道,将图像到信号的转换、肿瘤生长的数学模型与深度学习相结合,为更准确且更具可解释性的癌症筛查工具提供了一条有前景的道路。他们的方法仍处于早期阶段:主要在乳腺影像上验证,且在信号转换过程中可能丢失一些细微的视觉信息。未来工作将把方法推广到其他癌种,为医生提供更丰富的解释,并融合诸如组织切片、临床标志和遗传信息等附加数据。经过更广泛的验证,这类以数学为导向的人工智能最终可能支持实时决策系统,帮助放射科医生更早、更自信地发现癌症。
引用: Gopisairam, T., Thota, S. & Bikku, T. Integrative framework for cancer detection via integro-differential equations using deep learning techniques. Sci Rep 16, 9714 (2026). https://doi.org/10.1038/s41598-026-39283-z
关键词: 癌症检测, 医学影像, 深度学习, 数学建模, 乳腺钼靶