Clear Sky Science · zh
用于放射生物学模拟的细胞核间相聚合物物理模型
为何我们DNA的“住处”形态至关重要
辐射在医学上是一把双刃剑:它能杀死癌细胞,但也可能损伤健康组织。无论是风险还是益处,其核心都是紧密封装在细胞核内的DNA。本文展示了如何通过一个基于物理学的三维详细模型——将细胞核比作“DNA城市”——帮助科学家预测辐射如何断裂并错误修复染色体,从而有望改进癌症治疗和太空辐射风险评估。
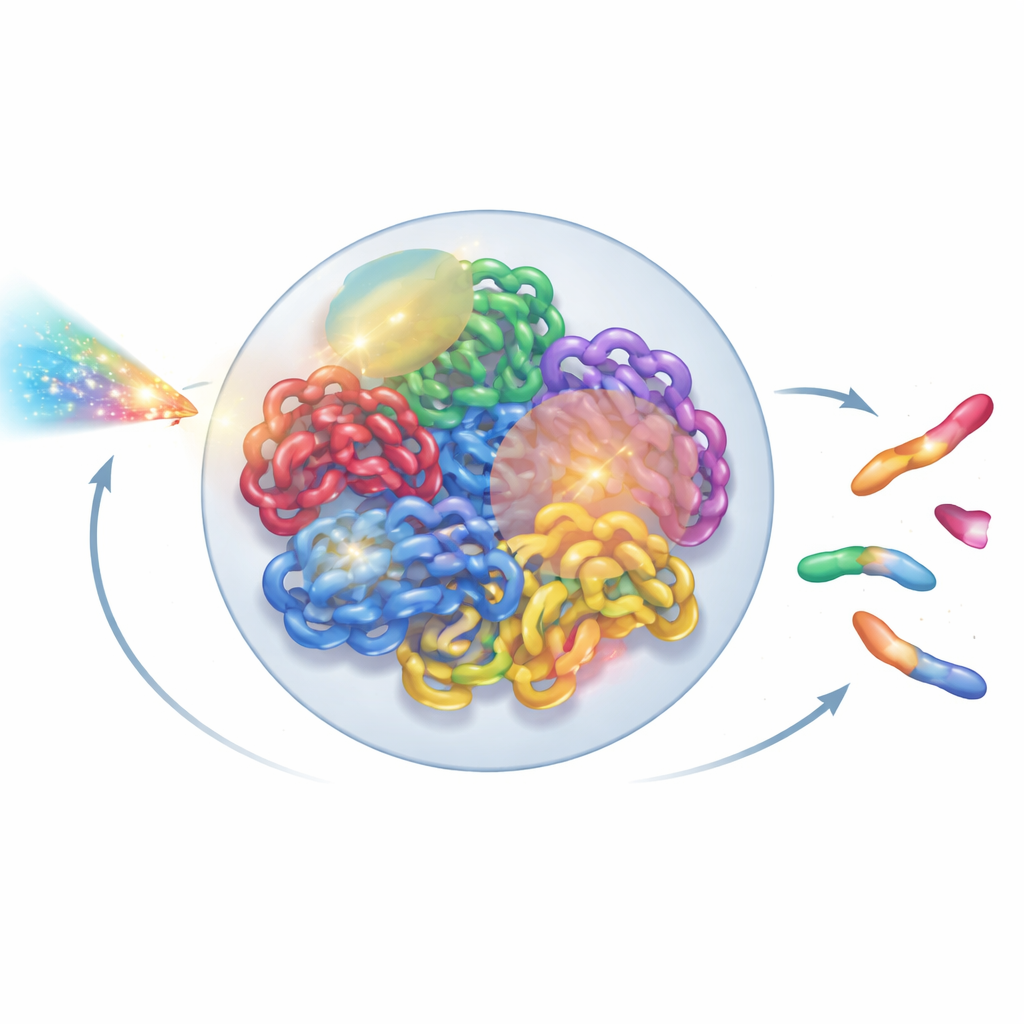
把基因组视为一种活的结构
在每个人类细胞内,约两米长的DNA被折叠进仅数微米宽的细胞核中。这种折叠并非随机:每条染色体倾向于占据自己的领域,这些领域又细分为邻里区和环路域。超分辨率显微镜和Hi-C接触图等新实验工具,已令人惊讶地揭示了这种复杂的三维排列。然而多数辐射模型仍将DNA简化为线状纠缠或理想化环路,忽略了这种更高阶的组织结构。作者着手构建一个尊重生物学观测的整核模型,同时仍能在普通实验室计算机上快速运行。
用聚合物物理构建虚拟细胞核
研究团队将染色体模拟为柔性链条,借用了研究塑料和软物质的聚合物物理学思想。他们将问题分为三个弛豫阶段以控制巨大的计算开销。首先,在细胞核内放置称为染色质域的大型构建模块,允许它们相互排斥、沿长度伸展并聚集成更大的亚区。其次,在每个域内放大查看以布置更细的染色质纤维,包括由结合蛋白维持的环路区域。第三,让所有纤维在核边界内再次自由相互作用以接近现实的最终构型。通过这样分阶段处理并加入分层搜索与并行计算技巧,他们将运算时间从不切实际的四个月缩短到在一台64核工作站上每个虚拟细胞核大约三小时。
从辐射轨迹到DNA断裂与修复
虚拟细胞核构建完成后,作者叠加了由Geant4-DNA模拟产生的详细辐射轨迹。他们使用分层搜索来定位每个电离事件最近的染色质域、纤维片段,最终定位到核苷酸,而无需将所有一百亿个核苷酸位置一次性存入内存。相反,他们保留了可重用的染色质模板并实时应用巧妙的坐标变换。发生在DNA骨架处的电离被视为链断裂,位于相对链上近邻的断裂则被合并为双链断裂。为模拟细胞的修复机制,作者引入了基于距离的重连规则:彼此接近的自由DNA末端更可能重新连接。重连决策逐步进行,直到所有末端要么配对完成,要么保持未修复,重现了正确修复与错误缝合的两类结果。
用网络逻辑整理断裂的染色体
在这次虚拟修复之后,细胞核中既有重组的染色体,也有残留片段。为对结果进行分类,作者将修复后的基因组转换为无向图:染色体片段作为边,其端点与断点作为节点。他们用标准的连通分量算法自动重建每一个新的类染色体对象并统计关键特征,例如着丝点(细胞分裂的附着点)和端粒(天然末端)的数量。由此识别出二着丝点染色体(有两个着丝点)、环形染色体和缺失。他们随后将模拟结果与经典的人类皮肤细胞在伽玛射线和α粒子照射下的实验数据比较,发现总染色体畸变数在约20%以内复现了观测值,这较早期模型有显著改进。
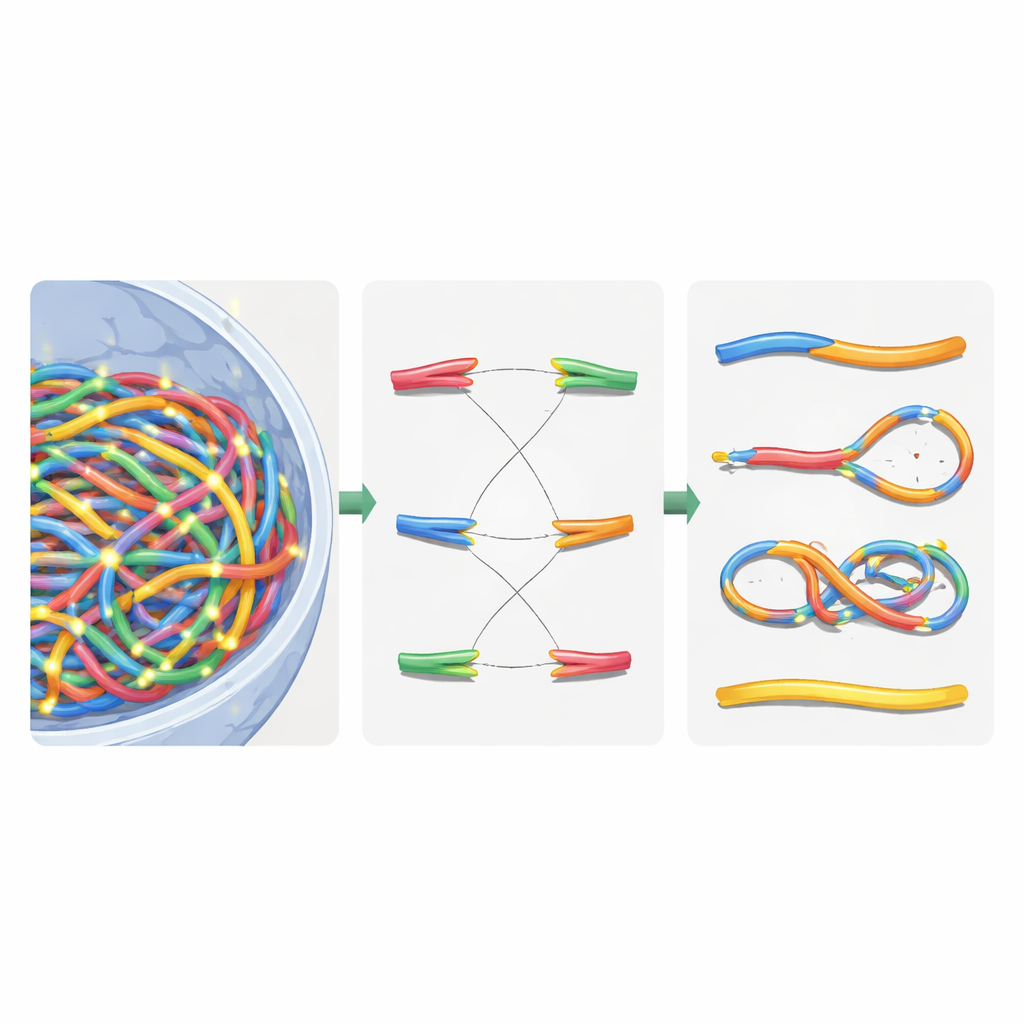
对病人和宇航员意味着什么
简而言之,这项工作表明DNA在细胞核中的“位点”和“折叠方式”会强烈影响辐射损伤如何累积成危险的染色体改变。通过结合现实的三维基因组结构、高效的基于物理的模拟和基于图的方法来读取断裂染色体,作者搭建了结构生物学与放射生物学之间的一座强有力桥梁。他们认为,未来的改进——例如加入详细的修复时序和使用全基因组测序数据——能使该方法在预测用于癌症治疗或在深空遇到的高能粒子生物影响方面更为准确。归根结底,对细胞内DNA“居所”更好的建模,可能有助于定制更安全、更有效的放射治疗并深化我们对长期辐射风险的理解。
引用: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
关键词: 辐射诱导的DNA损伤, 染色质三维结构, 染色体畸变, 聚合物物理建模, 粒子治疗