Clear Sky Science · zh
基于多模态信息融合的急性主动脉综合征 AI 驱动诊断
这对胸痛患者为何重要
急性主动脉综合征是一种医疗急症,主干动脉可能突然发生撕裂,如果漏诊,数小时内就可能致命。然而其症状常常伪装成心肌梗死、肌肉拉伤甚至消化不良,因此极易被误诊。本文介绍了一种新的人工智能系统,它将 CT 扫描与血液检测相结合,帮助医生更早、更准确地识别这些隐匿的动脉灾难,并对需复查的边界病例给出提示。
隐藏在表象之下的危险撕裂
急性主动脉综合征(AAS)包括主动脉壁的几种相关病变,如经典夹层、壁内血肿和穿透性溃疡。它们共有的危险是:血液侵入或穿透血管壁,这可能迅速导致破裂或重要器官供血中断。症状出现后头一两天内风险最高,如果不及时处理,死亡率可能接近 70%。医生使用 CT 血管造影查看主动脉,并用 D-二聚体及炎性标志物等血检指标评估凝血与免疫活动。但患者主诉往往含糊,体检可能蒙蔽观察,CT 图像有时细微或因运动伪影而退化,因此在常规临床中大约三分之一的病例最初被漏诊。
现有 AI 工具遗漏了什么
近年来出现了强大的图像识别系统,可以扫描 CT 或 X 光图像寻找主动脉撕裂的迹象。然而,大多数此类工具只看图像而忽略血检,或者只是将不同数据流机械地拼接在一起,却没有真正学会它们如何相互作用。这与临床医生的思考方式不符:临床医生会将影像所见与实验室数值和病史综合起来判断。简单地“堆叠”影像特征与检验数值反而可能带来问题,因为血检数据通常嘈杂、不完整且在数学上相互关联。许多 AI 模型还以黑箱形式运作,只给出结论而不展示推理过程,这使得急诊医生在生死攸关时对其依赖持谨慎态度。
一种融合影像与血检的新方法
作者构建了一个多模态多尺度融合(MMMF)模型,旨在模拟有经验的放射科医生与心脏病专家的推理方式。首先,一个双分支的影像编码器以两种尺度观察 CT 血管造影:大块视野把握主动脉的整体形状与走行,小块视野聚焦细微处,如微小的内膜裂口或壁内小血肿。同时,关键血液指标——包括 D-二聚体和由白细胞计数与血小板推导出的炎性指标面板——被转换为数值特征点。这些影像特征与化验特征作为图结构中的节点,由先进的图神经网络在它们之间传递“信息”,学习某些血液模式如何强化或抵触影像上的细微信号。
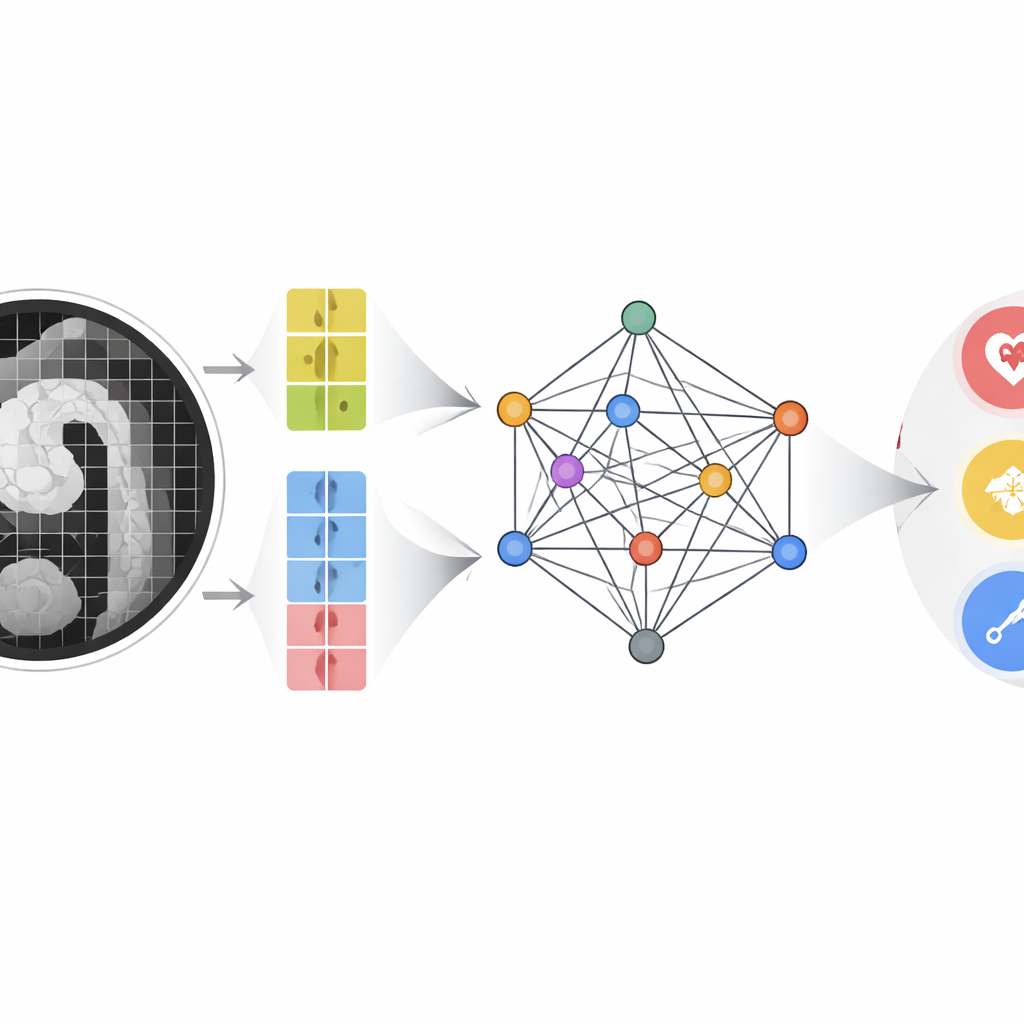
系统的表现如何
研究团队在 2019 至 2024 年间收集的 493 例同时具有 CT 扫描与血检的患者数据上训练和测试了 MMMF 模型,覆盖各种确诊的 AAS 病例及非 AAS 对照组。他们将该方法与常见的仅影像模型、仅血检模型以及若干最先进、原本用于图像与文本配对的多模态系统进行了比较。在准确率、精确率、召回率和 F1 分数等指标上,MMMF 模型均名列前茅。其受试者工作特征曲线下面积(AUC)超过 0.9,表明能较好地区分正常主动脉、涉及升主动脉或降主动脉的经典夹层以及非典型形式。影像数据依旧是单一信息源中最强的,但与血检数据经过精心结构化融合后带来了可测的提升,尤其在难判或边界病例中更为明显。消融实验表明两个要素至关重要:双尺度影像通路以及用于建模特征间长程关系的基于 transformer 的图结构。
迈向医生与机器的协作
除了总体准确率数字外,这项工作的关键贡献在于强调协作而非替代。该系统尤其擅长快速筛除明显正常的扫描和明确异常的非典型病例,充当一种智能的前线筛查工具。同样重要的是,它能够识别自身信心较低的情况——这些情况常常也是人类专家感到棘手的,比如早期或轻度的夹层——从而将这些患者标记为需紧急复核、追加影像或高级会诊。实质上,研究表明,当影像细节与血检线索以结构化、临床启发的方式交织在一起时,人工智能既能提升急性主动脉综合征的早期诊断,又能作为防止遗漏的安全网,同时把最终决策权牢牢留在医生手中。
引用: Yang, Z., Xu, S., Wang, B. et al. AI-driven diagnosis of acute aortic syndrome based on multi-modal information fusion. Sci Rep 16, 8332 (2026). https://doi.org/10.1038/s41598-026-39111-4
关键词: 急性主动脉综合征, 主动脉夹层, 医疗人工智能, 多模态诊断, 图神经网络