Clear Sky Science · zh
Dlgap2 缺失通过促进泛素介导的 Itsn1 降解破坏突触稳态:基于丙戊酸诱导的自闭症样模型
为何常用药与脑回路重要
丙戊酸是一种长期用于癫痫和情绪障碍的药物,但在妊娠期使用与子代自闭症风险升高有关。本研究提出了对家庭和医生都很重要的一个问题:这种药物究竟如何影响发育中大脑的连线?通过追踪至突触——神经细胞之间的通讯点——中特定分子的变化,研究者揭示了一条新的事件链,可能有助于解释类自闭症行为并指向未来的治疗策略。
跨物种寻找共有的脆弱环节
为了寻找可靠线索,研究团队没有仅依赖单一动物模型。他们比较了在出生前暴露于丙戊酸的人类皮质类器官、猴子、大鼠和小鼠的脑或类脑组织。通过大规模基因和蛋白质调查,他们识别出一小组在所有这些系统中均发生改变并与突触及神经纤维绝缘有关的基因。其中,Dlgap2 脱颖而出:这是一种有助于组织兴奋性突触突触后侧的支架蛋白。在接受产前丙戊酸处理的小鼠中,皮层中 Dlgap2 水平下降,且更具体地在微小的突触区室内减少,表明这一维持结构的分子是药物暴露的主要受害者之一。
从分子变化到行为改变
作者接着问:单独丧失 Dlgap2 是否足以扰乱大脑功能。他们使用携带短发夹 RNA 的病毒在培养的小鼠神经元和新生小鼠中降低 Dlgap2。在培养皿中,Dlgap2 降低的神经元树突分支更短且突触后点减少,表明连接被削弱。在活体中,针对性敲低脑内 Dlgap2 导致类自闭症行为:雄性幼鼠在水迷宫隐匿平台定位学习中表现困难,且在三腔室测试中对社交伙伴和社交新颖性的兴趣减少。这些变化模拟了产前暴露丙戊酸动物所见的学习和社交缺陷,进一步支持 Dlgap2 丧失不仅是副作用而是导致行为改变的驱动因素。
在突触中找到易受损的搭档
为了理解 Dlgap2 丧失如何在突触内产生连锁反应,研究者更仔细地观察了锚定在突触后致密区的蛋白质——这个富含分子的垫层负责接收化学信号。通过蛋白质组学,他们发现降低 Dlgap2 改变了数百种突触蛋白的丰度,尤其是那些参与突触组织和通过内吞回收囊泡的蛋白。其中一种蛋白 Intersectin‑1(Itsn1)下降得尤为明显。进一步的生化研究显示,Dlgap2 与 Itsn1 在突触富集的分馏中物理上共存于同一蛋白复合体中,且两者都出现在与自闭症相关的基因名单中。这指向了在拥挤的突触环境中,两种分子之间的一种集中的调控伙伴关系。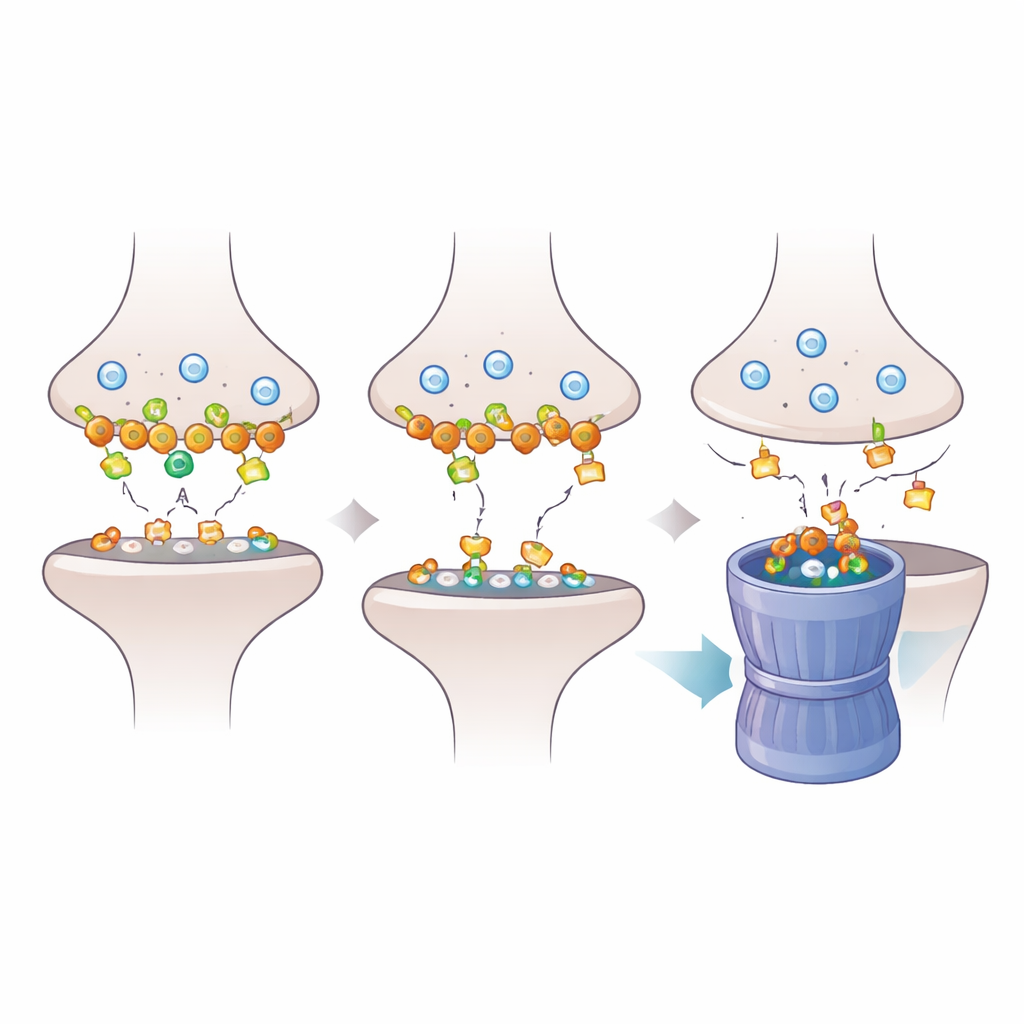
一种隐藏的降解通路浮出水面
团队接着探究为何在 Dlgap2 缺失时 Itsn1 水平下降。他们观察到在突触区室内,Dlgap2 敲低触发了一种称为 K48 连接型泛素化的蛋白标记方式,该标记将蛋白导向细胞的蛋白酶体“粉碎机”降解。用药物 MG132 阻断这一降解系统可以防止 Itsn1 的丧失,表明 Dlgap2 通常保护 Itsn1 不被标记和销毁。没有 Dlgap2,Itsn1 被更多地标记、送入蛋白酶体并从突触中耗尽,从而破坏内吞回收和突触活动的平衡。这项工作表明,关键蛋白周转速率的细微变化就足以在大脑发育期间使突触失稳。
这对自闭症和未来治疗意味着什么
综合来看,该研究向非专业读者提出了一个简明而有力的观点:产前暴露于丙戊酸可以削弱突触处的一种结构“支撑”蛋白(Dlgap2)。当该支撑丧失时,它的搭档蛋白(Itsn1)更易被细胞垃圾处理系统过度靶向,导致突触组分回收失常,最终引发连线错误和小鼠的类自闭症行为。虽然许多基因和环境因素共同影响自闭症的发生,但这个 Dlgap2–Itsn1 轴提供了一条从产前药物暴露到大脑功能改变的具体分子链。长期来看,保持这一伙伴关系或微调突触处的蛋白降解机器的策略,可能有助于保护发育中的大脑免受类似的破坏。
引用: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
关键词: 妊娠期丙戊酸, 突触支架蛋白, 自闭症谱系机制, 泛素-蛋白酶体途径, 小鼠自闭症模型