Clear Sky Science · zh
通过生物活性基质水凝胶的牵引力传递促进由整合素介导的上皮集体迁移
细胞如何协同牵拉以实现愈合
当皮肤被割伤或器官受损时,细胞层必须协调移动以封闭伤口。本研究提出了一个看似简单的问题:当细胞一起爬行时,它们仅仅互相拉扯,还是也通过下面的软性材料“交流”?通过在实验室中重建真实的凝胶状环境,作者展示了细胞可以通过这种软基质传递机械力来引导群体运动,揭示了一种隐藏的通讯层,这对伤口愈合、组织修复甚至癌症扩散可能至关重要。
承载力的柔软地基
在我们体内,许多细胞依附在柔软、富含蛋白质的支架上,而不是像玻璃或塑料那样的刚性表面。为了模拟这一点,研究人员在由Matrigel和胶原组成的生物活性水凝胶上培养了作为连续片的肾上皮细胞,这两种成分是天然组织的常见成分。随后他们在凝胶中间制造了一个小空区,类似微小的伤口,并观察细胞片如何向内推进以填补空隙。为了跟踪细胞内部一个关键信号通路的活性,他们使用了荧光生物传感器来报告ERK的活性,ERK是一种常常对机械线索作出反应的蛋白。这一设置使他们能实时观察软凝胶中的机械力如何与细胞运动和内部信号关联。 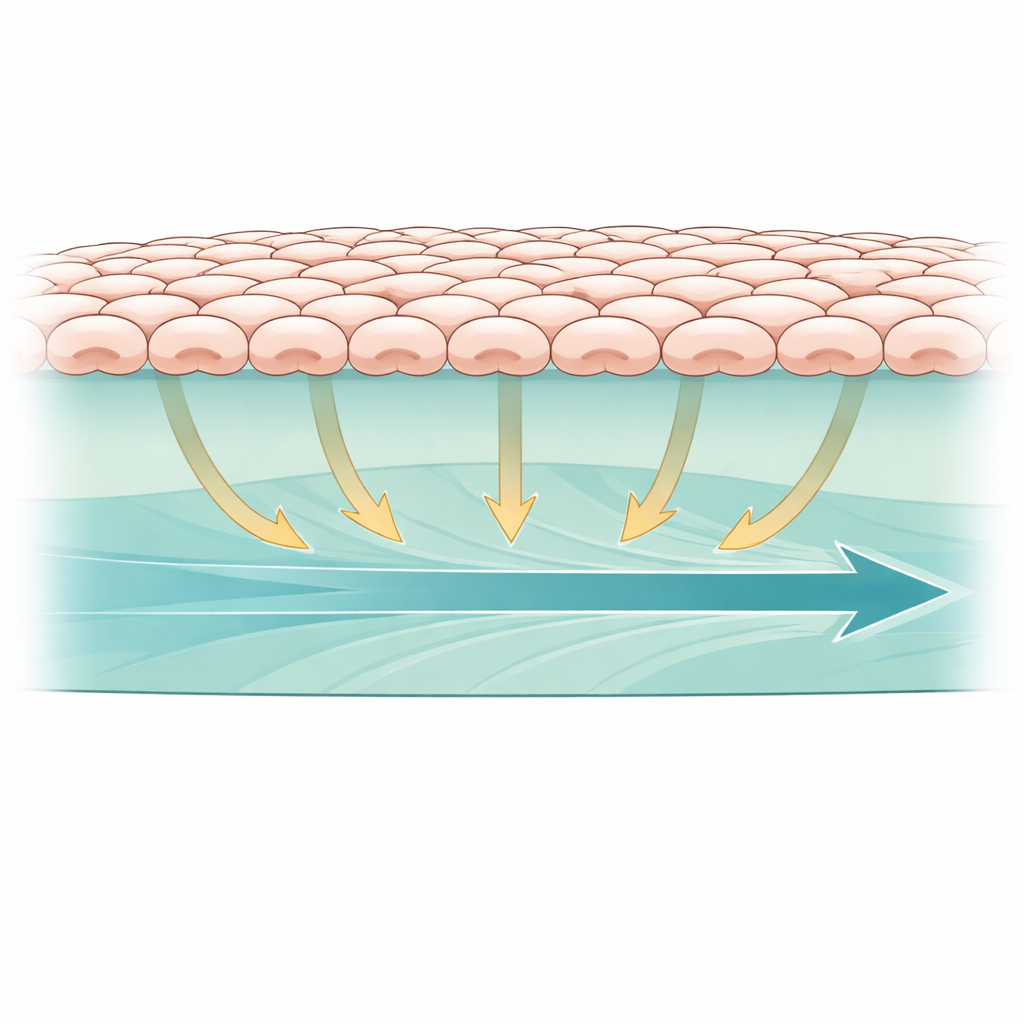
看见细胞下方地基的移动
为判断凝胶是否真正承载并传递力,团队在材料中混入微小的磁性微珠,并在细胞迁移过程中追踪它们的运动。在含有Matrigel和胶原的正常凝胶上,微珠缓慢向前滑动,与前进的细胞片方向一致,表明细胞在抓取并拖动下方的基质。而在仅含Matrigel的凝胶上,微珠移动得更慢,表明力传递较弱。当凝胶用戊二醛化学交联以变硬并“锁定”网络时,微珠几乎没有移动。在这些被锁定的条件下,细胞仍能附着,但集体推进明显减慢,ERK信号变弱且在前缘不再集中,将强基质牵引与更快、更定向的群体运动联系起来。
内部发动机与离子门驱动运动
作者接着探查了细胞内部是什么产生这些牵拉力以及这类活动如何被感知。他们使用药物阻断基于肌球蛋白的收缩,这种分子机械装置与肌肉驱动的机制相同。当收缩被抑制时,ERK活性下降,细胞片前进速度变慢,这与内部牵拉需要将张力传递到基质的想法一致。他们还干扰了细胞膜上和内部钙储库中的几类钙通道。阻断这些离子通路会减弱ERK活性并减慢集体迁移,指向这样一系列事件:对基质的机械拉扯被转化为钙信号和ERK信号,从而帮助群体维持协同前进。
通过表面抓握引导方向
一个尤为引人注目的发现来自对整合素的靶向,整合素是作为将细胞与其周围环境连接起来的小锚点的表面分子。当研究人员阻断一种主要的整合素亚型时,细胞片不再作为连贯的前沿向前推进,尽管单个细胞仍能在局部以几乎正常的速度摆动。同时,凝胶中微珠的运动几乎停止,表明整合素对将收缩细胞产生的力传递到基质至关重要。相比之下,阻断与Piezo1相关的机械敏感通道(帮助细胞感受物理压力)则既降低了迁移速度,也削弱了凝胶中的牵引力。这些结果共同勾勒出这样一幅图景:收缩产生力,整合素将其传递给基质,机械敏感通道与ERK信号解读这些力,以协调集体移动的方向性和效率。 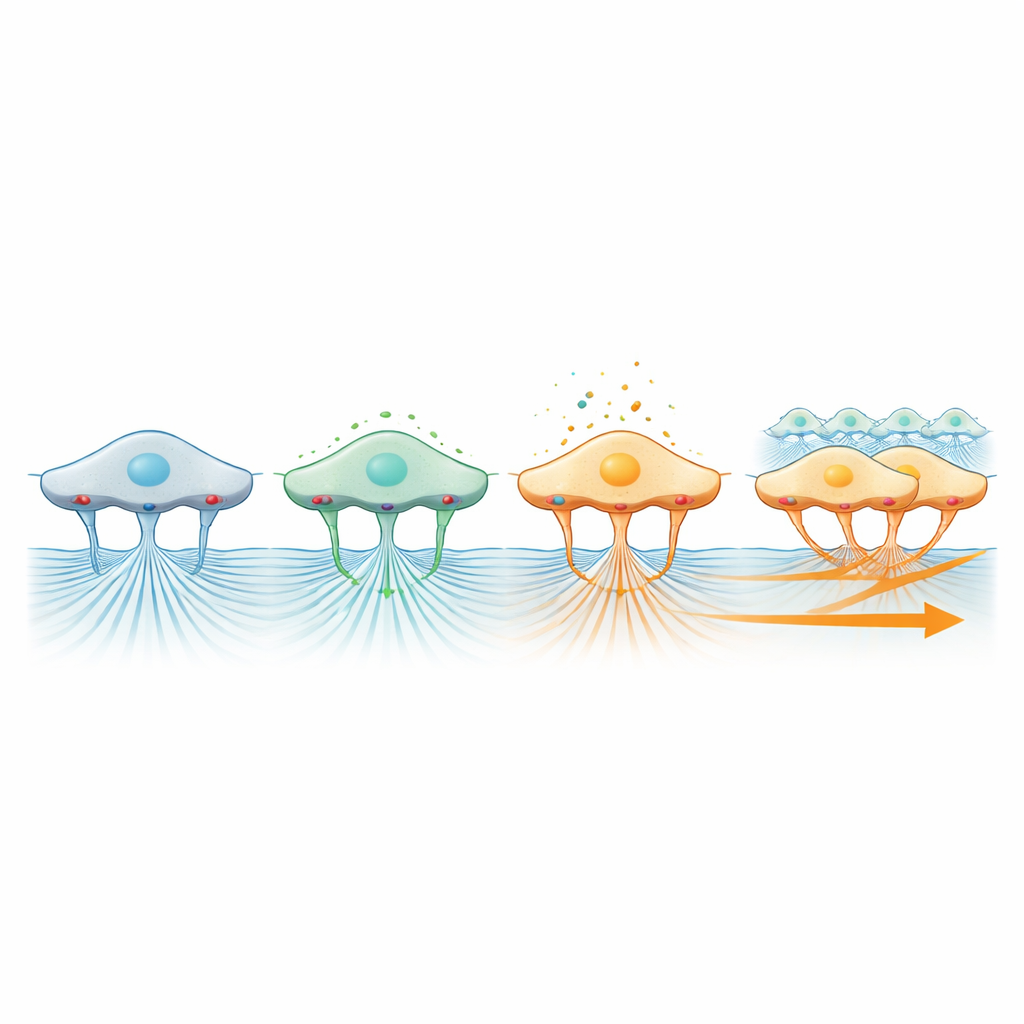
这对愈合与疾病意味着什么
简而言之,这项工作表明,细胞片不仅仅相互拉扯;它们还拉扯并穿过下面的柔软材料,将其用作一种机械上的“电话线”。细胞层的收缩将张力传递通过基质,而这种张力通过整合素和离子通道被感知,并由ERK活性读出,帮助细胞群体快速且统一地移动。当基质被化学锁定以阻止力传播,或关键的表面锚点与感受器被阻断时,集体推进就会受挫。这些见解加深了我们对伤口闭合、组织维持结构以及侵袭性细胞群(如癌症和纤维化中)可能如何利用其环境中的机械通路进行扩散的理解。
引用: Ouyang, M., Cao, Y., Sheng, H. et al. Traction force transmission via bioactive matrix hydrogel promotes epithelial collective migration mediated by integrin. Sci Rep 16, 8923 (2026). https://doi.org/10.1038/s41598-026-39048-8
关键词: 细胞集体迁移, 机械信号传导, 细胞外基质, 整合素, 伤口愈合