Clear Sky Science · zh
通过计算筛选可吸入的小分子IL-33/ST2拮抗剂以针对严重2型高炎性哮喘亚型
这为何与呼吸息息相关
对于数以百万计的重度哮喘患者来说,即便使用现代吸入器和先进的注射疗法,他们仍可能气短并面临危险性发作的风险。本研究探讨是否可以将常见的类片剂药物重新设计为吸入给药的形式,从而阻断肺部哮喘上游的“警报”信号之一。研究者仅使用计算机模拟,筛选可能嵌合到与严重过敏驱动性哮喘相关的关键受体上的小分子,为未来的实验室验证奠定基础,而非提出可立即使用的药物。
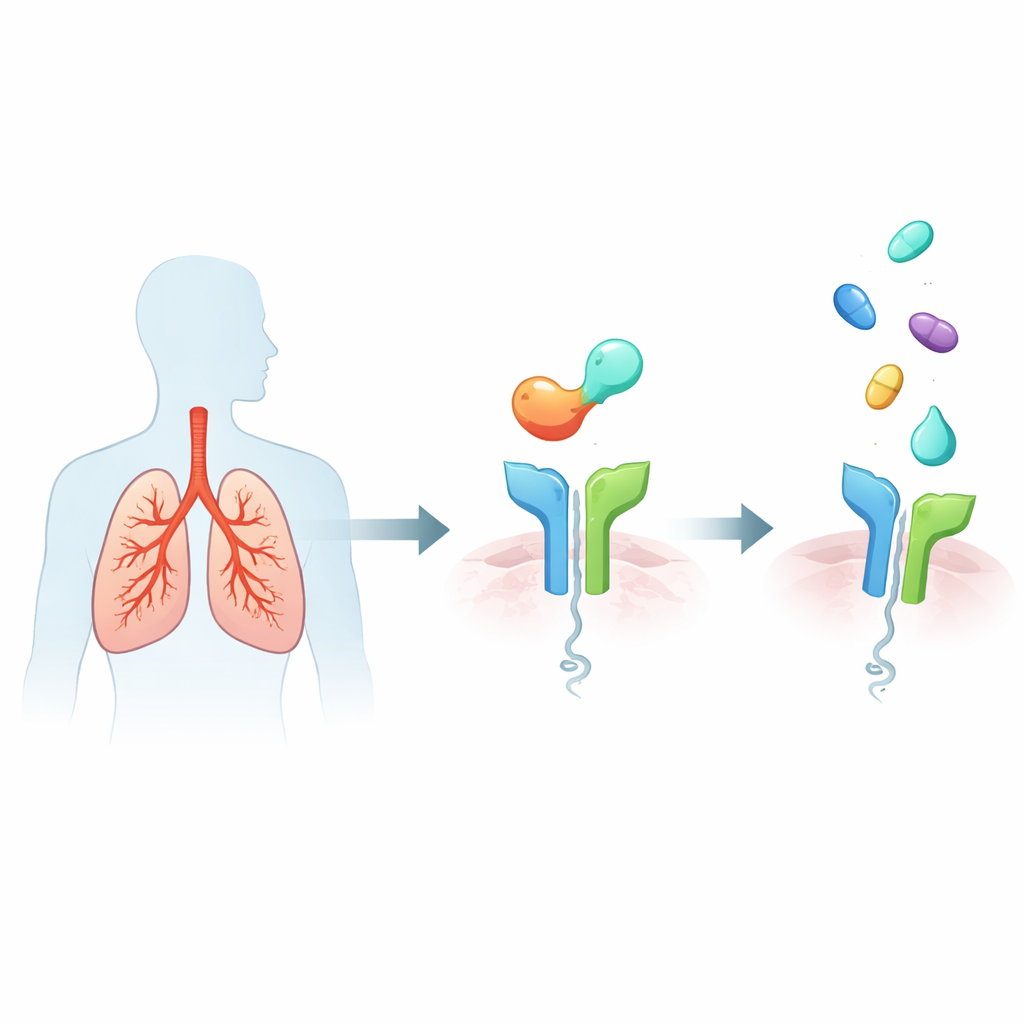
哮喘患者肺内的警报系统
重度2型高炎性哮喘以免疫反应过度活跃为特征,气道充满黏液和炎性细胞,气道变窄并随着时间损伤肺结构。一个主要触发因子是由受压的气道上皮细胞释放的蛋白质IL-33。IL-33与多种免疫细胞表面的ST2受体结合,促使它们释放强效的信使分子,驱动哮喘典型特征,如喘息、急性加重和长期气道重塑。鉴于较高的IL-33/ST2活性与症状更重、发作更频繁相关,ST2成为一个有吸引力的上游靶点:若能阻断ST2,可能同时抑制许多下游炎症信号。
从抗体到日常型小分子药物
目前若干针对重度哮喘的疗法使用注射抗体,在血液中清除炎性蛋白或阻断其受体。尽管对部分患者有效,这类生物制剂成本高昂、需注射给药,且主要针对通路下游的信号。相比之下,小分子药物——更像传统的片剂或吸入剂——可规模化生产、易于储存并有望直接送入肺部。挑战在于ST2通过广泛的蛋白-蛋白界面与IL-33结合,这对小分子而言比酶上一个深而整洁的口袋更难干扰。作者因此借助ST2–IL-33复合物的高分辨率结构数据和现代计算工具,查看是否有已知的抗炎小分子出人意料地能嵌入该界面的一部分。
通过计算机搜索受体表面
研究团队使用了人类ST2与IL-33结合的晶体结构,首先移除了IL-33以暴露受体的结合表面,并使用口袋检测程序定位最适合小分子嵌入的区域。随后他们挑选了十种在哮喘或相关免疫疾病中已有临床用途的小分子——例如白三烯拮抗剂孟鲁司特和扎鲁司特、免疫调节的沙利度胺衍生物以及JAK抑制剂——以及一已报道的针对ST2的分子作为参考。利用虚拟对接软件,每个化合物在ST2表面被定位数千次,最佳构象按预测结合强度评分。扎鲁司特成为排名最高的骨架,略微优于孟鲁司特和已知的ST2指向比较物。
在屏幕上优化先导分子
由于扎鲁司特在预测结合力和总体药物性之间显示出最有前景的平衡,作者使用AI指导的设计工具对该分子进行了改造。目标是在保持其对ST2结合能力的同时改善预测的安全性特征。重新设计的类似物具有非常接近的对接评分,并在计算上预测毒性较低。详尽的接触图显示,母体和改造化合物均接触到若干通常与IL-33接触的ST2氨基酸,暗示它们占据了界面的功能性重要部位。延长的分子动力学模拟——在水和盐溶液中进行的半微秒虚拟运动——显示受体与配体均保持柔性,小分子沿表面取样不同位置而非僵硬锁定。随时间计算的相互作用能量指向有意义但动态的结合,符合小分子在相对平坦的蛋白-蛋白表面上探测性的结合模式。
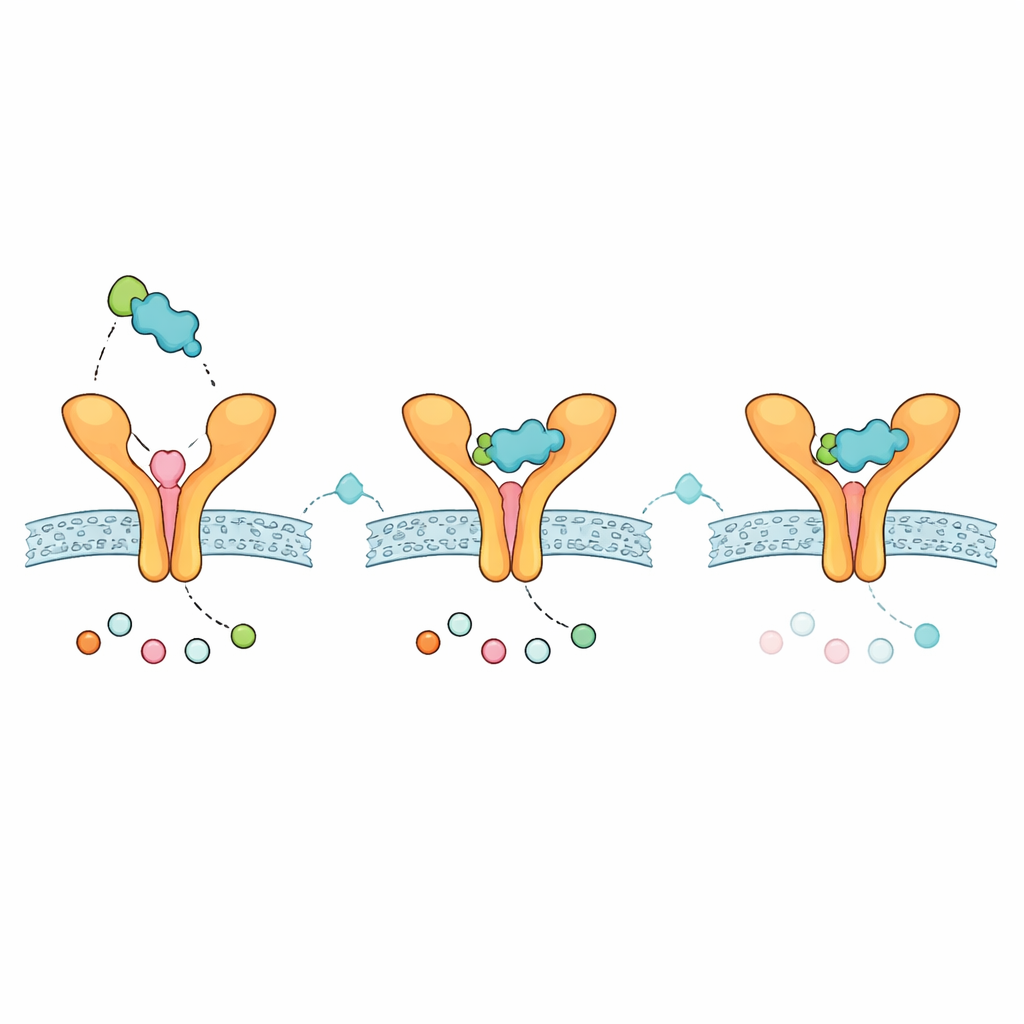
关于未来吸入剂行为的线索
为评估改造后扎鲁司特是否具有作为药物的可行性,团队进行了标准的计算吸收、分布、代谢、排泄和毒性(ADMET)检查。该类似物满足常见的口服药物可行性规则,显示出中等的分子量和脂溶性,并被预测难以进入脑部——这些特征可能有利于以肺为主要作用部位、全身副作用有限的治疗。溶解度估计因模型而异,暗示在配方上需谨慎处理,尤其是非口服给药路线如吸入。该化合物还被预测会与某些肝脏酶相互作用,提示若与其他药物合并使用时需关注潜在的药物相互作用。
这项工作真正表明了什么
这项研究并非交付一种新的哮喘药物,而是展示了一套逐步的计算策略,用于发现和优化可能干扰气道细胞表面IL-33/ST2警报系统的小分子。它指出了扎鲁司特及其AI优化的类似物作为可进入实验室验证的合理起点,显示它们能占据ST2界面的关键部分并具有总体可接受的预测安全性和药物特性。然而,所有证据均为虚拟:该工作并不能证明这些分子能阻断IL-33与ST2结合、抑制炎性信号或改善患者的呼吸。这些问题需要通过生化检测、细胞研究、动物模型以及最终的临床试验来回答。目前,该研究提供了一条计算路线图和一份候选骨架的简短清单,供科学家将机体自身的哮喘警报开关转化为实际、可吸入的药物靶点时参考。
引用: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
关键词: 重度哮喘, IL-33 ST2途径, 小分子拮抗剂, 计算机药物设计, 吸入性治疗