Clear Sky Science · zh
MUC14 通过整合素 α8β6/PI3K/AKT/MAPK 调控顺铂反应与免疫,从而抑制肺腺癌
这项肺癌研究为何重要
肺腺癌是最常见的肺癌类型,常以化疗药物顺铂治疗。不幸的是,许多肿瘤会获得对该药的耐受性,患者长期生存率仍然偏低。本研究揭示了一种鲜为人知的细胞表面蛋白 MUC14,它似乎在肺肿瘤上发挥天然制动作用。理解 MUC14 的作用机制可能为提高化疗效果并增强免疫系统识别和清除癌细胞开辟新途径。
隐身却具有保护作用的蛋白
MUC14(又称 endomucin)位于细胞表面,属于一类糖衣修饰的蛋白——黏蛋白家族。通过挖掘大型公共癌症数据库并分析患者样本,研究者发现肺腺癌肿瘤通常比邻近正常组织产生更少的 MUC14。肿瘤中维持较高 MUC14 水平的患者比低表达者具有更长的生存期和更慢的疾病进展。在多种癌症类型中,MUC14 多呈下调趋势,提示它更常充当抑癌因子而非促癌因子。 
减缓癌细胞并缩小肿瘤
为探明 MUC14 的实际功能,团队在肺癌细胞系中操控其表达。当强制使细胞过表达 MUC14 时,细胞分裂变慢、迁移减少,并且侵袭基质模拟凝胶的能力下降。它们黏附关键支架分子的能力也变弱,形成的克隆数量和体积均减少。在小鼠体内,经工程化使其过表达 MUC14 的癌细胞在皮下形成的肿瘤更小,静脉注射后在肺部的转移灶也更少。相反,当用小干扰 RNA 抑制 MUC14 时,则出现相反变化:细胞增殖更快、运动性更强、黏附性提高并形成更多克隆,均表明癌性行为更具侵袭性。
在细胞表面切断生长信号
作者随后探讨了 MUC14 如何发挥这些强大效应。他们将注意力集中在整合素上——一类将细胞锚定于周围基质并将生长与存活信号传入细胞的受体蛋白。来自数百例肺肿瘤的数据指出 MUC14 与两种整合素组分 α8 和 β6 之间存在强相关性,它们在细胞表面形成配对。研究者使用一种基于光学、可检测彼此相距十亿分之一米级别蛋白相互靠近的技术,证实 MUC14 与 α8β6 整合素复合体在细胞膜上并列存在。过量 MUC14 干扰了这些整合素的聚集,并抑制了它们通常激活的两条主要生长通路:PI3K/AKT 与 MAPK/ERK。当 MUC14 水平降低时,这些通路活性增强,部分解释了为何癌细胞更易生长与扩散。 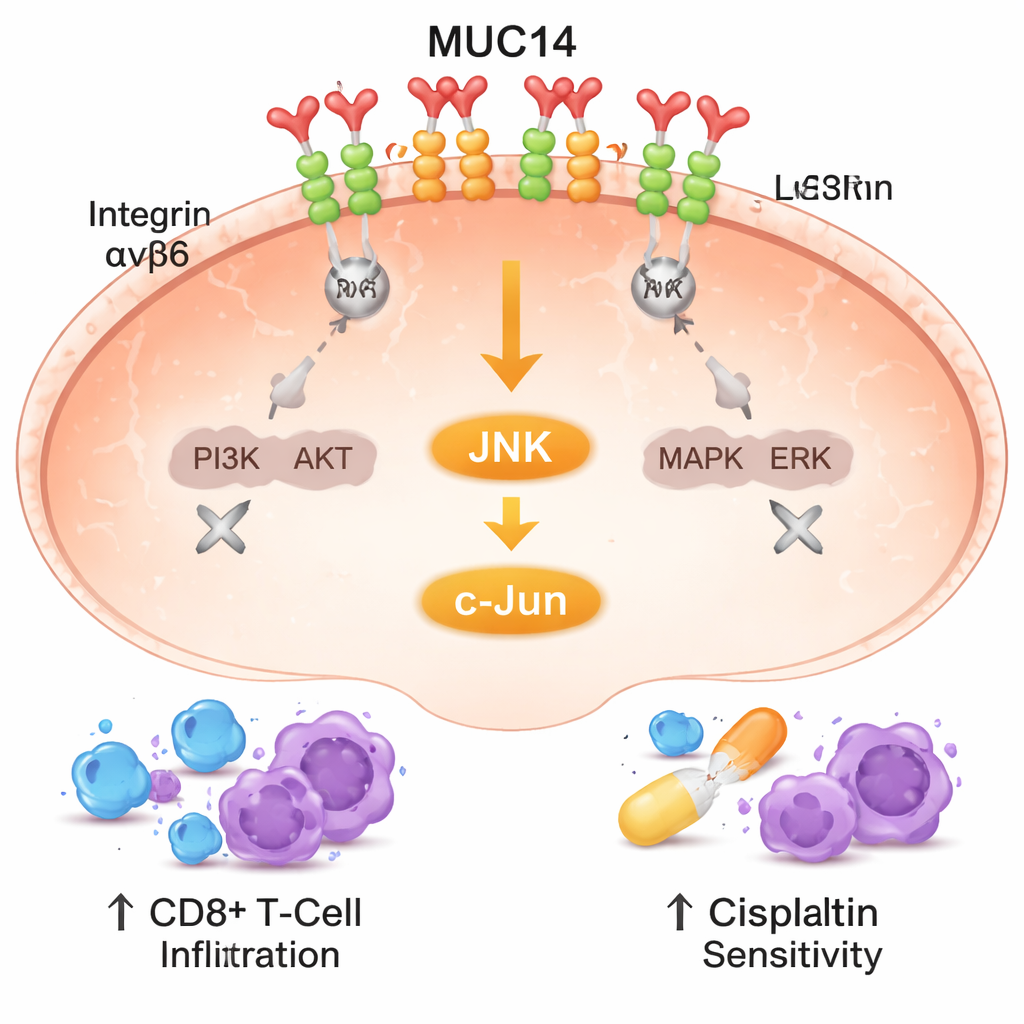
促进免疫与化疗协同作战
癌症结局不仅由肿瘤细胞本身决定,也受周围免疫细胞的影响。通过分析免疫分型数据库并对人体肿瘤切片进行染色,研究团队发现 MUC14 表达较高的肿瘤在 MUC14 阳性肿瘤区域附近聚集了更多 CD3+ 和 CD8+ T 细胞——这些免疫细胞可以直接杀伤癌细胞。这表明 MUC14 有助于营造更利于免疫攻击的肿瘤微环境。研究者还评估了顺铂,这是一线治疗肺腺癌的常用药物。在细胞培养中,过表达 MUC14 的肿瘤对顺铂的抑制所需剂量显著降低,而缺乏 MUC14 的细胞则对药物更具耐受性。重要的是,MUC14 并非简单地使细胞在基线更易凋亡;相反,它放大了顺铂的杀伤效应,部分通过激活由 DNA 损伤触发的应激通路 JNK/c-Jun 来实现。
走向更聪明的肺癌组合治疗
简而言之,这项工作将 MUC14 描绘为对抗肺腺癌的内在防线。其存在可阻断细胞表面的关键生长开关、减缓肿瘤扩散、吸引抗癌 T 细胞,并在动物试验中增强顺铂疗效而不增加器官毒性。MUC14 丧失时,肿瘤变得更强韧、更易转移并对标准疗法反应减弱。研究结果提示,测量 MUC14 可能有助于预测预后与治疗反应,未来设计用于增强 MUC14 活性或模拟其对整合素信号影响的疗法,或可使临床医生更有效地将化疗与免疫疗法结合用于晚期肺癌患者。
引用: Li, X., Li, M., Huang, S. et al. MUC14 suppresses lung adenocarcinoma via integrin α8β6/PI3K/AKT/MAPK modulating cisplatin response and immunity. Sci Rep 16, 7784 (2026). https://doi.org/10.1038/s41598-026-39019-z
关键词: 肺腺癌, MUC14, 顺铂耐药, 整合素信号, 肿瘤免疫