Clear Sky Science · zh
基于结构的建模揭示CYP153A6对甲苯衍生物新活性的分子基础
把难啃的化学活交给自然
化学家和工业界依赖能向顽固的碳–氢键引入氧的反应,例如用于去除污染物或合成药物与香料的前体。要在不使用强烈化学品或重金属废弃物的情况下做到这一点很困难。本研究考察了一种天然催化剂——来自土壤细菌的酶CYP153A6,并提出一个简单但意义重大的问题:是否可以引导该酶选择性地将甲苯类化合物(燃料和溶剂中的常见成分)“升级”为更有用、更环保的产物?
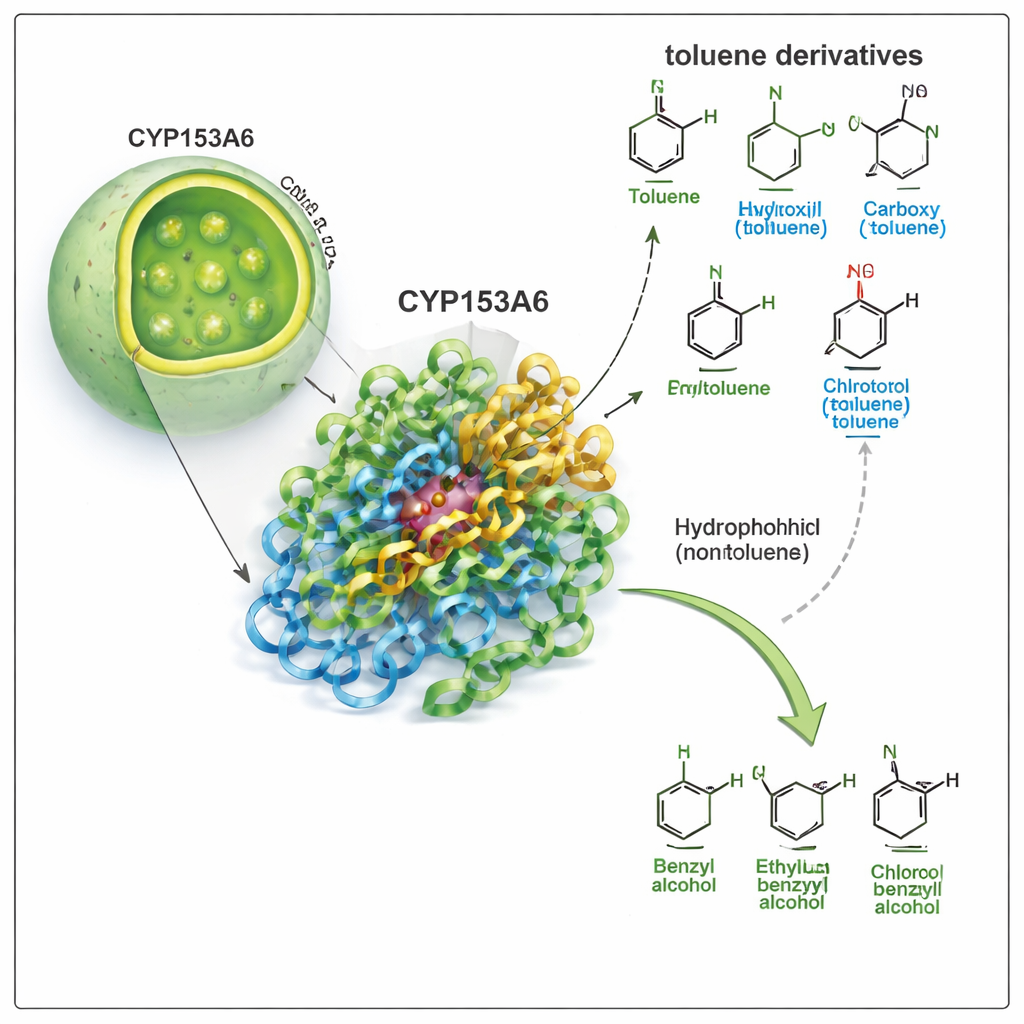
选择单一位点的酶
CYP153A6属于大型的细胞色素P450家族,是自然界中多才多艺的氧化专家。与许多工业催化剂不同,这种酶在水相、适中温度下工作,并且能在分子上选择非常特定的位置。早期工作表明CYP153A6会在简单烃链的末端和某些植物来源的芳香物质上插入氧。本文作者探讨它是否也能攻击甲苯及相关化合物的“苄位”——连接在苯环上的小侧链。该转化能将甲苯衍生物转化为苄醇,苄醇是制药、香料和精细化学品的重要构建模块。
测试酶偏好的分子
研究团队首先使用表达CYP153A6的工程化大肠杆菌细胞进行生物转化实验,包括全细胞和细胞裂解液两种形式。他们用一组甲苯衍生物考察酶的活性,改变连接在芳环上的取代基(如甲基、氯、甲氧基、羟基或硝基)及其位点(对位、间位或邻位)。酶对疏水或仅稍带极性的化合物表现良好,如对位愈创木烯(p-cymene)、对二甲苯(p-xylene)、对甲氧基甲苯(p-methylanisole)和对氯甲苯(p-chlorotoluene),持续将苄位甲基转化为苄醇。显著的是,它完全忽视了更强极性的分子,如对甲酚(p-cresol)、对甲基苄醇(p-methyl benzyl alcohol)和对硝基甲苯(p-nitrotoluene),尽管这些在结构上很相似。这一模式表明酶的口袋高度疏水,不利于带极性基团的底物。
构建分子机器的三维地图
由于CYP153A6的实验三维结构尚未解析,研究者使用已知结构的密切相关P450构建了高质量的计算模型。他们通过检查几何结构并运行长时间的分子动力学模拟来验证该模型,结果显示蛋白质在时间尺度上保持稳定。模拟揭示了一个埋藏的活性位点,通过狭窄的通道与外界相连,底物通过这些通道进入、产物则离开。通道由蛋白表面的柔性环段塑形和门控,这有助于解释酶如何将疏水分子引导至含有反应性血红素铁的中心,同时允许水和氧化产物逸出。
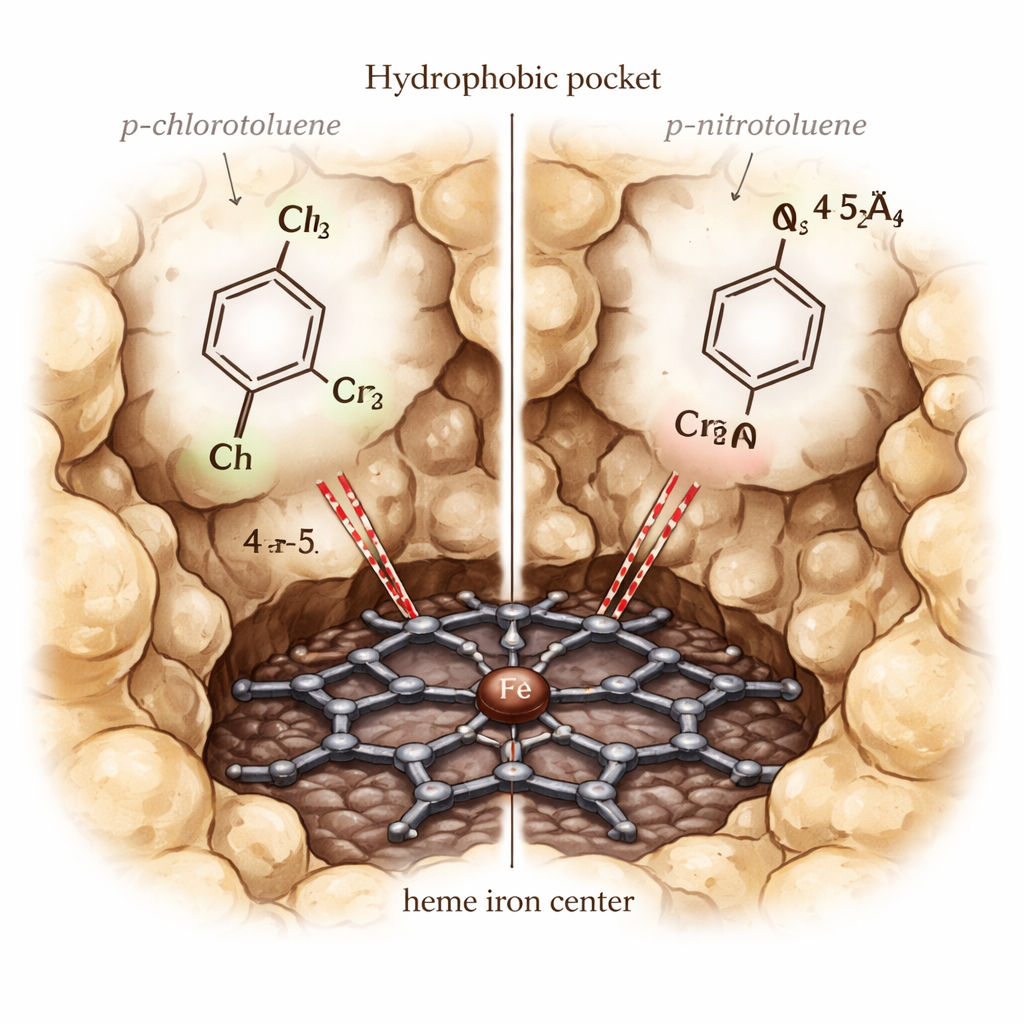
观察分子如何停靠、移动与反应
有了模型后,作者模拟了不同甲苯衍生物在CYP153A6内的结合方式。他们使用了一种称为集合对接(ensemble docking)的方法,尝试许多略有不同的蛋白构象以及几种血红素铁的电子态,以识别哪些设置能最好地区分真实底物与非底物。最佳情景使用了处于休止的铁(ferric)态且口袋内无额外水分子,该情景正确优先考虑了已知的底物。后续模拟逐帧跟踪每个分子相对于血红素的位置。表现良好的底物(如p-cymene和p-xylene)保持靠近铁,苄位甲基指向铁,预测结合能显著有利。表现差的底物则倾向于漂离、采取尴尬的取向,或与衬托口袋的主要油性侧链发生不利相互作用。
为何长得相似的分子反应性却不同
一个难题是:p-氯甲苯能被CYP153A6高效氧化,而p-硝基甲苯不能,尽管两者在模拟中都能进入口袋并显示出类似的结合强度。为了解释这一点,作者对酶的高反应性“化合物I”(Compound I)态进行了更精细的量子力学/分子力学(QM/MM)计算。这些计算显示,硝基强烈抽取苄位碳的电子密度,使其变得难以被氧化,即使几何上足够接近。相比之下,氯基允许血红素与底物之间有更好的电子通讯,表现为芳环和甲基上较高的自旋密度,并且在关键的氢抽取步骤中呈现出更具反应性的排列。
对更清洁化学的意义
通俗来说,CYP153A6像一只微小的油性手套,以恰当的方式抓住某些类燃料分子,使氧能在特定位置被引入——将它们转化为更易溶于水、更有用且更易降解的产物。研究表明,该酶偏好非极性取代基,并且分子形状与电子流动共同决定了某个甲苯衍生物是否会被转化。通过阐明CYP153A6如何识别并激活这些分子,这项工作为工程改良版本奠定了蓝图,未来可用于治理芳香族污染物或以更可持续的方式制造复杂化学品。
引用: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
关键词: 生物催化, 细胞色素P450, 甲苯羟基化, 酶工程, 绿色化学