Clear Sky Science · zh
用于营养和治疗应用的能产生功能性人α-乳白蛋白的叶绿体转基因生物工厂
将植物改造为乳蛋白生产者
现代饮食高度依赖乳蛋白,但以全球规模养牛伴随环境成本和伦理问题。本研究探索了一种完全不同的制造关键人乳蛋白的方法——让植物叶片来生产它。研究表明,烟草植物可以被重新编程以合成人α‑乳白蛋白,这是一种对婴儿营养重要且具有潜在抗癌特性的蛋白,为无动物来源婴儿配方成分和新的抗癌食品成分开辟了道路。
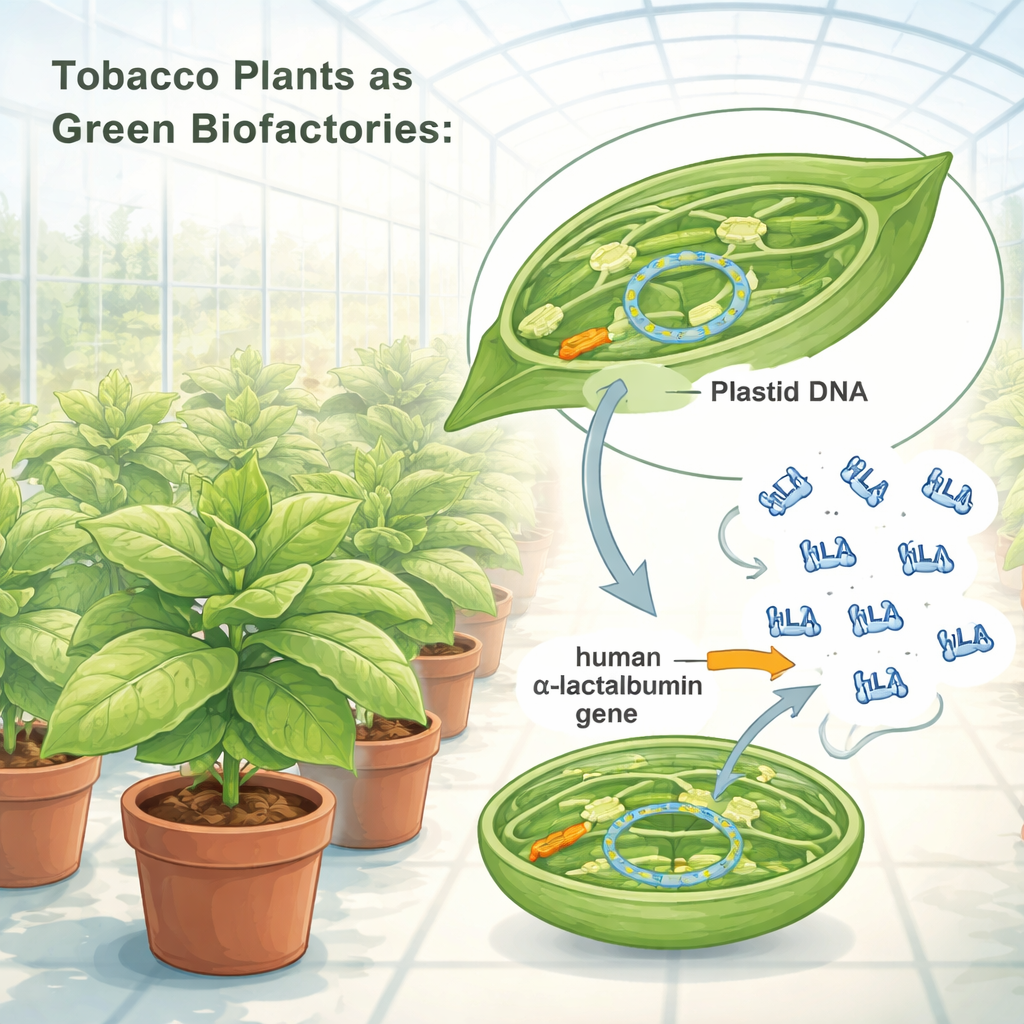
为何这种乳蛋白很重要
人乳不仅是食物;它是针对婴儿需求精细调整的蛋白、脂肪和糖类混合物。其最重要的蛋白之一是α‑乳白蛋白,它有助于合成乳糖——乳中的主要糖,是婴儿的关键能量来源。α‑乳白蛋白富含必需氨基酸,包括色氨酸(大脑“愉悦”化学物质血清素的前体),并与更好的应激耐受性以及对某些癌症的潜在保护相关。由于它易于消化、味道温和且在较宽的酸碱范围内稳定,广泛用于婴儿配方和营养饮品——而且需求正在增长。
传统乳业的问题
依赖奶牛提供乳蛋白存在缺点。畜牧业贡献了相当比例的全球温室气体排放,大型奶业需要大量土地、水和饲料。此外,牧场管理可能引入激素、抗生素和病原体进入乳制品链。这些压力促使人们关注“细胞农业”方法,即由微生物或培养细胞而非动物来生产乳蛋白。然而,许多此类系统仍然成本高昂、难以规模化,或产生的蛋白与人源版本不完全相同。植物,特别是叶片中的叶绿体——驱动光合作用的小型绿色工厂,提供了一个有前景的替代平台。
将叶绿体重新编程为生物工厂
研究人员重塑了人α‑乳白蛋白的遗传指令,使烟草叶绿体能够高效识别并表达。研究团队将经优化的基因插入叶绿体DNA,使用由强效植物调控元件构成的“基因盒”,这些元件相当于强力的开关。通过微粒轰击法,他们将该基因盒传递到烟草叶细胞中,然后筛选出叶绿体完全接受新基因的植株。遗传学检测证实这些植株中所有叶绿体DNA拷贝现均携带该人源蛋白的蓝图。经改造的植株在温室条件下正常生长、结籽且在大小、形态和生育力方面未见明显代价,表明额外的蛋白负荷并未损害植物健康。
证明植物产生的蛋白有效
接着,团队检验植物合成的α‑乳白蛋白是否与天然人源蛋白表现一致。他们从叶片中提取可溶性蛋白,纯化出α‑乳白蛋白,并用能反映蛋白折叠状态的技术检查其结构。植物来源蛋白的光谱“指纹”几乎与商业人源α‑乳白蛋白重叠,表明折叠相似。在功能上,植物制得的蛋白对乳糖合成酶的激活能力接近天然版本,驱动乳糖生成的速率约为标准蛋白的93%。值得注意的是,α‑乳白蛋白在叶片中累计量约占全部可溶性蛋白的23%——这是在植物叶绿体中表达的人源蛋白所报告的较高水平之一,表明该系统可以提供工业相关的产量。
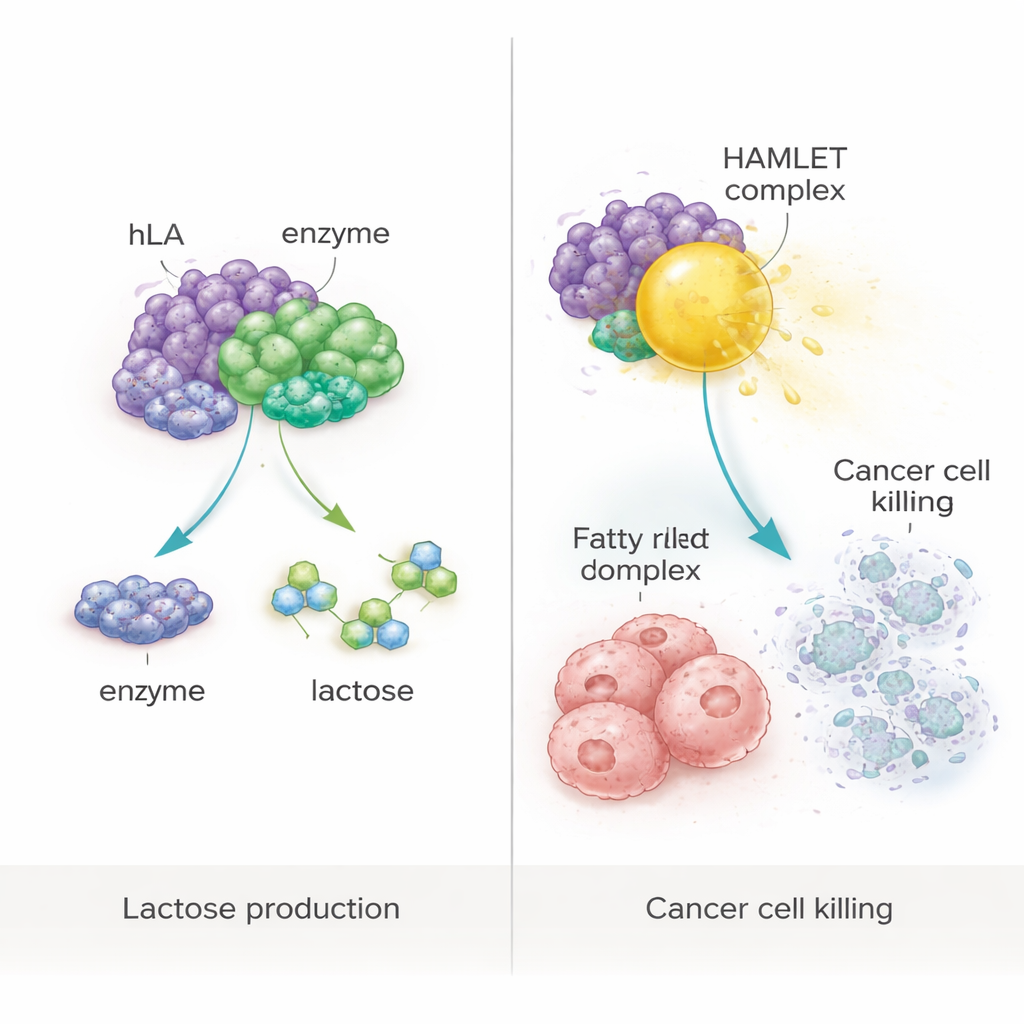
从营养到抗癌复合物
研究还测试了一个更具野心的想法:将植物制得的蛋白作为已知抗癌复合物HAMLET的构建模块,HAMLET在α‑乳白蛋白与油酸(一种常见脂肪酸)紧密结合时形成。通过在可控条件下将纯化的植物蛋白与油酸轻度加热,研究者制备出类似HAMLET的复合物。将这一复合物施用于体外培养的人结直肠癌(WiDr)和乳腺癌(MCF‑7)细胞时,细胞存活率显著下降至10%以下。后续分析显示,大多数受影响细胞处于凋亡状态,这是一种程序性细胞死亡而非失控破裂。重要的是,单独的蛋白、单独的脂肪酸或未改造植物提取物均未引起显著细胞死亡,证实了杀癌效应依赖于该特定复合物。
这对未来食品与药物意味着什么
综合来看,研究表明植物叶绿体可以可靠地大量生产一种既有营养价值又具治疗活性的人人乳蛋白。对非专业读者而言,这意味着未来的婴儿配方、功能性食品或补充剂有可能来自叶片中生长的蛋白而非奶牛,从而在减少环境影响的同时更贴近人类生物学。同时,同样的植物来源蛋白在实验室中可被转化为靶向抗癌复合物,暗示了建立基于植物的廉价生物治疗产品的可能性。尽管仍需更多研究以确认在动物和人类中的安全性与效果,并将该技术转移到可食用作物上,研究为植物作为下一代营养与医药微型工厂提供了引人注目的前景。
引用: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
关键词: 植物制造的乳蛋白, 叶绿体生物工厂, 人源α-乳白蛋白, 可持续乳制品替代品, HAMLET 抗癌疗法