Clear Sky Science · zh
miR-340通过下调MDM2提高p53基因疗法在转移性前列腺癌细胞中的疗效
这项研究对患者的重要性
对于已发生转移且对激素治疗不再敏感的晚期前列腺癌男性,现有疗法能够延缓疾病进展但很少能治愈,约只有一半患者能活过五年。该研究探索了一种通过强化机体自身抗癌防线——p53“守护者”蛋白——来提升现有疗法效果的新思路,工具是称为miR-340的微小遗传因子。
重新唤醒体内的肿瘤守护者
许多癌症,包括侵袭性前列腺肿瘤,会使p53失活。p53通常能阻止受损细胞、修复它们或诱导其自我毁灭。已有针对其他癌种的临床尝试之一是p53基因疗法:将健康的p53基因拷贝送入肿瘤细胞,使其恢复对损伤的应答。但肿瘤常通过增加MDM2的表达来反击,MDM2会标记p53使其被降解。作者推测,如果在补入p53的同时降低MDM2,就有可能在难治性前列腺癌中恢复这一肿瘤防护通路的全部功能。
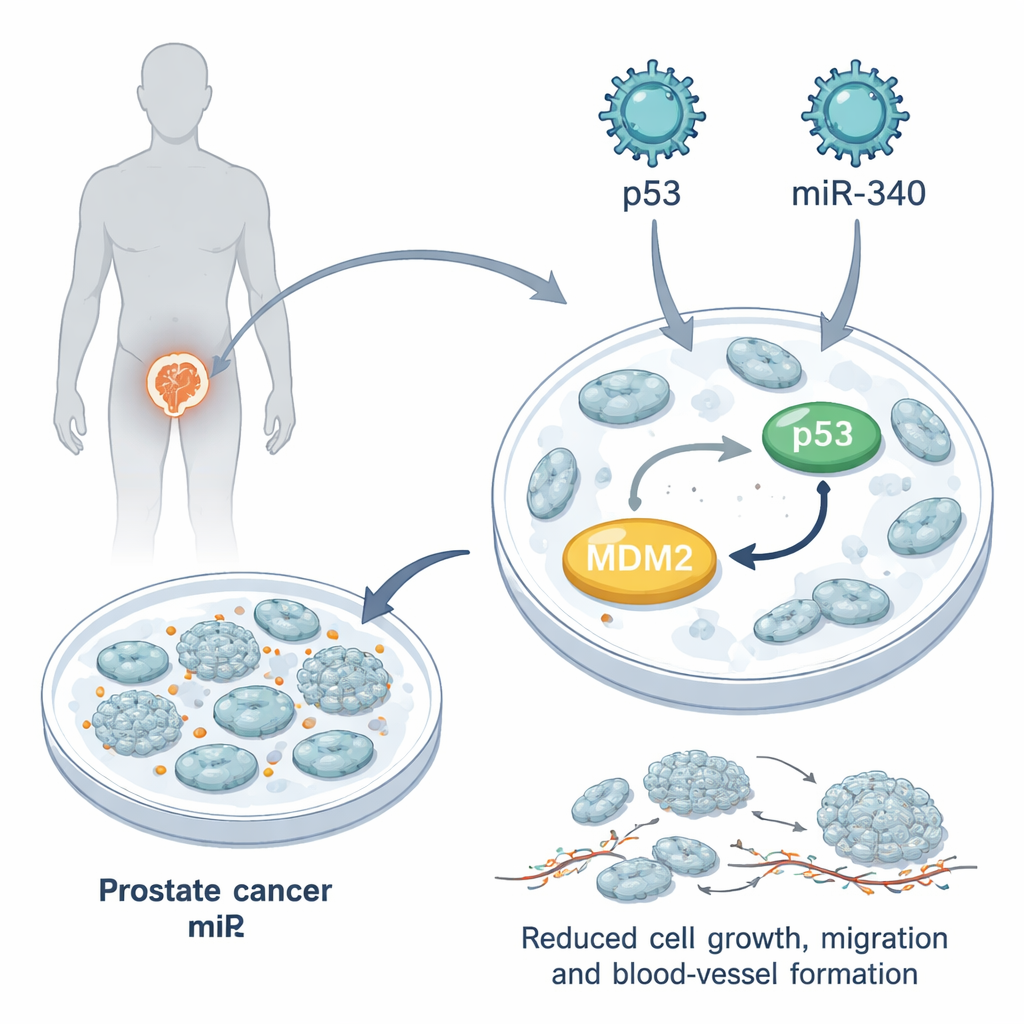
一种小RNA带来大影响
研究团队聚焦miR-340,这是一种天然存在于细胞中的小RNA,参与基因表达的精细调控。数据库分析显示,前列腺肿瘤中的miR-340水平低于健康前列腺组织,在去势抵抗性疾病中甚至更低。先前研究提示miR-340可以结合MDM2的遗传信息并减少其产生。本研究中,研究者使用工程化慢病毒载体向完全缺失功能性p53的常用实验模型PC3前列腺癌细胞中导入额外的miR-340、额外的p53或两者同时导入。他们证实miR-340可强烈降低MDM2,且miR-340与p53共同作用时,p53关键下游伙伴p21的水平显著升高,p21在阻止细胞分裂方面至关重要。
减缓癌细胞生长与扩散
在改造后,研究者检测了这些前列腺癌细胞的增殖速度、迁移能力以及支持血管生成的能力——这些都是侵袭性肿瘤的特征。单独的p53能减慢细胞生长并使更多细胞停滞在细胞周期的静止G0/G1期。单独的miR-340对生长影响不大,但与p53联用时极大地放大了这种减缓:细胞倍增时间延长,形成的三维类肿瘤球体更小且更脆弱。在模拟肿瘤细胞迁移的划痕“愈合”实验中,单独的miR-340对细胞迁移几乎没有影响,但能增强p53阻止细胞进入缺口的能力。联合治疗还降低了促血管生成的信号,来自处理后前列腺癌细胞的培养液使血管细胞的增殖和迁移减少。
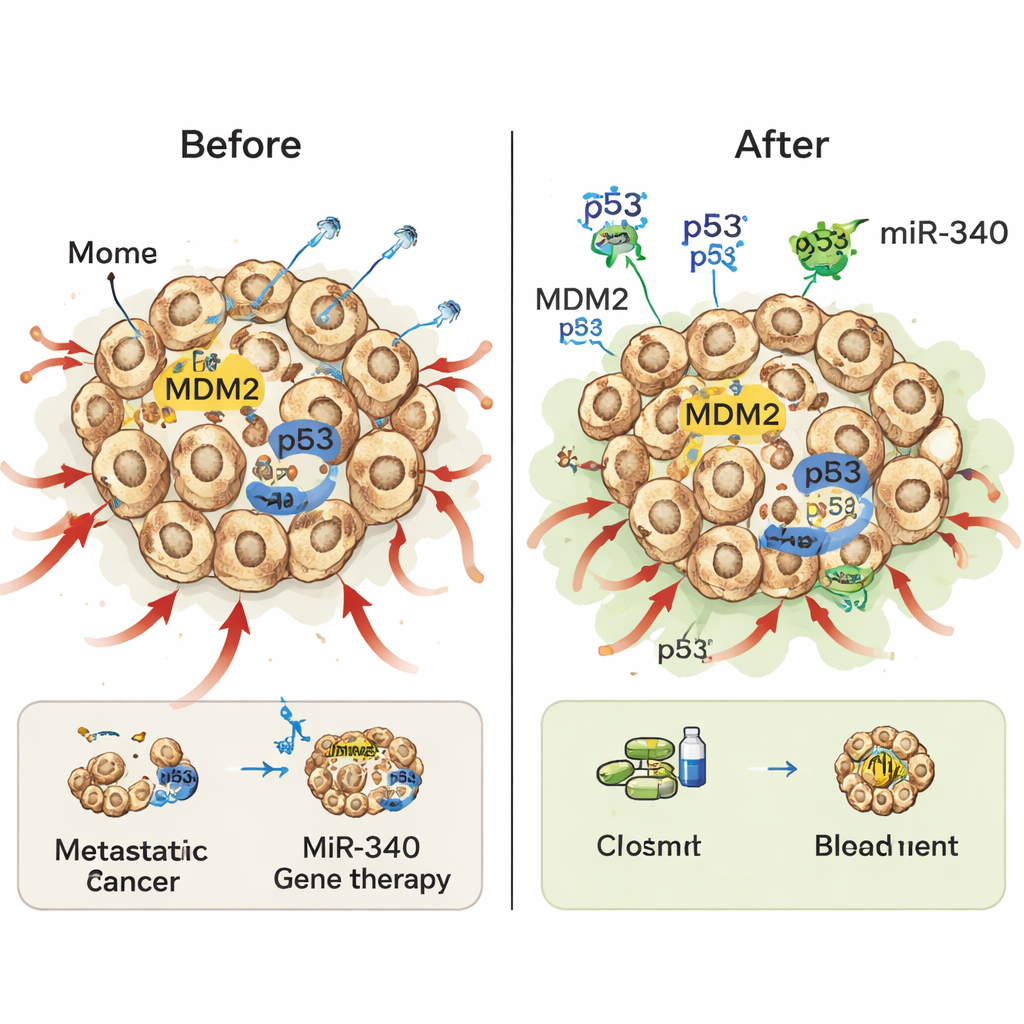
让化疗和放疗更具杀伤力
一个引人注目的发现是,miR-340/p53联合基因疗法在自身毒性不强的情况下,使标准疗法的效果更强。当被改造的前列腺癌细胞暴露于低剂量化疗药物多西他赛时,同时携带miR-340和p53的细胞比仅给p53或仅给miR-340的细胞显示出明显更高的程序性细胞死亡。同样的模式也出现在X射线照射下:单独miR-340作用甚微,但与p53联用能显著增加癌细胞的敏感性,照射后其形成克隆的能力大幅下降。在这两种情况下,miR-340似乎通过降低MDM2来发挥作用,使补入的p53得以积累,并在化疗或放疗对癌细胞造成损伤后充分激活其诱导细胞死亡的程序。
这对未来治疗的可能意义
作者总结称,在p53基因疗法中加入miR-340可以显著强化该方法对转移性、耐治疗前列腺癌的作用——尤其是在与现有化疗和放疗联合使用时。尽管本项工作是在体外细胞实验中完成,仍面临诸如改进基因递送方法并在动物和人体中确认安全性等实际挑战,但它勾画出一条明确且可检验的策略:通过降低MDM2来削弱肿瘤对p53的制动,然后让标准疗法触发更强、更有针对性的反应。如果未来研究证实该策略有效,患者有望在使用更低剂量有毒药物的同时实现更强的肿瘤控制。
引用: Deyhimfar, R., Kehtari, M., Saadatpour, F. et al. miR-340 improves the efficiency of p53 gene therapy in metastatic prostate cancer cells through downregulation of MDM2. Sci Rep 16, 7527 (2026). https://doi.org/10.1038/s41598-026-38963-0
关键词: 前列腺癌, 基因疗法, p53, MDM2, 微小RNA-340