Clear Sky Science · zh
A2-泛皮钙蛋白与Bcl-xL和WAVE1相互作用,促进线粒体-内质网接触位点(MERCs)并加剧线粒体钙升高以介导中风中的细胞死亡
为何新生儿大脑中的微小连接至关重要
中风常被视为成年人的疾病,但当它发生在新生儿时,可能在不显眼中损害发育中的大脑并导致终生问题。本研究深入探究在这一危机中神经细胞内部发生的变化。作者聚焦于一种鲜为人知的蛋白家族——泛皮钙蛋白(pancortins),并展示了两种发育期形式如何像危险的“助推器”一样,收紧关键细胞结构间的连接,诱发钙洪流,推动幼年神经元走向死亡。
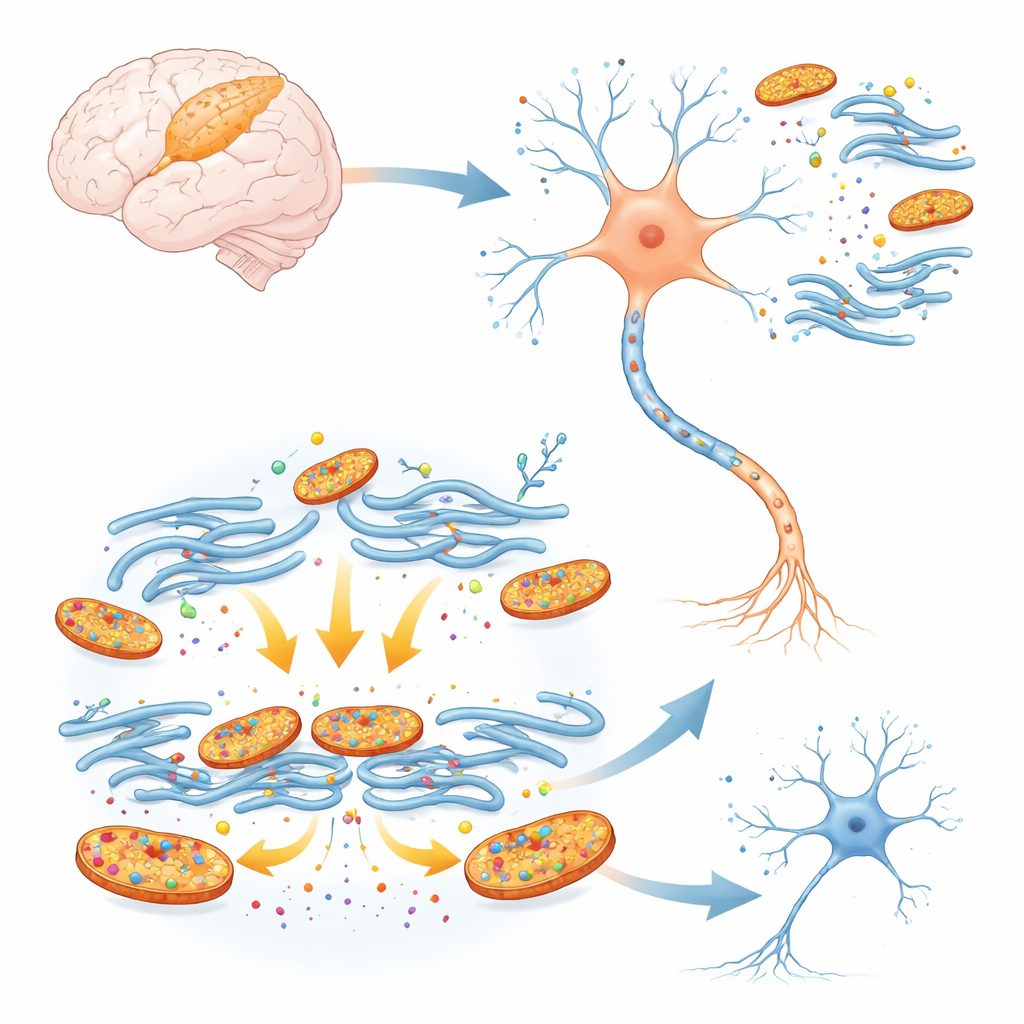
新生大脑中的隐匿罪魁
泛皮钙蛋白类似支架,参与塑造发育中的大脑。两种称为A2-泛皮钙蛋白的形式在早期发育期间丰富,随着大脑成熟则大幅减少。由于新生大脑对缺氧特别敏感,研究者探究这些早期表达的蛋白是否会在大脑皮层短暂缺血时(如新生儿中风)加剧损伤。在培养的鼠类皮层神经元中,他们使用遗传学工具降低所有泛皮钙蛋白的水平,然后让细胞经历模拟中风的缺氧缺糖。泛皮钙蛋白被下调的神经元存活率显著更高,表明这些蛋白并非保护幼年细胞,反而在应激下促使其受损。
从小鼠中风模型到受保护的脑组织
为验证这种有害作用是否在完整大脑中也存在,团队构建了专门缺失发育期A2-泛皮钙蛋白的小鼠。两周大的幼鼠敲除鼠及其正常同窝对照接受了一种阻断大脑主要动脉的处理,这是缺血性中风的标准模型。一天后,两组在深层脑区都出现损伤,但缺失A2-泛皮钙蛋白小鼠的皮层受损约为正常动物的一半。值得注意的是,这种保护效应在五周龄小鼠(成体泛皮钙蛋白变体占主导时)消失。上述依赖年龄的结果将A2-泛皮钙蛋白指认为新生儿皮层中重要的促死因子,将一个发育程序与中风易感性联系起来。
神经元内部的危险接触区
在细胞内部,能量生产的线粒体靠近储存钙的内质网(ER)。当两层膜接近接触时,所谓的线粒体–内质网接触位点充当微观通道,使钙得以通行。适度的钙转移支持能量代谢,但过量会使线粒体超载并触发细胞死亡。研究者发现A2-泛皮钙蛋白与两个伙伴——Bcl-xL和WAVE1——一起组装成一个三元复合体,定位于这些接触位点。当他们促使细胞过度表达A2-泛皮钙蛋白及其伙伴时,通过一种专门的分裂荧光传感器观测到线粒体与内质网的接触更频繁且更紧密。一个名为GRP75的牵连蛋白加入该复合体,帮助稳定这些接触区。
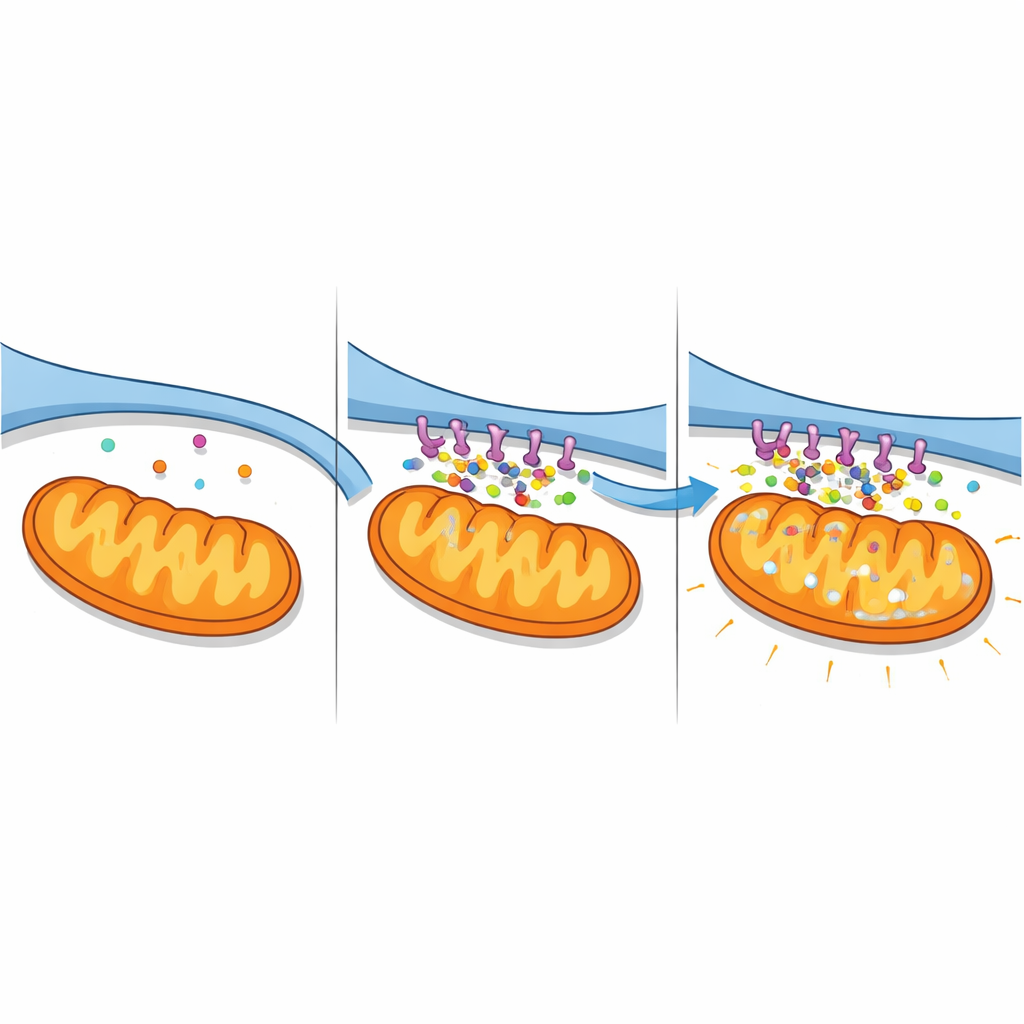
钙洪流与失灵的能量工厂
这种加强的接触对钙平衡产生了严重后果。作者使用分别报告细胞质、内质网和线粒体中钙的荧光指示剂,实时观察钙水平变化。表达A2-泛皮钙蛋白复合体的细胞显示线粒体内及细胞周围液体中的钙稳步上升,同时内质网储钙下降,这表明大量从内质网转移到线粒体。阻断内质网上的关键钙释放通道(IP3R)在很大程度上阻止了这些变化,证实该复合体放大了特定的内质网到线粒体的通路。在暴露于类中风的缺氧缺糖条件下,敲低泛皮钙蛋白的神经样细胞则表现相反:钙超载被减弱,内质网储钙更好地保留。综上,这些发现将A2-泛皮钙蛋白描绘为组织钙“高速通道”的构建者,在缺血应激下该通道变得致命。
对保护新生儿大脑的意义
对非专业读者来说,核心结论是这项工作识别出一个新的分子开关,决定年轻神经元在中风后是生存还是死亡。通过收紧储钙膜与细胞能量工厂之间的显微连接,A2-泛皮钙蛋白使线粒体因过量钙而窒息并功能衰竭。在幼鼠中去除这些蛋白减轻了实验性中风的影响,这提示未来可通过药物或基因疗法干扰A2-泛皮钙蛋白复合体——或放松其巩固的接触位点——来降低受影响新生儿的脑损伤。尽管此类治疗尚属前景,但该研究绘制了一条从发育蛋白到钙超载与神经元丧失在新生儿中风中的清晰且可检验的通路。
引用: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
关键词: 新生儿中风, 线粒体-内质网接触位点, 钙超载, 泛皮钙蛋白家族, 神经元细胞死亡