Clear Sky Science · zh
一种新的 C/EBPα–miR-335-5p–PRKAA2 调控轴驱动 MASLD 中的肝脂质堆积
为什么脂肪肝病重要
许多几乎不饮酒的人仍然会出现“脂肪肝”,这种状况现在称为代谢功能障碍相关脂肪肝病(MASLD)。它与肥胖和2型糖尿病密切相关,且可能在不知不觉中进展为肝纤维化、肝硬化,甚至肝癌。本研究提出了一个看似简单但至关重要的问题:肝细胞内部发生了什么,促使它们储存大量脂肪?我们能否找到一个可被关闭以保护肝脏的分子开关?
肝细胞中的一个隐藏连锁反应
研究人员聚焦于将饮食与代谢连接到肝脏脂肪积累的分子连锁反应。他们研究了喂以高脂饮食的小鼠以及用脂肪酸处理的培养肝细胞以模拟 MASLD。在这些模型中,动物体重增加、血脂升高、肝脏充满油滴,重现了人类脂肪肝的关键特征。在这些脂肪肝中,团队注意到一个特定的基因调控因子——转录因子 C/EBPα 和一种小 RNA 分子 miR‑335‑5p 水平都上调,而一个保护性酶亚基 PRKAA2(属于众所周知的能量感应器 AMPK)则被下调。
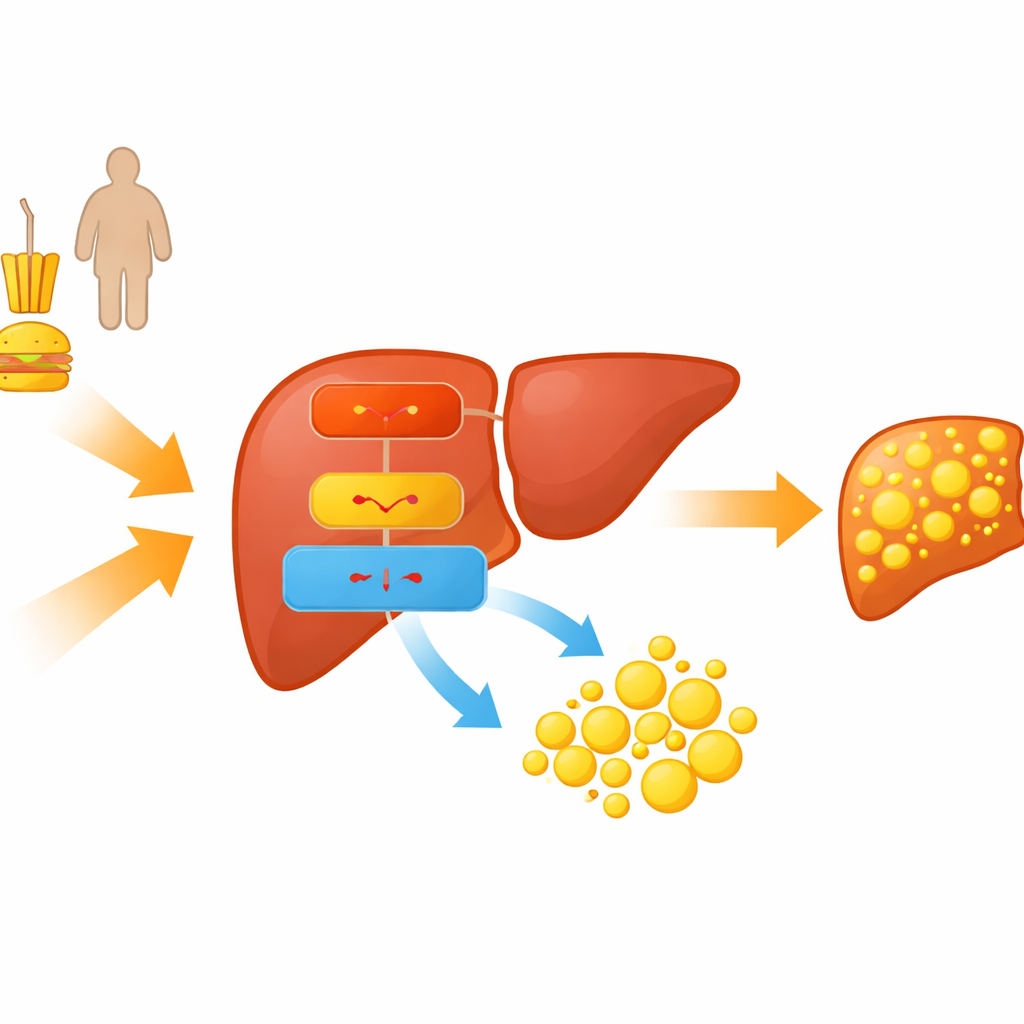
小 RNA 如何将平衡倾向于脂肪
被称为微小 RNA(microRNA)的小分子 RNA 像分子调光器一样,调低特定基因的表达。研究团队证明 miR‑335‑5p 直接结合编码 PRKAA2 的信使 RNA,阻止细胞合成该蛋白。PRKAA2 有助于组装 AMPK 复合体,AMPK 通常在能量不足时被激活,通过抑制脂肪合成并促进脂肪分解来响应。当在肝细胞中人为提高 miR‑335‑5p 水平时,PRKAA2 水平下降,AMPK 活性降低,促进脂肪合成的蛋白上升,导致可见的脂滴堆积。阻断 miR‑335‑5p 则出现相反效果:PRKAA2 与 AMPK 活性上升,脂质积累减少。
启动该级联反应的主开关
那么最初是什么启动了 miR‑335‑5p?通过扫描控制该 microRNA 的 DNA 序列,科学家预测了几个可能的主开关并将注意力集中在已知影响脂肪和糖代谢的 C/EBPα 上。他们证实 C/EBPα 直接结合 miR‑335‑5p 的调控区并增强其活性。在肝细胞中增加 C/EBPα 会提高 miR‑335‑5p 水平、降低 PRKAA2、削弱 AMPK 信号并促进脂肪积累。沉默 C/EBPα 则产生相反效应,加强细胞的能量感应制动并减少脂质。拯救性实验中,阻断 miR‑335‑5p 或恢复 PRKAA2 显示出 C/EBPα 促进脂肪的效应在很大程度上是通过这条单一链传导的。
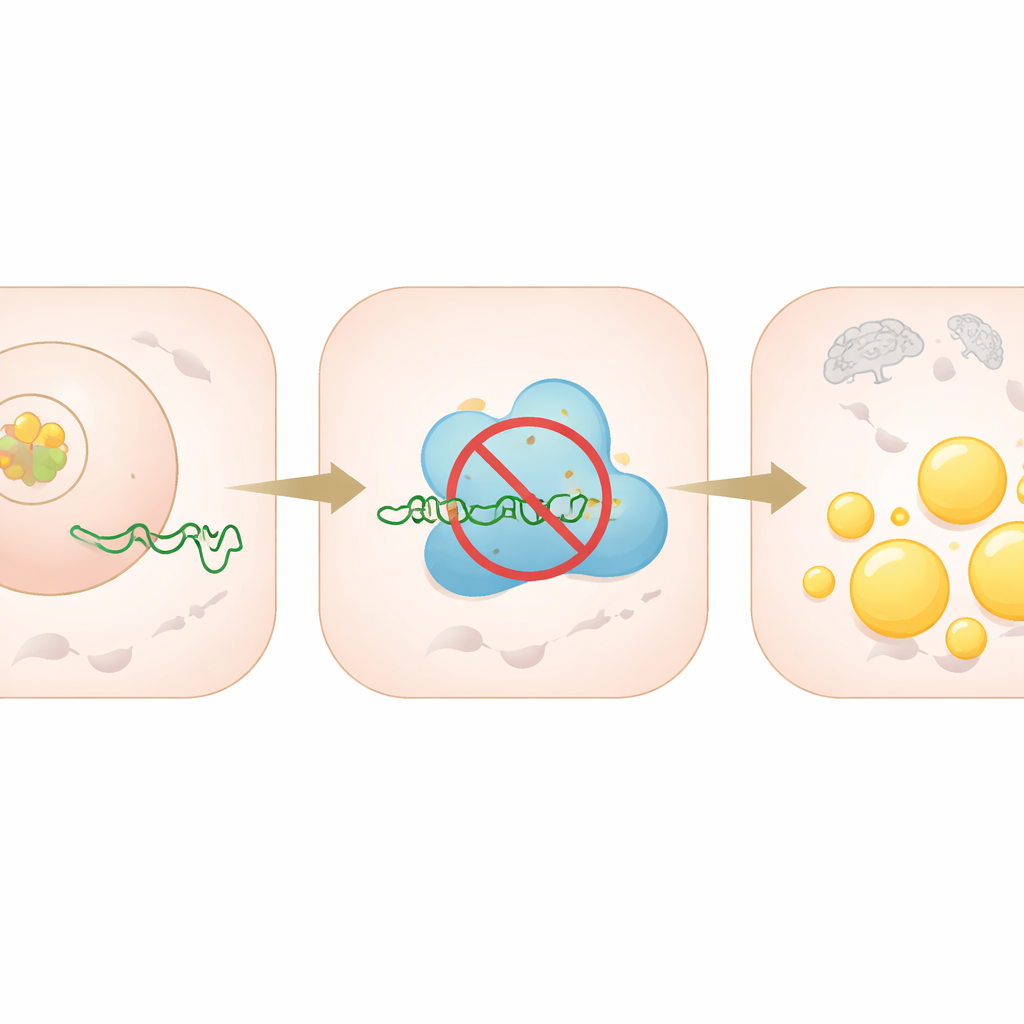
从细胞培养到活体小鼠
为检验该通路在活体动物中是否重要,研究人员使用工程病毒将遗传工具直接输送到高脂喂养小鼠的肝脏中。一种工具降低了 C/EBPα 水平;另一种则清除过量的 miR‑335‑5p。在两种情况下,动物的肝脏脂肪含量减少,显微形态改善,PRKAA2 与 AMPK 活性回升,而驱动脂肪合成的蛋白下降。这些体内结果与细胞培养发现一致,强调 C/EBPα–miR‑335‑5p–PRKAA2 链条不仅是实验室现象,而是在活体中驱动脂肪肝的强力机制。
这对未来治疗意味着什么
简而言之,本研究揭示了一个三步分子接力,使肝细胞囤积脂肪:C/EBPα 激活 miR‑335‑5p,后者关闭 PRKAA2 并削弱细胞的能量刹车 AMPK。刹车被关闭后,脂肪合成机制不受抑制,肝脏被脂质充盈。中断该接力的任一环——抑制 C/EBPα、阻断 miR‑335‑5p 或增强 PRKAA2/AMPK——都能减少小鼠肝脏中的脂肪。尽管在这些策略能否安全用于人体之前仍需大量工作,但该通路为未来旨在减缓或逆转 MASLD 的药物提供了明确且可检验的靶点。
引用: Zeng, X., Xu, Y., You, S. et al. A novel C/EBPα–miR-335-5p–PRKAA2 regulatory axis drives hepatic lipid accumulation in MASLD. Sci Rep 16, 9255 (2026). https://doi.org/10.1038/s41598-026-38918-5
关键词: 脂肪肝病, 微小RNA, AMPK, 脂质代谢, 代谢性疾病