Clear Sky Science · zh
接受心脏移植患者术前术后感染组与非感染组的肠道微生物群及代谢通路特征
移植新心后为何肠道很重要
心脏移植能为严重心力衰竭患者带来第二次生命机会,但术后数周内的感染仍然是主要威胁。本研究提出了一个看似简单却意义深远的问题:围绕心脏移植,居住在肠道内的微生物群——肠道微生物群——如何变化,这些变化是否能解释哪些患者会发生感染、哪些不会?
移植患者体内的微小生态系
我们的肠道寄居着数万亿细菌,它们帮助消化食物、教育免疫系统并抵御入侵病原。手术、强效免疫抑制剂和广谱抗生素都可能冲击这一脆弱生态。为追踪心脏移植患者的变化,中国的研究团队随访了20例接受供体心脏的成人患者。他们在术前约一周和术后30天采集粪便样本,随后使用DNA测序来记录哪些细菌存在,并用计算工具预测这些微生物在代谢上可能的功能。
四组患者,四种微生物格局
研究团队将患者分为四组:术前有感染和无感染者,以及术后一个月内有感染和无感染者。移植前,无论患者是否已有感染,肠道微生物的总体多样性和结构看起来出人意料地相似。术前无感染者多被一种名为拟杆菌属(Bacteroides)的常见属所定植,该属常与肠道稳态相关。相比之下,有感染的患者显示出一种混合群落,既有潜在有害的糠粪肠球菌(Enterococcus casseliflavus),也存在如拟乳杆菌属(Limosilactobacillus)和细小魏斯菌(Weissella cibaria)等通常被认为是有益的细菌,提示肠道群落处于微妙且易变的平衡中。
术后:微生物命运的分岔
术后30天时,未发生感染的患者的微生物群呈现一种可识别的模式,而出现感染的患者则表现出截然不同的格局。未感染患者拥有更丰富、更均衡的微生物群落,许多成员属于布劳氏菌属(Blautia)及相关的产丁酸细菌,这类短链脂肪酸可为肠上皮细胞提供能量并支持免疫稳态。他们的肠道生态显得多样且平衡。然而发生感染的患者,群落多样性下降,群落被通常在院内获得性感染中出现且具有抗药性的粪肠球菌(Enterococcus faecium)所主导。统计分析显示,这些感染组的肠道微生物与其他组明显分离,指向术后微生物扰动或菌群失调的清晰迹象。
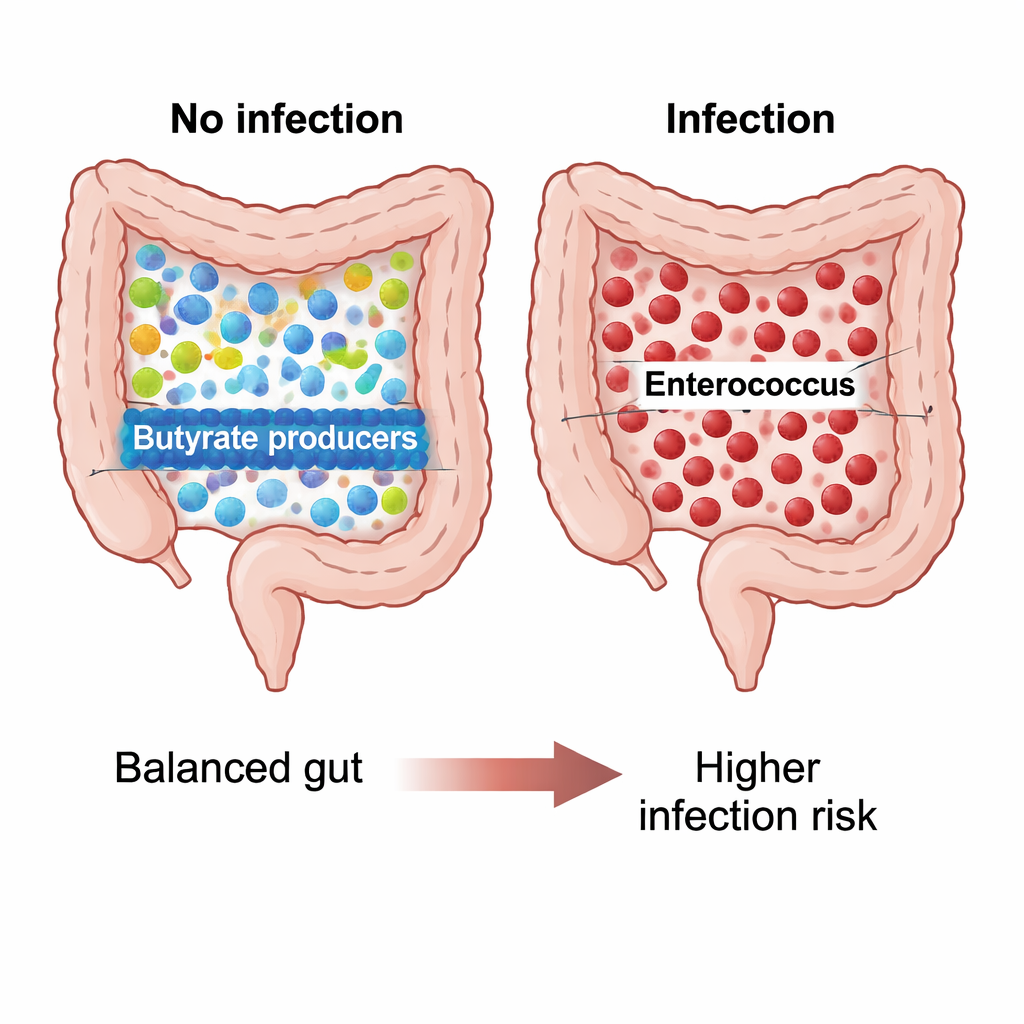
微生物代谢学与保护或风险的关联
研究者还探讨了这些微生物可能承担的化学功能。通过预测性软件,他们发现术后未感染组中,布劳氏菌属与分解一种称为L-1,2-丙二醇的化合物的通路相关——该物质是纤维发酵的中间产物,最终可促进有益脂肪酸如丙酸的生成。而在感染患者中,这种预测到的代谢潜力明显较低,符合肠道群落较少产生保护性分子的情况。术前,有感染患者中的糠粪肠球菌与一些不寻常的发酵途径相关,这可能反映出一个受压、能量需求增加的微生物环境,但这仍需通过实验室直接验证。
对患者与医疗团队的意义
对面临心脏移植的人而言,这些发现表明肠道并非旁观者;它可能影响危险感染的风险。研究显示术前从拟杆菌优势出发,术后可能朝两条不同路径发展:一是布劳氏菌等保护性菌群的富集,二是肠球菌的有害过度增殖,取决于早期恢复期间的具体情况。严重的感染应激与抗生素使用似乎会将肠道群落推向以肠球菌为主、低多样性的状态。作者提出一种“双重目标”策略:一方面支持产丁酸细菌的恢复——可能通过饮食或经过筛选的益生菌;另一方面密切监测肠球菌水平。尽管需要更大规模和更长期的研究,但这项工作为未来将调节肠道微生物群作为常规手段以保护移植患者免受危及生命感染的方向打开了大门。
引用: Han, J., Hua, L., Yang, B. et al. Gut microbiota and metabolic pathway profiles in infected and non-infected heart transplant patients before and after surgery. Sci Rep 16, 7697 (2026). https://doi.org/10.1038/s41598-026-38911-y
关键词: 心脏移植, 肠道微生物群, 术后感染, 抗生素, 产丁酸细菌