Clear Sky Science · zh
构象动力学与结合自由能分析揭示出针对登革热病毒NS5聚合酶的稳定黄酮类抑制剂
为什么这种蚊媒病毒需要植物的帮助
近年来,登革热在全球范围内迅速蔓延,使数百万人患病并造成数千人死亡。然而,我们仍缺乏一种广泛有效且价格可承受的抗病毒口服药物来治疗感染者。本研究提出了一个看似简单但意义重大的问题:天然存在的植物化合物能否被改造为精确的分子“扳手”,去卡住登革热病毒最重要的分子机器之一?
科学家们试图关闭的病毒引擎
登革热病毒通过在我们细胞内复制其遗传物质而存活。为此,它依赖于一种关键蛋白NS5,NS5像一个微小的复制引擎一样负责病毒RNA的复制。如果NS5停止工作,病毒就无法制造新的基因组,感染将陷入停滞。因此,药物开发者把NS5——尤其是其负责RNA复制的区域(即RNA依赖的RNA聚合酶)——视为新药物的主要靶点。已有若干合成化合物和植物提取物表明NS5可以被阻断,但这些早期候选物中许多要么结合力弱、要么不稳定、要么在安全性和体内转运方面存在顾虑。
在植物中寻找有希望的化学“针”
研究者将注意力集中在黄酮类化合物上,黄酮是一大类存在于浆果、茶叶和草本植物等食物中的植物成分,长期以来以其抗病毒和抗炎作用闻名。从一个精心整理的植物次级代谢物数据库中,他们挑选出326种黄酮并为病毒NS5酶与每种候选分子建立三维模型。通过分步骤的计算对接,他们提出问题:哪些分子形状最适合进入NS5上的一个特定“后门”区域——称为N位点的别构位点?该位点一旦被占据可以关闭酶活性,且相较于主活性位点更少发生突变。
在这每一步的虚拟筛选中,结合性差或看起来不太可能具备药物性状的化合物被剔除。剩下的分子不仅按几何契合度打分,还根据估算的结合强度进行评估,使用了一种在水性、类细胞条件下近似化合物与NS5结合时能量的方法。该过程将候选范围缩小到少数顶级黄酮,其中一位代号为PSCdb01560的候选物以其特别强的预测结合能脱颖而出。
在虚拟显微镜下观察分子运动
在静态快照中契合并不足够;有用的药物还必须在一切抖动时保持就位。为此,团队运行了长时程、详细的分子动力学模拟——相当于半微秒的计算电影——用于NS5与最佳黄酮以及一个已知参考抑制剂的配对。他们追踪了蛋白质和每个化合物的晃动程度、复合体的紧密程度、暴露于周围水分子的程度,以及关键化学接触形成和断裂的频率。PSCdb01560表现出异常稳定的行为:它牢牢嵌入N位点,与竞争分子相比几乎不移动,并且似乎使NS5的总体构象更稳定而非扰动它。
相比之下,另外两种最初看起来有希望的黄酮在口袋内开始漂移或随着时间推进变得更暴露于溶剂——这是结合较弱、依赖性较差的迹象。当研究者绘制每个复合体的“自由能景观”——一种可视化热力学上更有利构象的方法——发现PSCdb01560占据了一个深而清晰的能量谷,而不太稳定的化合物则在几个较浅的能槽间跳动。当他们将最低能量的快照与最初的对接构象比较时,PSCdb01560的位置几乎没有改变,进一步强调了其构象上的忠诚性。
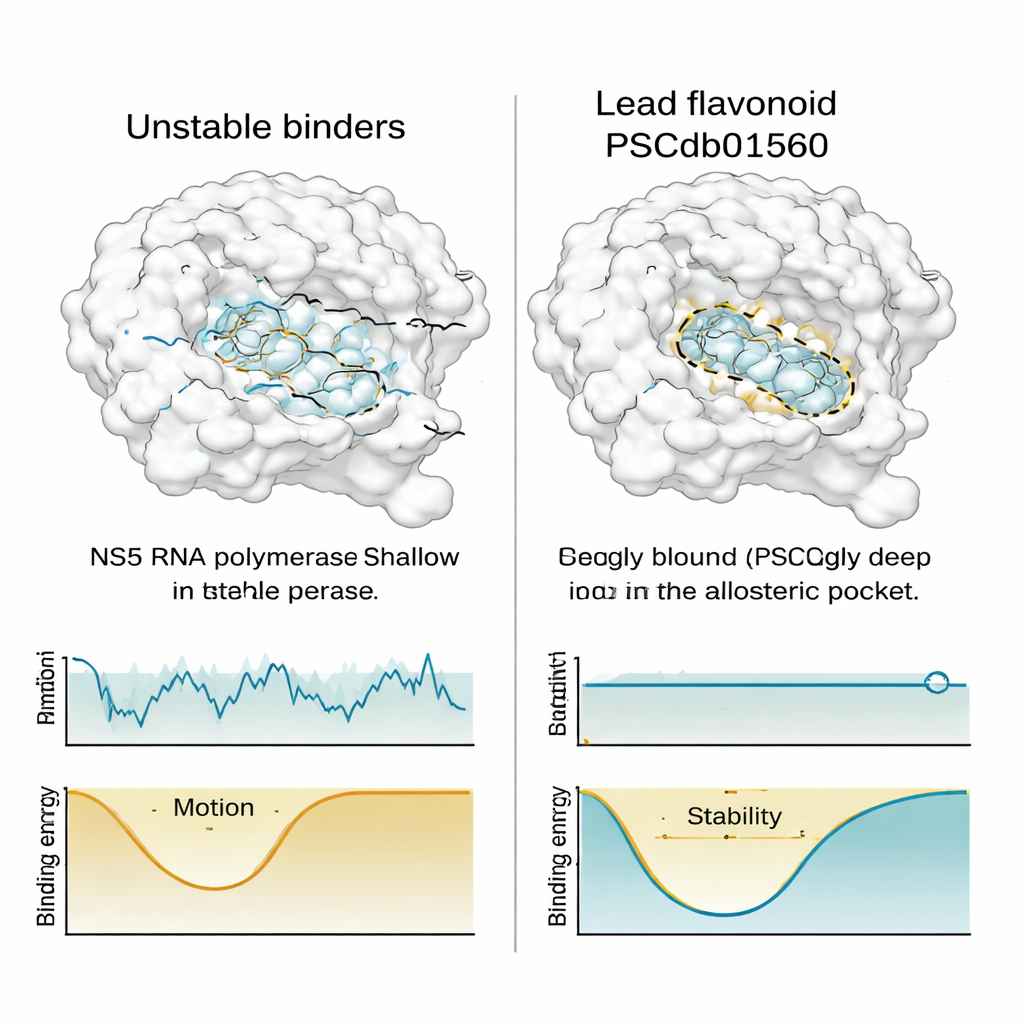
暗示具药物级别潜力的数据
最后,团队使用一种能量计算框架来估算在考虑所有模拟运动后每种黄酮的结合强度。PSCdb01560获得的结合自由能比已建立的参考化合物更有利,这主要归因于形状互补的紧密配合、吸引性的电性相互作用以及位点内部的疏水接触。这一模式——强的计算亲和力、随时间保持稳定的位置、内部柔性受限,以及与不同登革热毒株共享的关键NS5残基发生接触——使PSCdb01560成为一个特别有吸引力的药物设计起点。
这对未来登革热治疗意味着什么
这些结果尚不足以直接交付一种登革热药丸,但它们大大缩小了搜索范围。该研究识别出一种来源于植物的黄酮骨架,在计算机模拟中在稳定性和预测结合强度方面优于数个竞争者乃至已知的基准抑制剂。下一步是实验验证:测试PSCdb01560是否确实能在试管中抑制NS5、阻止感染细胞中的登革热复制,并在动物模型中证明安全性。如果这些关卡被突破,化学家可以将这种黄酮进一步优化为临床可用的抗病毒药物。目前,该研究传达了一个令人振奋的信息:自然的化学库仍然蕴藏着有希望的工具,可用于解除这一全球增长最快的蚊媒威胁之一的武装。
引用: Alsaady, I.M., Gattan, H.S., Aljahdali, S.M. et al. Conformational dynamics and binding free energy analyses unveil a stable flavonoid inhibitor of dengue virus NS5 polymerase. Sci Rep 16, 7761 (2026). https://doi.org/10.1038/s41598-026-38864-2
关键词: 登革热病毒, NS5聚合酶, 黄酮类抑制剂, 抗病毒药物发现, 分子对接