Clear Sky Science · zh
镉通过激活ROS–TCA通路在小鼠精母细胞中诱导铁死亡
为什么一种常见金属关系到男性健康
镉是一种用于电池、颜料和其他工业产品的软金属。它会在土壤、水体和食物中累积,随着时间悄然进入我们体内。大量研究将镉暴露与男性精子数量下降和精子质量变差联系起来,但它伤害产生精子的细胞的确切机制仍不清楚。本研究聚焦于这一问题,揭示镉如何把小鼠精子形成细胞推向一种与铁和线粒体能量系统应激相关的特定细胞死亡途径。
从污染到脆弱的精子细胞
镉是男性生殖系统的众所周知的环境祸害。职业暴露或生活在污染地区的男性常表现为精子数量、活动力和形态正常率下降,甚至精子DNA损伤。动物研究也有类似发现,表现为睾丸萎缩、屏障渗漏、睾酮降低以及生殖细胞大量丧失。作者之前观察到镉可在睾丸组织中诱发一种不寻常的、依赖铁的细胞死亡形式——铁死亡。在本研究中,他们聚焦于正处于生成过程中间阶段的小鼠精母细胞,研究镉如何具体损伤这些细胞,以及这种与铁相关的死亡途径是否参与其中。
铁过载与一种特殊的细胞死亡
为探明机制,研究团队在培养皿中培养小鼠精母细胞系,并用镉处理,部分样本同时加入已知可阻断铁死亡的药物。镉使细胞存活率约减半并减缓细胞分裂。细胞内游离铁水平与一种脂质损伤标志物——丙二醛显著上升,而关键保护酶GPX4下降。参与铁储存与外排的其他蛋白表达增加,表明铁稳态严重受扰。当研究者加入铁螯合剂和保护脂质的分子等铁死亡抑制剂时,许多有害变化得到缓解,细胞存活也有所改善。总体来看,这些变化符合铁死亡的特征,表明镉并非以模糊的方式杀死细胞,而是通过驱动其进入这一特定的铁与脂质驱动的死亡程序。
线粒体遭受围攻
当科学家把注意力转向线粒体——既是能量中心又会产生作为副产物的活性氧(ROS)——故事进一步展开。在显微镜下,健康的精母细胞呈现长而丝状的线粒体,而暴露于镉的细胞则显示短小、碎裂的线粒体,这是结构损伤的标志。测量结果证实线粒体ROS激增,同时线粒体膜电位——衡量功能的重要指标——下降。细胞通过上调以应激传感器Nrf2为主导的内部防御体系作出反应,但这些防御不足以挽回局面。重要的是,铁死亡阻断剂减少了线粒体ROS并部分恢复了线粒体健康,直接将受损的“动力工厂”与这一依赖铁的死亡途径联系起来。
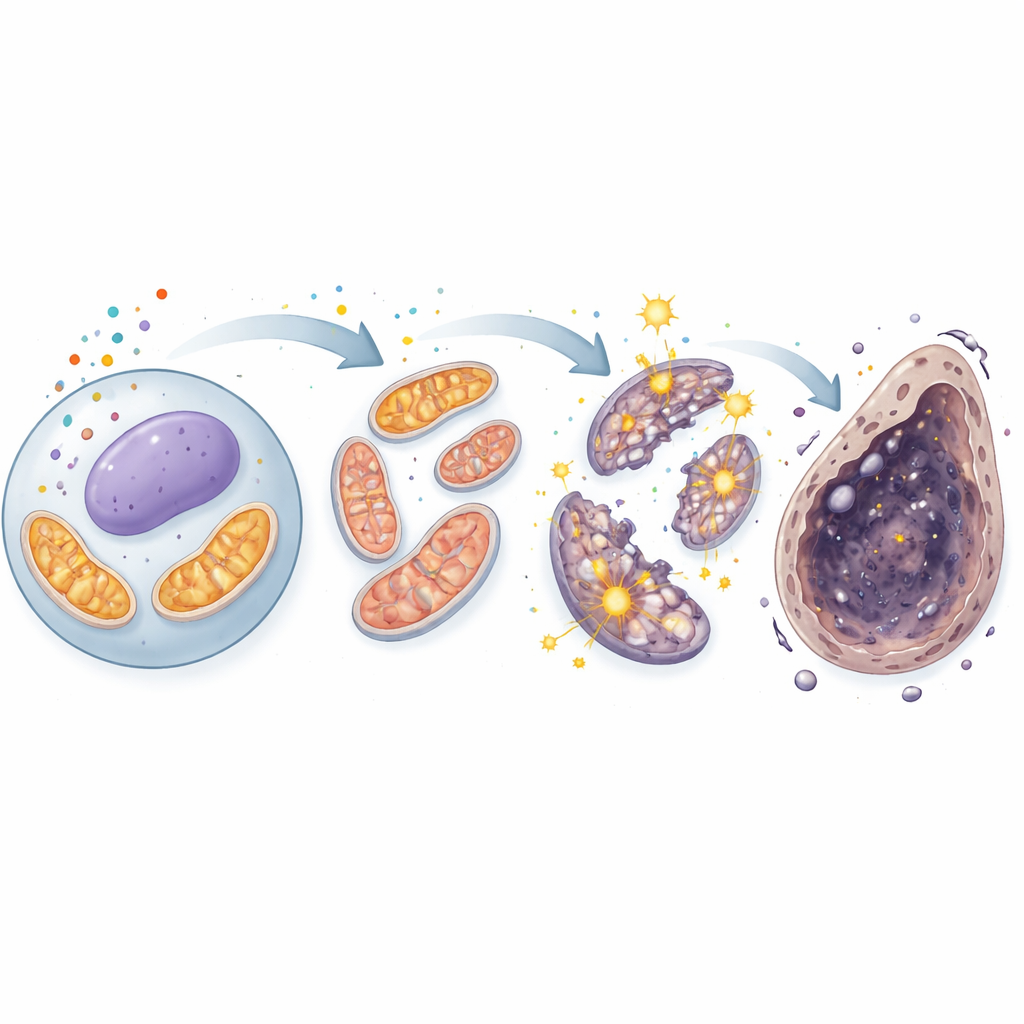
细胞动力工厂中的恶性循环
通过基因表达谱与代谢物测定相结合,研究者发现镉不仅仅损伤线粒体——它似乎劫持了线粒体的核心能量回路,即三羧酸(TCA)循环。两种关键的TCA中间产物α-酮戊二酸和琥珀酸显著升高,而将新燃料输入循环的酶丙酮酸羧化酶活性也被增强。这表明在受损细胞中,TCA循环异常过度活跃,迫使更多电子流经呼吸链并导致更多ROS泄漏。额外的ROS又反馈影响铁化学与膜损伤,强化了铁死亡。再次强调,铁死亡抑制剂能回拨这些代谢紊乱,强调了镉、线粒体过载与依赖铁的细胞死亡之间的紧密联系。
对生育力和未来研究的意义
简而言之,这项研究表明镉通过直接损伤精子形成细胞的线粒体并使其能量循环陷入有害的过度运转来攻击这些细胞。这种组合使细胞充斥活性氧并扰乱铁稳态,推动它们走向铁死亡。由于精母细胞对产生健康精子至关重要,它们的丧失可以解释镉暴露为何与男性生育力下降密切相关。尽管这些实验是在培养皿中的小鼠细胞完成,但它们提供了一个清晰的机制图谱,未来动物与人类研究可以据此验证。该工作还突出了潜在的保护策略:能缓解线粒体应激、精细调控TCA循环或防止铁驱动的膜损伤的药物或营养物质,可能有助于保护男性生殖系统免受镉等环境金属的伤害。
引用: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
关键词: 镉毒性, 男性生育力, 线粒体应激, 铁死亡, 活性氧种