Clear Sky Science · zh
极端嗜热Ts2631内溶菌酶热稳定性的残基级决定因素
嗜热病毒为何对未来抗生素至关重要
随着抗生素耐药性的上升,科学家正竞相寻找新的杀灭危险细菌的方法。一种有前景的策略借用了感染细菌的病毒——噬菌体——的武器。这些病毒产生的酶称为内溶菌酶,能够在细菌细胞壁上打孔。这里讨论的研究聚焦于一种异常耐热的内溶菌酶Ts2631,来自冰岛温泉中的病毒。通过揭示构成该蛋白的哪些单个组分使其在近沸点温度下仍然稳定,研究人员希望为医疗和生物技术设计更坚固、更持久的抗菌酶提供基础。
在沸腾温泉中锻造的病毒工具
Ts2631来自感染嗜热细菌Thermus scotoductus的噬菌体,该细菌能在超过60 °C的水体中生长。Ts2631酶切割肽聚糖中的特定位点——这是围绕细菌细胞的坚韧网状结构。Ts2631的显著之处在于其极高的热稳定性:在不同溶液中其折叠状态可维持到约100–105 °C。这远高于大多数蛋白质发生解折叠的温度。作者将Ts2631与研究最多的近缘蛋白、来自中温噬菌体的T7溶菌酶进行了比较,以弄清自然界采用了哪些结构策略使Ts2631在如此苛刻的条件下仍能保持完整。
更短的回环和不同的构成混合
蛋白质由20种氨基酸构成,通过折叠形成复杂的三维结构。当研究人员将Ts2631与T7溶菌酶的三维结构叠合时,发现整体架构非常相似:两者都有由螺旋和链构成的紧凑核心。关键差异在于连接这些元件的柔性回环区域。Ts2631中的这些回环更短且柔性更低,而T7溶菌酶则具有更长、更松弛的回环。Ts2631还富含某些通常与耐热性相关的氨基酸:刚性的脯氨酸运动受限;芳香族残基如酪氨酸和色氨酸;以及带正电的精氨酸。与此同时,它含有较少的丝氨酸、天冬氨酸和谷氨酸,这些残基在高温下可能使蛋白更脆弱。这一模式不仅在与T7溶菌酶的对比中成立,在将Ts2631与数十万计的病毒蛋白和数百万计的细菌蛋白比较时也同样明显。
通过交换单个氨基酸测试其重要性
为了从相关性走向因果关系,团队系统性地替换了Ts2631中的55个单个氨基酸,并测量每个突变对熔点温度(Tm)和酶降解细菌细胞壁能力的影响。一些围绕含锌的活性位点的变化特别破坏性。当他们改变三个配位锌的残基(H30、H131和C139)时,蛋白的Tm最多下降了约20 °C,并且活性丧失。两个保守的酪氨酸(Y60和Y69)也对稳定性有贡献。出人意料的是,去除二硫键——连接半胱氨酸C80和C90的一种共价键——实际上提高了熔点温度,尽管它破坏了活性。这表明在试验管中高度稳定并不总是意味着蛋白在真实条件下功能更好。
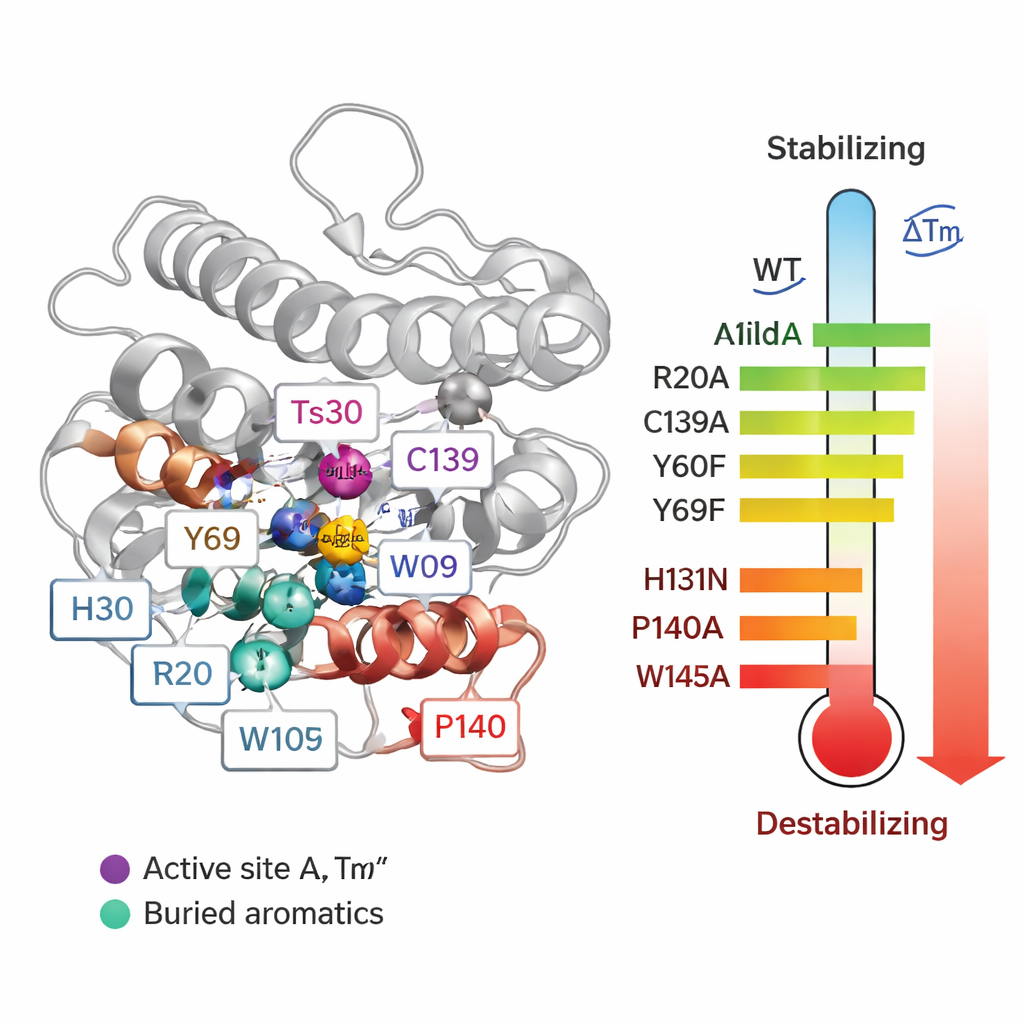
隐藏的芳香族“锚点”和对细胞壁的关键抓手
最引人注目的结果来自对脯氨酸和色氨酸残基的突变。将一个位于锌配位C139旁边的脯氨酸(P140)替换,会使Tm下降超过21 °C,并在加热后显著削弱活性,因为该突变破坏了金属配位所需的特殊键几何。若干深埋的色氨酸(W102、W109,尤其是W145)同样至关重要:将它们替换为丙氨酸导致Tm下降14–24 °C,并使酶在活性测试中对高温更敏感。这些芳香族残基像内部锚点一样将蛋白核心锁定。对于精氨酸来说,大多数残基对稳定性影响不大,但R20被证明对应肽聚糖的抓握至关重要。当R20被替换时,酶对细胞壁的结合能力下降,并在加热后失去活性,表明有些残基对功能的贡献超过对纯粹热稳定性的贡献。
从温泉酶到更坚固的抗菌剂
综合来看,研究表明Ts2631的非凡耐热性依赖于少数位置精确布置的氨基酸,而不是对整个蛋白进行均匀强化。配锌残基、活性位点附近的保守脯氨酸和埋藏的芳香族侧链共同形成了一个稳定核心,而一些经典的稳定特征(如二硫键或盐桥)在这里的重要性低于预期。对于更广泛的领域而言,这项工作表明可以通过谨慎地将中温内溶菌酶的某些位点替换为色氨酸或脯氨酸,来提高其耐久性而不牺牲抗菌活性。换言之,通过学习自然如何构建能抵抗近沸温度的酶,科学家们获得了用于工程更可靠、寿命更长的基于蛋白质的抗生素的实用蓝图。
引用: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
关键词: 耐热内溶菌酶, 噬菌体酶, 蛋白质热稳定性, 抗生素耐药性, 蛋白质工程