Clear Sky Science · zh
同型半胱氨酸诱导血管平滑肌细胞向泡沫细胞转化的生物标志物研究
为什么动脉堵塞始于微小的细胞变化
动脉粥样硬化——动脉缓慢堵塞和硬化——是导致心肌梗死和中风的主要原因之一。我们通常听到的是胆固醇和饮食,但较少关注血管壁中单个细胞在疾病发展过程中的改变。本研究深入考察了一个触发因素——血液中的分子同型半胱氨酸,展示了它如何促使通常行为规整的血管平滑肌细胞囤积脂质并转变为所谓的泡沫细胞,而这些泡沫细胞正是危险斑块的构建单元。
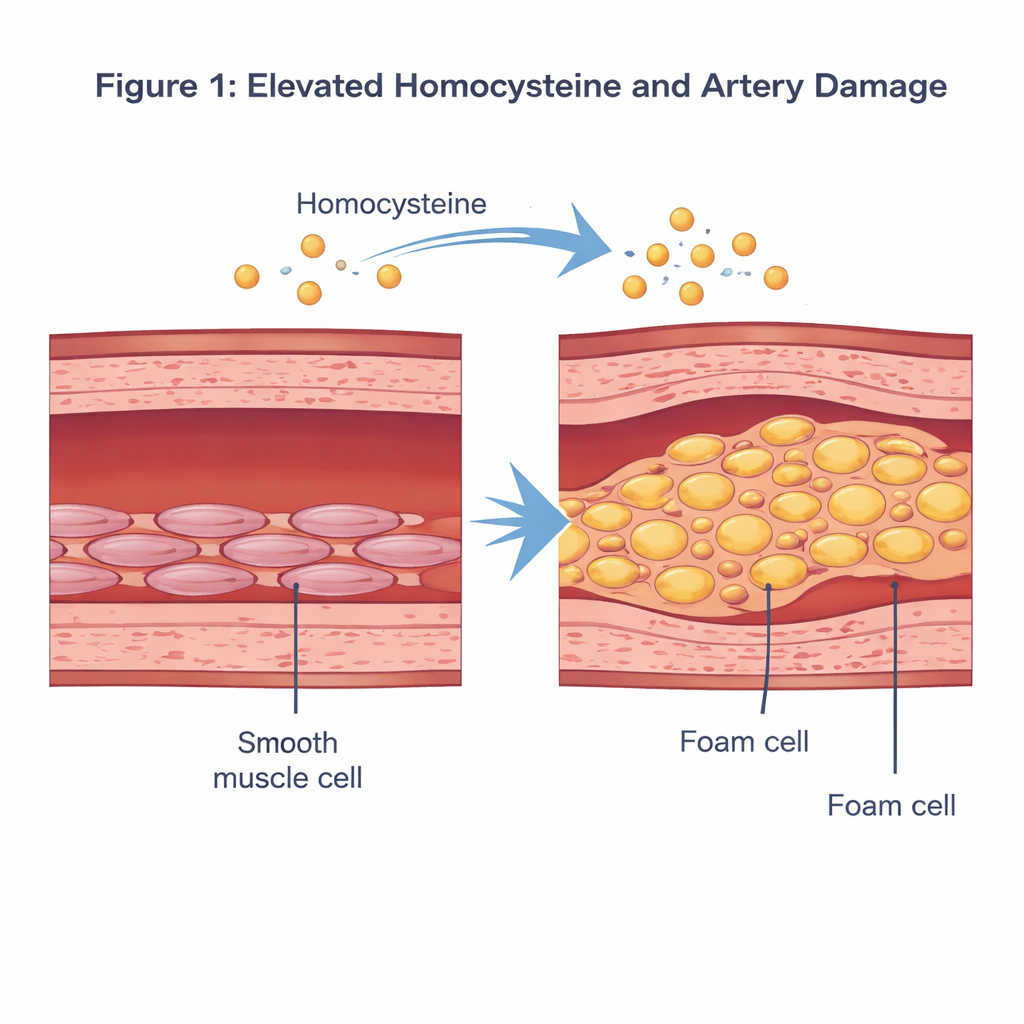
血液中的含硫氨基酸麻烦制造者
同型半胱氨酸是一种含硫氨基酸,在机体代谢膳食营养素蛋氨酸时产生。正常情况下,其血浓度较低。当其升高到约15微摩尔/升以上(称为高同型半胱氨酸血症)时,流行病学研究已将其与心血管疾病风险增加联系起来。早期研究表明,过量的同型半胱氨酸可损伤动脉内皮,激发炎症,并改变位于血管壁中层、通过收缩与舒张调节血压的血管平滑肌细胞的行为。
血管肌细胞如何转变为载脂泡沫细胞
研究者聚焦于同型半胱氨酸如何重塑这些平滑肌细胞。在体外培养皿中,他们给予人源血管平滑肌细胞模拟疾病状态的同型半胱氨酸剂量,并与未处理的细胞进行比较。通过常规染色和生化检测,他们观察到同型半胱氨酸处理的细胞充满了呈红色的脂滴,且胆固醇和甘油三酯水平均显著升高。与此同时,代表其常规“收缩型”特征的蛋白标志物下降,而代表更具合成性、促斑块形成状态的标志物增加。综合这些变化表明,同型半胱氨酸能将平滑肌细胞从其正常功能驱离,使其趋向类似泡沫细胞的脂质负荷表型,直接促进斑块形成。
在细胞内寻找分子指纹
为了解在该转化过程中哪些蛋白发生改变,研究团队采用了现代蛋白质组学技术,这种技术可以同时测量数千种蛋白。他们比较了同型半胱氨酸处理细胞与对照细胞的蛋白水平,并可靠定量了近4,800种蛋白。在这些蛋白中,有54种显著改变:13种上调,41种下调。许多变化的蛋白参与脂质处理、细胞存活、氧化应激以及细胞结构重塑。作者随后使用生物信息学工具将这些蛋白分组到功能通路中,并绘制它们之间的相互作用网络,突出与胆固醇代谢和血管壁应激反应相关的网络。
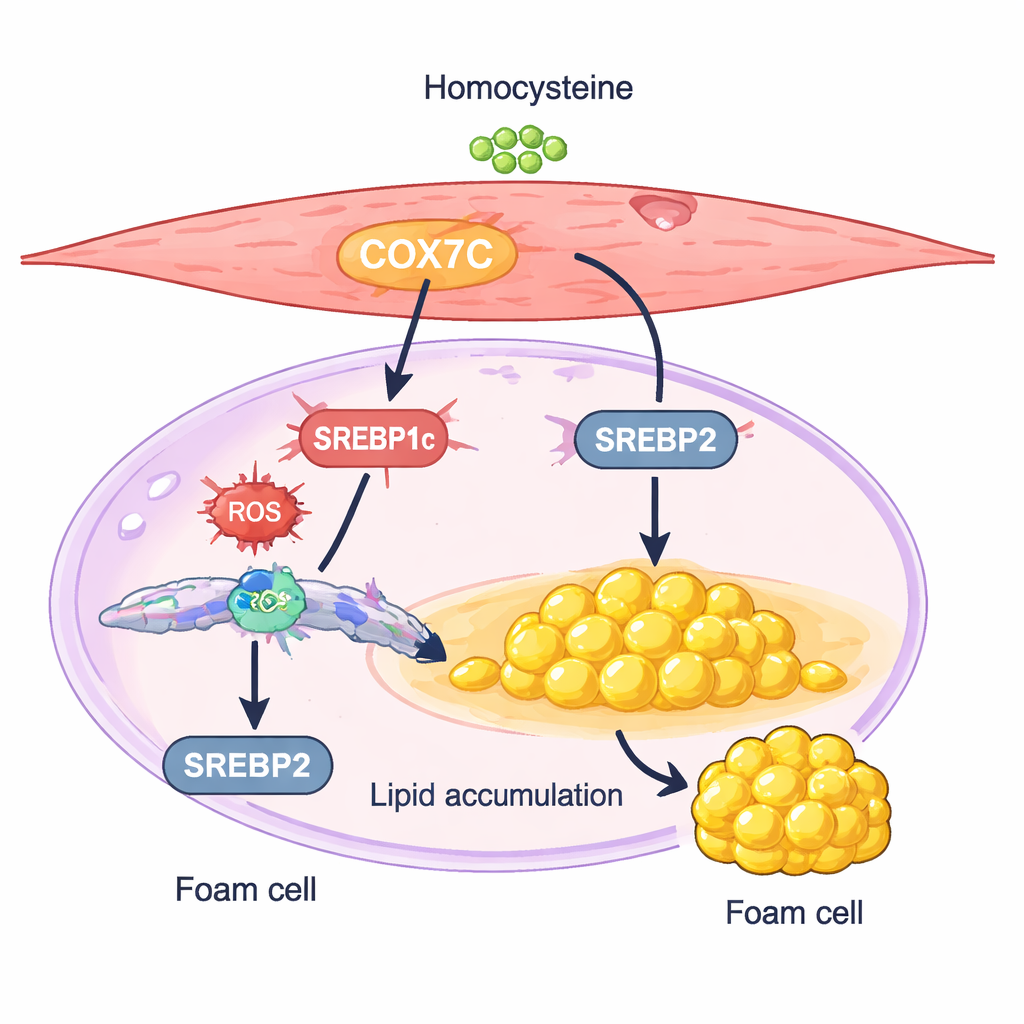
推动细胞储脂的线粒体开关
有一种叫做COX7C的蛋白成为了特别有趣的嫌疑对象。COX7C是线粒体这一细胞能量工厂的组成部分,参与能量产生的调控。在同型半胱氨酸处理的平滑肌细胞中,COX7C的水平高于对照组。研究者证明,进一步增加COX7C会使细胞积累更多脂质,并提高两种脂质合成主调控因子SREBP1c和SREBP2的表达。沉默COX7C则产生相反效果:削弱SREBP活性,减少胆固醇和甘油三酯的积累,并减轻类似泡沫细胞的变化。这些结果支持这样一种模型:同型半胱氨酸在细胞线粒体中上调COX7C,增加细胞应激信号,进而激活SREBP驱动的脂质合成,使平滑肌细胞转向囤积脂质的状态。
对心脏健康和未来疗法的意义
这项工作尚不能证明这些变化在人体动脉中也会发生,且研究是在培养细胞中完成,而非患者体内。然而,它提供了关于升高的同型半胱氨酸如何促使有益的动脉肌细胞转变为有害泡沫细胞的详尽观察,并将COX7C及相关蛋白识别为潜在的生物标志物或药物靶点。对普通读者来说,关键讯息是,除了“好”与“坏”胆固醇之外,血液化学的小幅改变——例如同型半胱氨酸过高——也能从内部重新编程血管壁。通过定位像COX7C和SREBP通路这样的分子参与者,这项研究为未来通过阻止动脉细胞成为微型脂质储存库来阻止斑块形成的策略奠定了基础。
引用: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
关键词: 动脉粥样硬化, 同型半胱氨酸, 泡沫细胞, 血管平滑肌细胞, COX7C