Clear Sky Science · zh
新的氨基嘧啶-4-基-1H-吡唑衍生物的化学合成作为脾酪氨酸激酶(SYK)抑制剂
为何阻断单一酶可助于抗击癌症和炎症
我们的免疫系统依赖快速的内部信号传递来指示细胞何时攻击入侵者、何时停止。当这些信号出错时,可能导致自身免疫疾病和癌症。本研究探索了一种有前景的方法,通过设计选择性阻断关键酶脾酪氨酸激酶(SYK)的小分子药物来抑制这些错误信号,SYK位于许多免疫反应的核心位置。
许多疾病核心处的信号开关
SYK在某些免疫细胞内像个主控开关。被激活时,它促使炎症、抗体产生和细胞增殖。在健康情况下,这有助于抵抗感染。但在类风湿性关节炎、哮喘以及若干血液和实体肿瘤等疾病中,SYK活性可能过度,导致免疫细胞持续处于激活状态并支持肿瘤存活。正因为其中心作用,全球研究者致力于开发既有足够效力又能精确避免作用于大量其他酶从而减少副作用的SYK抑制剂。
构建一系列量身定制的小分子
作者以一种被称为氨基嘧啶-4-基-1H-吡唑的通用化学骨架为核心,创建了一系列相关分子。研究人员从简单的构件出发,逐步拼合这些片段,然后修改结构的一部分,最终得到九个候选化合物。每一分子都用标准的分析方法仔细鉴定,以确认其结构和纯度符合预期。该模块化方法使团队能够探究形状和柔性等细微变化如何影响这些化合物与SYK的相互作用。
观察这些化合物如何抓住其靶点
在进入实验室之前,研究者使用计算机模拟来评估每种分子可能与SYK结合的紧密程度。对接计算估算了化合物与酶结合口袋的契合度,其中编号为44的候选者尤为突出。更详细的分子动力学模拟(追踪蛋白-药物复合体数百纳秒)显示,44与SYK形成尤其稳定的结合。蛋白保持紧致,关键接触位点稳定,体系趋向于单一低能量构象,并形成多处强氢键,特别是与色氨酸和丝氨酸等氨基酸的相互作用,有助于“托住”该分子。
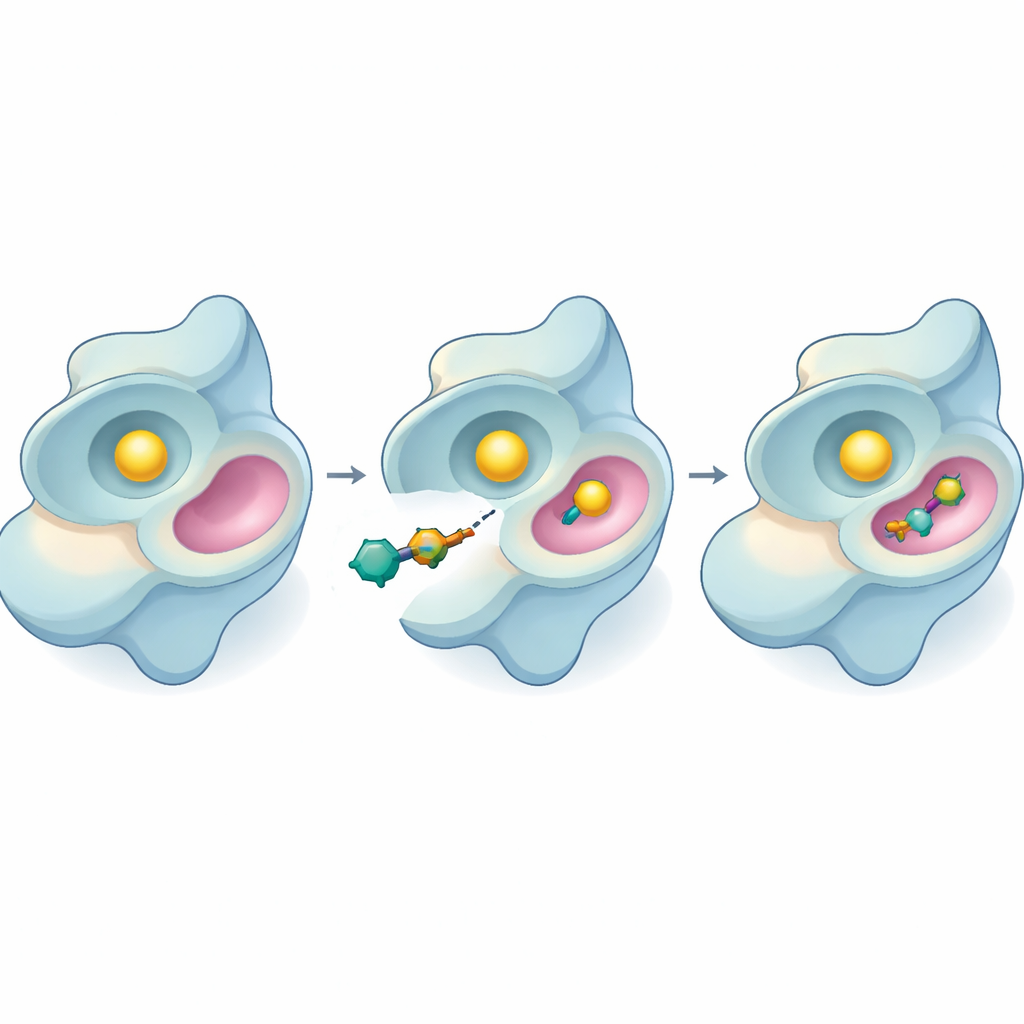
将新抑制剂付诸考验
随后团队通过一种基于发光/光学的测定在实验室中检验,评估SYK消耗其底物ATP的活性。若干新化合物减缓了该酶的活性,但44再次表现突出。它在极低浓度下就能抑制SYK,并且随与酶接触时间延长而效力增强。通过改变底物含量,研究者推断44的作用方式:它并非直接与ATP在主要活性位点竞争,而是可能结合到另一个变构位点,从远端改变酶的行为。这一点很重要,因为变构抑制剂通常在ATP水平较高或主位点发生突变时仍能维持作用。
这对未来治疗意味着什么
综合计算模型和实验测量,描绘出一致的结论:分子44与SYK结合紧密,使酶保持在一种更稳定、较不灵活的状态,并通过一种间接、非竞争的机制关闭其活性。对非专业读者而言,这意味着研究者找到了一把经精细调校的化学“钥匙”,能契合对许多免疫驱动疾病至关重要的“锁”,而不是简单地堵塞主要开口。尽管仍需大量后续工作——尤其是细胞、动物实验以及对更广泛相关酶面板的测试——这一骨架为未来通过靶向SYK来抑制有害炎症并减缓某些癌症的发展提供了有希望的起点。
引用: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
关键词: 脾酪氨酸激酶, 激酶抑制剂, 癌症治疗, 自身免疫性疾病, 变构药物