Clear Sky Science · zh
在泛癌症分析中鉴定出的潜在肺腺癌标志物:PTGDS
为何一 种鲜为人知的酶对癌症患者可能至关重要
大多数人可能从未听说过PTGDS,这是一种帮助我们体内合成类激素分子——前列腺素的酶。然而,这个不起眼的因子可能为我们理解癌症如何生长、如何与免疫系统相互作用以及为何某些肺肿瘤更具侵袭性提供重要线索。在这项研究中,研究人员梳理了庞大的癌症数据库并进行了实验室实验证实,观察PTGDS在多种肿瘤类型中的表现,以及它是否可以作为癌症的警示信号——甚至成为抑制肿瘤的“刹车”,特别是在非吸烟人群中最常见的肺腺癌。
以广泛视角观察多种癌症
为了从宏观层面理解PTGDS,研究团队开展了所谓的“泛癌症”分析,利用癌症基因组图谱(The Cancer Genome Atlas)等大型公共资源以及跟踪RNA、蛋白质、DNA变化等的多组学数据,考察了33种不同癌症类型中PTGDS的活性。他们发现,与健康组织相比,大多数癌症在基因和蛋白水平上PTGDS水平异常降低。只有少数肿瘤类型(如卵巢癌和胰腺癌)表现出较高的水平。这些模式提示,在许多情况下,PTGDS更可能充当保护者而非促癌因子。
来自患者生存和肿瘤DNA的线索
研究人员接着考察PTGDS水平是否与患者生存时间或疾病进展速度相关。在包括肺腺癌和某些脑肿瘤在内的几种癌症中,较高的PTGDS与更好的生存相关;而在某些肾脏肿瘤中则与更差的预后相关,这暗示其作用强烈依赖于组织与疾病的具体背景。他们还研究了PTGDS基因在肿瘤DNA中被改变的频率,以及其与肿瘤基因不稳定性指标(如肿瘤突变负荷和微卫星不稳定性)的关系。在许多癌症中,较高的PTGDS常与较少的突变和较低的“干样”特征并存,而这些特征通常标志着较低的侵袭性疾病。
肿瘤周边环境与免疫系统
癌症并非孤立生长——它持续与周围的支持细胞和免疫细胞相互作用。利用从基因表达推断免疫细胞存在的计算工具,研究团队发现PTGDS水平与肿瘤内免疫细胞和结缔组织细胞的数量密切相关。在肺腺癌和其他几种癌症中,较高的PTGDS与关键免疫细胞(如T细胞、B细胞、巨噬细胞和自然杀伤细胞)的更多浸润相关。单细胞数据集(逐一分析单个细胞)显示,在正常肺组织中,PTGDS在成纤维细胞(结构细胞)、血管细胞和若干免疫细胞类型中特别活跃。这支持了PTGDS参与塑造肿瘤“邻里”环境的观点,可能影响免疫系统识别和控制癌细胞的能力。
聚焦肺癌:细胞内的工作机制
由于在肺腺癌中观察到的模式尤其显著,研究人员在实验室中对该癌种进行了更深入的研究。他们在两条人类肺癌细胞系(A549和H1975)中改变了PTGDS水平。当他们强制细胞表达更多PTGDS时,细胞生长减慢、克隆形成减少,表明肿瘤样行为被抑制;降低PTGDS则产生相反效果:细胞增殖更快。进一步的实验显示,额外的PTGDS改变了细胞利用脂肪类燃料的方式,增强了脂肪酸分解同时抑制了支持快速生长的通路。它还扰动了正常的细胞分裂周期,使细胞在再次分裂前停滞更久。有趣的是,尽管某些与细胞死亡相关的蛋白上调,但总体细胞凋亡并未显著增加,这表明PTGDS主要通过减缓生长而非直接诱导大量细胞死亡来起作用。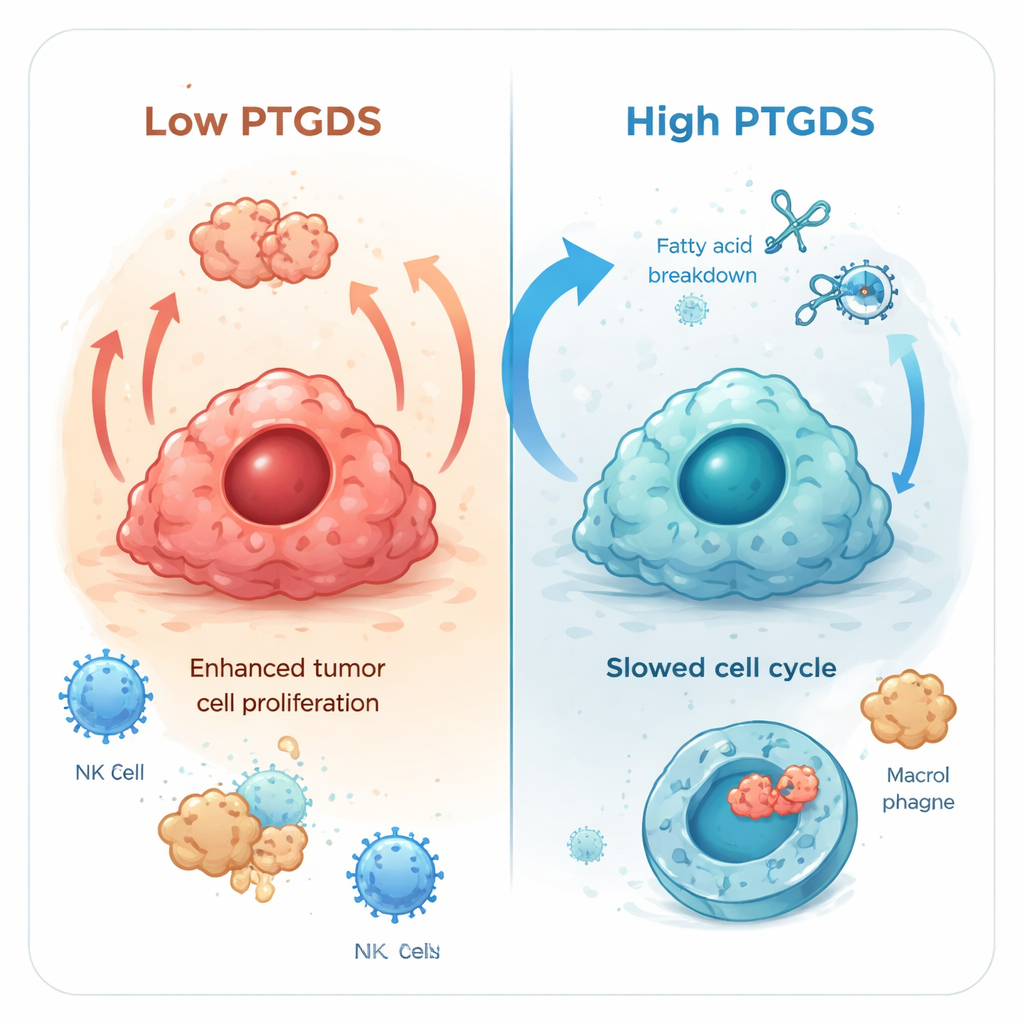
表观遗传开关与微RNA调控
研究还探讨了PTGDS自身的调控机制。团队发现,PTGDS基因区域在肺肿瘤中的某些DNA化学修饰(称为甲基化)比正常肺组织更为常见,且其中若干甲基化位点与PTGDS的表达量相关。这提示肿瘤可能通过表观遗传开关沉默PTGDS。此外,通过扫描微小调控RNA(microRNA)的模式,他们指出了一个候选者miR‑3944,该分子在肺肿瘤中更为丰度且与PTGDS水平呈负相关。综合来看,这些发现表明肿瘤可能通过多层次的调控机制来调节PTGDS的表达。
这对未来患者可能意味着什么
对非专业读者而言,关键结论是PTGDS在许多癌症中呈现出被下调的稳定模式,尤其在肺腺癌中,其似乎扮演着抑制肿瘤生长的天然“刹车”角色。PTGDS的水平不仅与肿瘤的生长和分裂有关,还与肿瘤如何与机体免疫防御互动以及如何利用能量燃料相关。尽管仍需更多研究——包括动物实验和临床验证——PTGDS最终或可帮助医生更好地预测预后,筛选更可能从特定免疫疗法中获益的患者,并可能激发恢复或模拟其肿瘤抑制作用的新型治疗策略。
引用: Wang, R., Shao, F., Liu, D. et al. PTGDS is a potential marker for lung adenocarcinoma identified in a pancancer analysis. Sci Rep 16, 7611 (2026). https://doi.org/10.1038/s41598-026-38688-0
关键词: 肺腺癌, 癌症生物标志物, 肿瘤微环境, 脂肪酸代谢, 前列腺素D2合酶