Clear Sky Science · zh
ConvAHKG:基于作用的混合知识图谱与双通道卷积方法用于药物重新定位
为老药寻找新用途
将一种全新药物推向市场可能需要十多年并耗资数十亿美元,而且许多候选药物在此过程中失败。本文研究一种更聪明的捷径:利用数据和人工智能发现现有、已获批准药物可能安全治疗的新疾病。作者提出了一个名为 ConvAHKG 的框架,它将多种生物医学信息编织成单一的连接地图,然后用现代神经网络识别有希望的药物—疾病配对——为新疗法提供更快、更廉价的路径。
描述药物与疾病相互作用的丰富地图
该工作的核心是一个“混合知识图谱”,这是一个将药物、疾病、蛋白质、副作用、化学结构与生物通路等连接起来的巨大地图。图谱并非仅记录简单的是/否关联(例如“药物 A 治疗疾病 B”),而是记录药物如何作用于蛋白质——例如激活、抑制或结合——以及蛋白质如何参与疾病,例如作为生物标志物或活动变化。该图谱包含超过 11,000 个实体和 59 种关系类型,包括关于药物分类、副作用、蛋白质相互作用以及化学亚结构的详细信息。通过捕捉这些多层次的上下文,图谱能够更好地反映治疗效果和不良反应背后的真实生物复杂性。 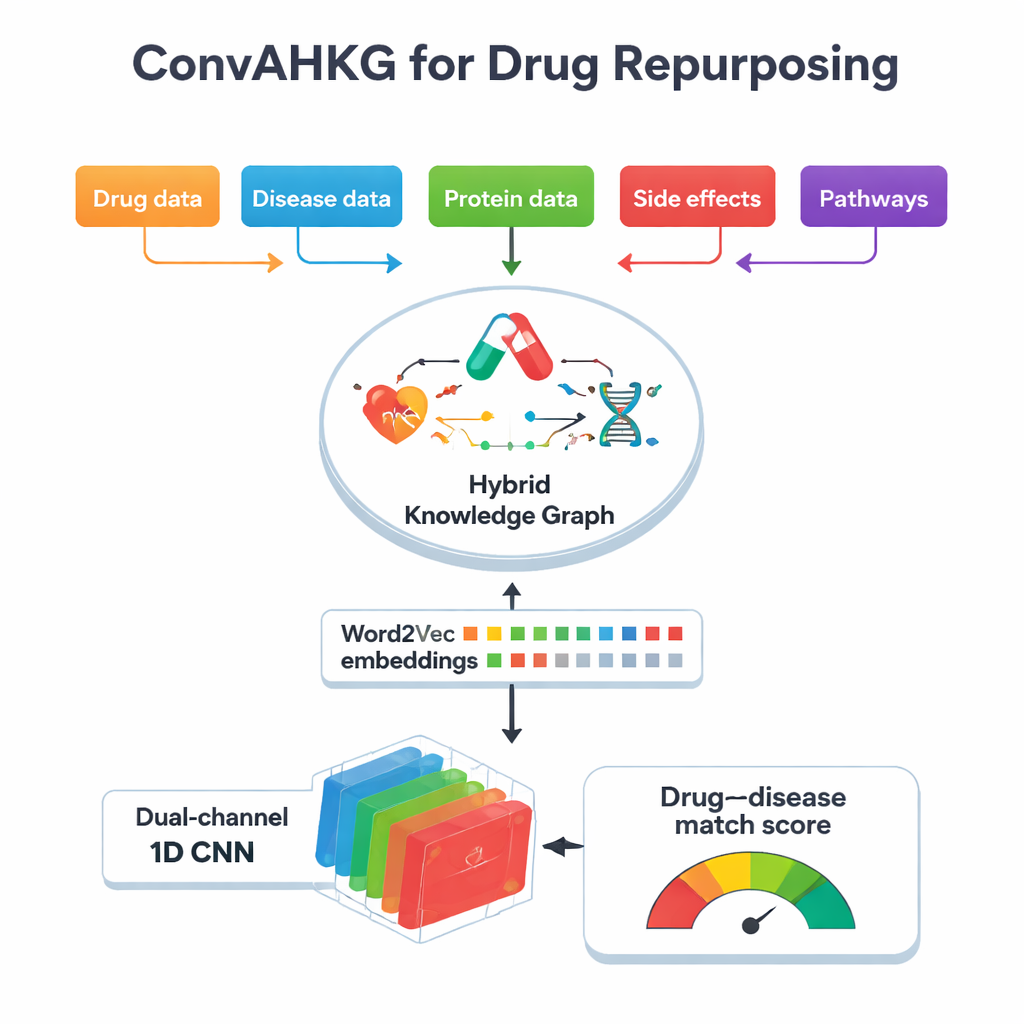
教计算机“生物学的语言”
为了使这个复杂的图谱可用于机器学习,团队将图中每个连接转换为一个简单的三部分“句子”:主项(例如疾病)、关系(例如生物标志物)和宾项(例如蛋白质)。然后他们应用 Word2Vec——一种最初为自然语言处理开发的方法——为每种药物、疾病和蛋白质学习数值“嵌入”。经常在这些句子中共同出现的项在这个数学空间中会彼此靠近,就像在文本中意义相近的词会靠近一样。这种方法比许多针对图的嵌入技术要简单且更快速,但仍能捕捉细微模式。在与几种流行的知识图谱嵌入方法的比较测试中,Word2Vec 在预测能力上与它们相当或更优,同时使用的计算时间远少于这些方法。
用于二元治疗决策的双重神经通路
一旦每种药物和疾病被转换为数值向量,ConvAHKG 将它们输入双通道一维卷积神经网络。一个通道处理药物向量,另一个通道处理疾病向量,使用一系列卷积滤波器来检测局部模式和更广泛的特征,设计灵感来自图像识别领域的架构如 InceptionNet 和 AlexNet。经过各自处理后,两条流合并并通过若干全连接层,输出一个单一概率:该药物—疾病配对更可能是有效治疗还是更可能为有害副作用。为应对已知正例远少于负例的问题,作者引入加权损失函数,对漏检真实治疗的情况给予更重的惩罚,从而提升对这些难以发现的病例的性能。 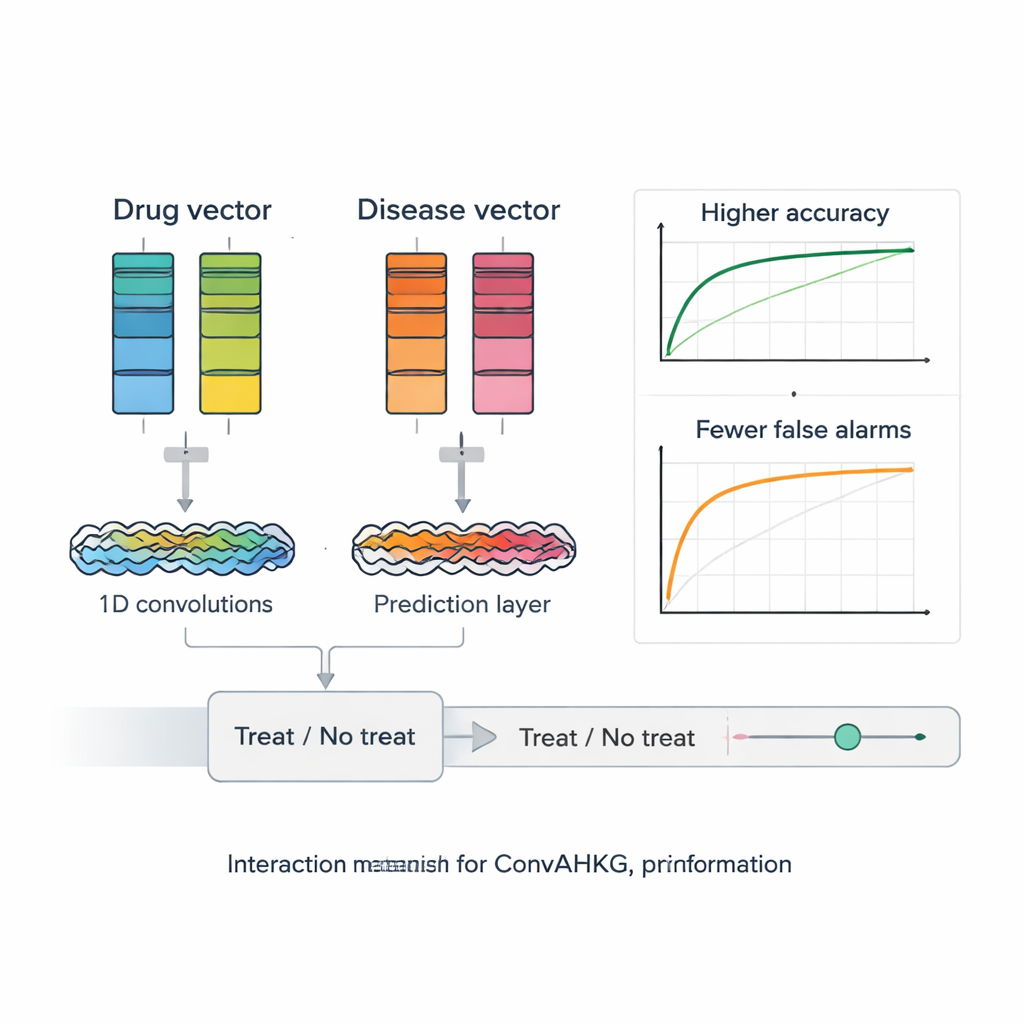
超过现有方法并识别癌症候选药物
研究者将他们的框架与若干最先进的药物重新定位工具进行了严格比较,这些工具采用矩阵分解、图神经网络和深度自编码器等方法。在相同基准数据集上,ConvAHKG 实现了 0.9836 的 ROC 曲线下面积和 0.9686 的精确率—召回率曲线下面积,优于所有竞争方法。随后他们将模型应用于非小细胞肺癌——全球最常见且致死性最高的肺癌类型。ConvAHKG 突出了若干此前未标注为该病治疗药物的候选药物,包括靶向 HER2 蛋白并已有肺癌临床证据支持的抗体曲妥珠单抗,以及其他生物制剂,甚至经典抗生素苄青霉素。对接模拟表明苄青霉素可能与 DNA 及常在此类肿瘤中升高的拓扑异构酶 IIα 强烈结合,提示一种可能的抗癌机制,值得开展实验室验证。
这对患者为何重要
简单来说,ConvAHKG 类似一个知识渊博的媒人,将现有药物与疾病相匹配:它利用详尽的生物作用地图和强大的模式识别引擎来预测哪些老药可能在新适应症中有效。通过将已通过安全性测试的药物视为可重复使用的构件而非单一用途工具,这一框架可加速针对如肺癌等疾病的疗法发现,尤其在传统药物开发过慢或成本过高时更具价值。尽管这些预测仍需谨慎的实验与临床验证,但该研究表明,将丰富的生物学知识与现代人工智能结合,可以大幅缩小搜索范围,使潜在救命疗法更快地变为可能。
引用: Khodadadi AghGhaleh, M., Abedian, R., Zarghami, R. et al. ConvAHKG: Action-based hybrid knowledge graph with a dual-channel convolutional approach for drug repurposing. Sci Rep 16, 7592 (2026). https://doi.org/10.1038/s41598-026-38656-8
关键词: 药物重新定位, 知识图谱, 深度学习, 肺癌, 药物发现