Clear Sky Science · zh
DNMT3A p.R882C 驱动的胰腺癌细胞增殖与抗凋亡作用
这项研究为何对胰腺癌重要
胰腺癌以发现时已晚、扩散迅速且对治疗反应差著称。大多数患者被诊断为胰腺导管腺癌(PDAC),这是一种特别具有侵袭性的病型。本研究关注单一基因 DNMT3A 的一个微小改变,并提出一个重要问题:这种细微的变异能否帮助解释为何某些胰腺癌生长更快且更能抵抗细胞凋亡?理解此类变化可能为更早期的检测和更精确的靶向治疗开辟道路。
对致命癌症的更细致观察
PDAC 占胰腺癌的90%以上,五年生存率低于13%。该病通常由已知的癌基因驱动,如 KRAS 和 TP53,但许多患者仍无法从现有的靶向治疗中获益。近期研究表明,不仅基因突变,所谓的“表观遗传”变化——即控制基因开启或关闭的 DNA 化学标记——在该癌中也发挥关键作用。DNMT3A 是负责写入这些化学标记的主要酶之一,其缺陷已与急性髓性白血病等血液癌症相关联。
寻找危险的 DNA 变化
研究者从三名中至低分化 PDAC 患者采集了肿瘤样本及邻近的非肿瘤组织。他们使用全外显子测序——读取基因组中所有编码蛋白的区域——并应用严格的计算筛选以区分无害的 DNA 变异与可能损害细胞行为的变异。从数百个变异中,他们将候选名单缩小到68个高风险变化。其中,DNMT3A 的一个罕见变体 p.R882C 引人注目,因为它几乎不出现在大型人群数据库中,并且被多种预测工具一致判定为有害。
这种突变在细胞内的作用
DNMT3A 是一条由912个氨基酸构成的蛋白,参与建立 DNA 甲基化模式——这些化学标签像基因的“开/关”开关。p.R882C 位于 DNMT3A 的关键功能区域,可能会干扰酶的活性。通过三维计算建模,团队发现蛋白的整体折叠并未发生显著变化,这提示问题更可能出在酶的功能而非折叠上。为验证这一点,他们改造了胰腺癌细胞系(PANC‑1 和 PaTu 8988t),使其分别表达正常的 DNMT3A 或 p.R882C 版本,并与携带空载对照的细胞进行比较。
更快的生长、更强的迁移、更少的细胞死亡
出人意料的是,p.R882C 突变并未改变 DNMT3A 在 RNA 或蛋白水平的表达量;酶的总量大致相同。然而,该突变对细胞行为产生了显著影响。在克隆形成和生长检测中,携带突变 DNMT3A 的细胞形成了更多克隆并表现出更高的生长信号。伤口愈合和 Trans‑well 迁移实验显示,带突变的细胞迁移更快。使用流式细胞术检测程序性细胞死亡(凋亡)时,p.R882C 突变细胞在早期和晚期凋亡阶段的凋亡细胞明显更少,表明其具有显著的存活优势。
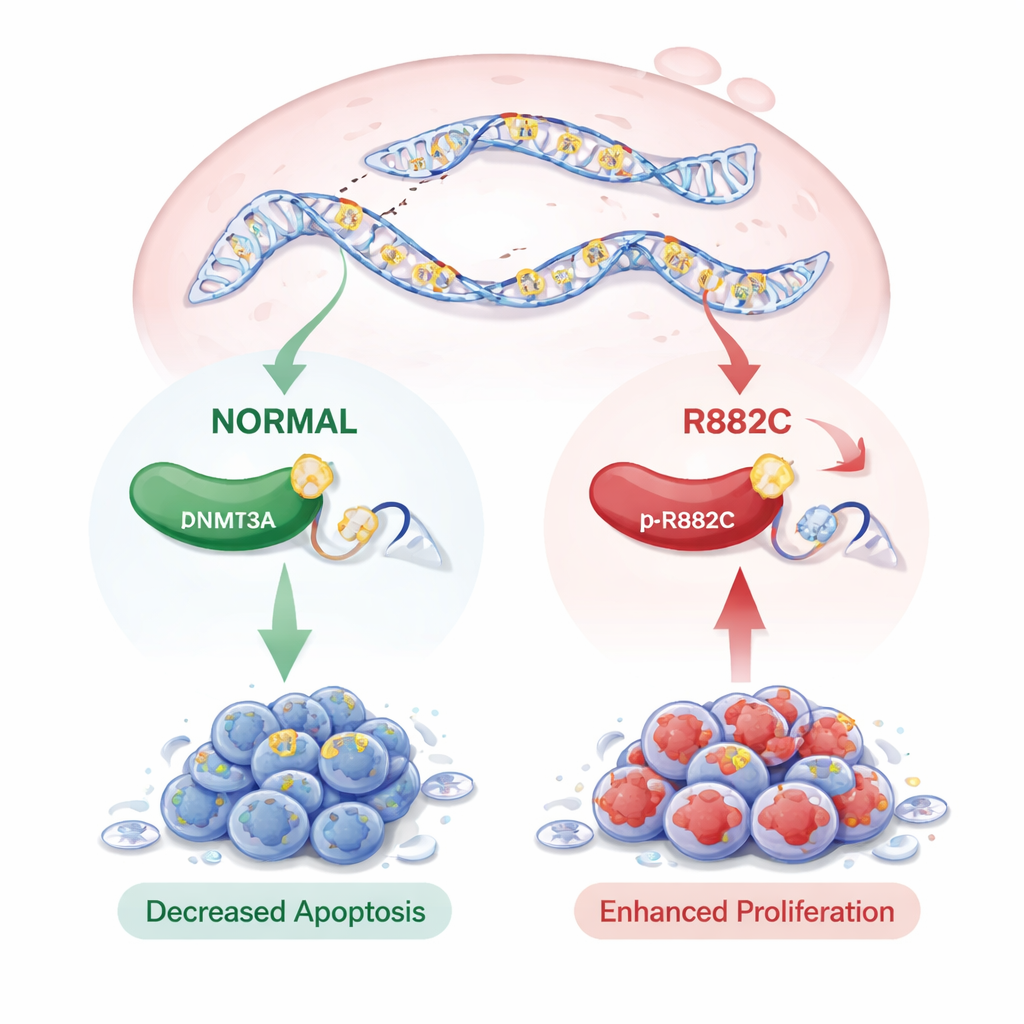
这对未来治疗可能意味着什么
综合这些发现,研究表明罕见的 DNMT3A p.R882C 突变可促使胰腺癌细胞更快生长、更易迁移并抵抗自我毁灭——这些特征可能推动癌症进展。尽管该突变并未提高 DNMT3A 的表达量,但它很可能改变酶的活性和全基因组的甲基化模式,这与某些血液癌中的观察一致。作者指出,该变异罕见,在公共数据库中尚未显示与患者生存的明确关联,部分原因是现有研究样本量小且常不包含 DNMT3A。尽管如此,在 PDAC 中发现这一突变强调了一个可能的重要新参与者,并提出未来 DNMT3A p.R882C 或可作为风险标志或用于更个性化治疗的靶点的可能性。
引用: Qu, Z., Mao, J., Qian, Y. et al. DNMT3A p.R882C driven proliferation and anti-apoptotic effects in pancreatic cancer cells. Sci Rep 16, 7659 (2026). https://doi.org/10.1038/s41598-026-38613-5
关键词: 胰腺癌, DNMT3A 突变, 胰腺导管腺癌 (PDAC), DNA 甲基化, 靶向治疗