Clear Sky Science · zh
膀胱类器官条件培养基在无血清条件下促进肌母细胞增殖
为什么在实验皿中培养肉很重要
培养肉——在大型生物反应器中培养动物肌肉细胞而不是饲养整只动物——有望带来气候影响更小、动物痛苦更少的汉堡和牛排。但目前许多实验室培养的细胞仍依赖胎牛血清,这是一种昂贵且来自动物的混合物,取自牛胎体内。本研究探索了一种用由微小三维“微器官”——类器官——自然分泌的物质来喂养肌肉细胞的新方法,指向更清洁、更具伦理性的培养肉路线,减少对传统血清的依赖。
微型器官作为微小工厂
为检验这一想法,研究者在实验室中构建了几种小鼠器官的微型版本:肺、胆囊、脾、肾和膀胱。这些类器官是模仿真实组织结构和行为的三维细胞团块,包括它们向周围液体分泌丰富生物信号的能力。团队收集了来自每种类器官的这种液体,称为条件培养基,并将其与一种简单的无血清基础溶液混合。随后,他们用这些来自类器官的混合物在不添加血清的条件下培养小鼠肌肉前体细胞,即肌母细胞。
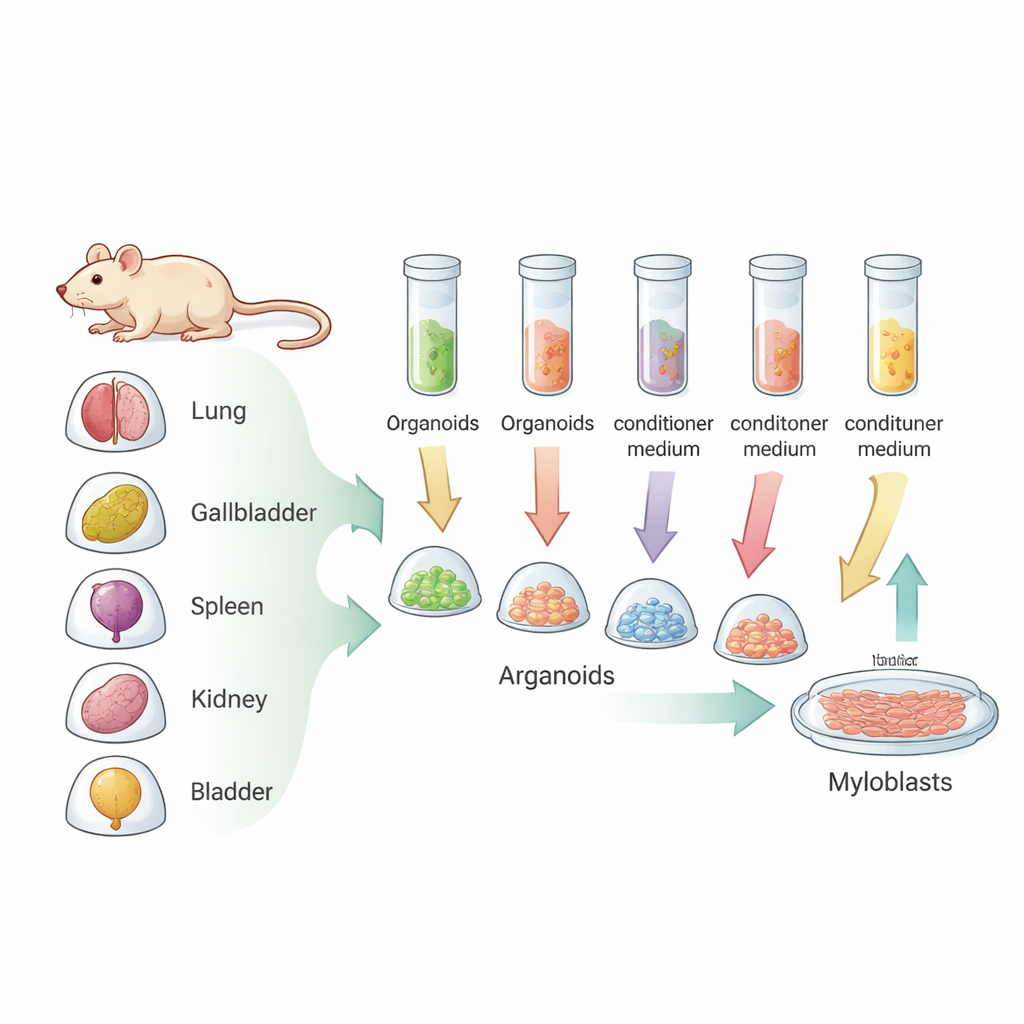
寻找最强的生长促进剂
当肌肉细胞用每种类器官来源的培养基培养时,所有处理组的生长都优于单纯的无血清基础溶液。然而,来自膀胱类器官的培养基——称为MBOS——脱颖而出。它使肌母细胞的增殖几乎可以与使用含胎牛血清的标准配方相媲美。MBOS的效果在不同批次间保持一致,且在稀释时仍然强劲,这表明膀胱微器官产生了一种尤其稳定且有效的支持生长的因子组合。
细胞内的响应机制
为了弄清MBOS在肌肉细胞内部的作用,研究者检测了细胞的基因表达活动和细胞周期行为。通过大规模RNA测序,他们发现MBOS激活了许多与细胞分裂相关的基因,特别是两个关键调控因子CCNB1和CDK1。后续在RNA和蛋白水平的测试证实这些分子在MBOS处理的细胞中更为丰富。流式细胞术——一种测量单个细胞DNA含量的方法——显示更多细胞进入了G2/M期,即分裂前和分裂期间的阶段。综合这些结果表明,MBOS更有效地推动肌母细胞通过细胞周期,帮助它们分裂并增加细胞数量。
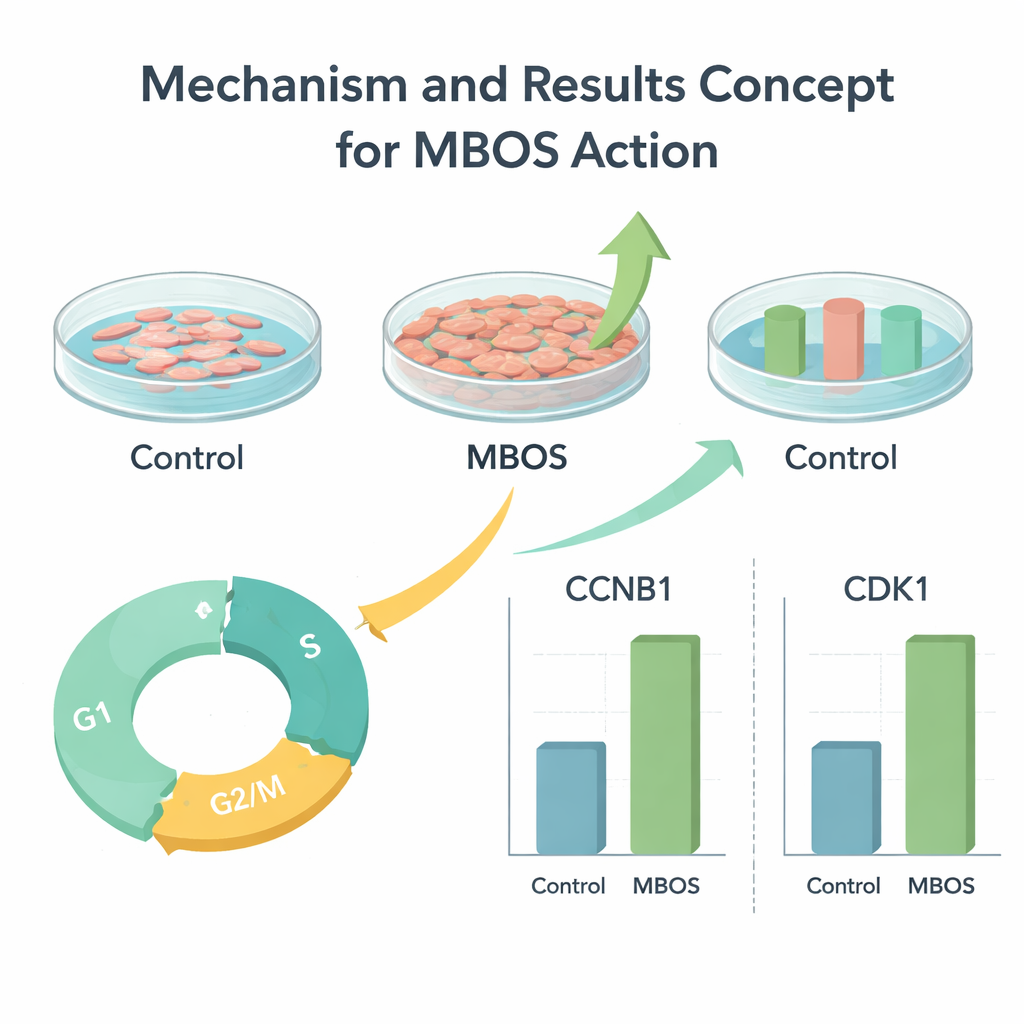
不止一种生长因子在起作用
团队还测量了MBOS中已知的肌肉生长信号水平,重点关注类胰岛素生长因子IGF-1和IGF-2。他们发现MBOS中IGF-1含量高于对照培养基,而IGF-2保持大致相同。然而,当他们加入抗体以阻断IGF-1时,肌肉细胞仍然保持强劲增殖。这表明IGF-1只是部分原因,MBOS很可能含有多种有益分子的混合物——可能包括其他生长因子和辅助蛋白——这些成分一起协同推动细胞生长,单一纯化成分无法完全复制这种效果。
从小鼠到牛,迈向未来的牛排
关键是,MBOS不仅对小鼠细胞有效。当研究者将其应用于取自牛的原代肌母细胞时,这些牛细胞在无血清对照条件下也增殖更快。这种跨物种效果暗示膀胱类器官条件培养基可能有助于支持实际食用动物的肌肉细胞扩增,而不只是用于实验模型。尽管现有类器官的培养仍然使用一些动物来源的投入,且MBOS的确切活性成分尚待绘制完整图谱,但这项工作展示了一条有前景的路径:使用类器官衍生的分泌物作为一种可重复、富含生物活性的补充,减少或最终替代培养肉生产中使用的胎牛血清。
引用: Nagashima, Y., Yamamoto, H., Elbadawy, M. et al. Bladder organoid conditioned media enhances myoblast proliferation under serum free conditions. Sci Rep 16, 7582 (2026). https://doi.org/10.1038/s41598-026-38603-7
关键词: 培养肉, 无血清培养基, 类器官, 肌母细胞增殖, 生长因子