Clear Sky Science · zh
活化T细胞通过TRPV4介导的钙流入诱导A549肺腺癌细胞凋亡
这项研究对肺癌为何重要
肺癌仍然是最致命的癌症之一,部分原因是肿瘤常常学会抵抗化疗和放疗等常规治疗。近年来,利用机体自身免疫系统带来了新的希望。本研究探讨了这一思路的一个新侧面:研究显示一种特定类型的免疫细胞——活化T细胞,能通过促使肿瘤细胞经由被称为TRPV4的分子“闸门”摄取钙离子,从而推动肺癌细胞走向自我毁灭。理解这一通路可帮助科学家设计更强大、更精准的免疫疗法。
免疫系统的“士兵”与肺肿瘤细胞相遇
研究者以人源肺腺癌细胞A549为研究对象,这是一种广泛用于非小细胞肺癌研究的模型。他们将这些癌细胞与Jurkat T细胞配对,后者作为体内杀伤性T细胞的替代模型,通常负责寻找并消灭受感染或恶性细胞。通过化学方式活化Jurkat细胞,团队模拟了处于真实免疫反应中高度警觉状态的T细胞。随后,他们以不同的比例将活化或未活化的T细胞与肺癌细胞混合并在一到三天内观察变化,重点关注有多少癌细胞存活以及经历程序性细胞死亡(凋亡)的比例。
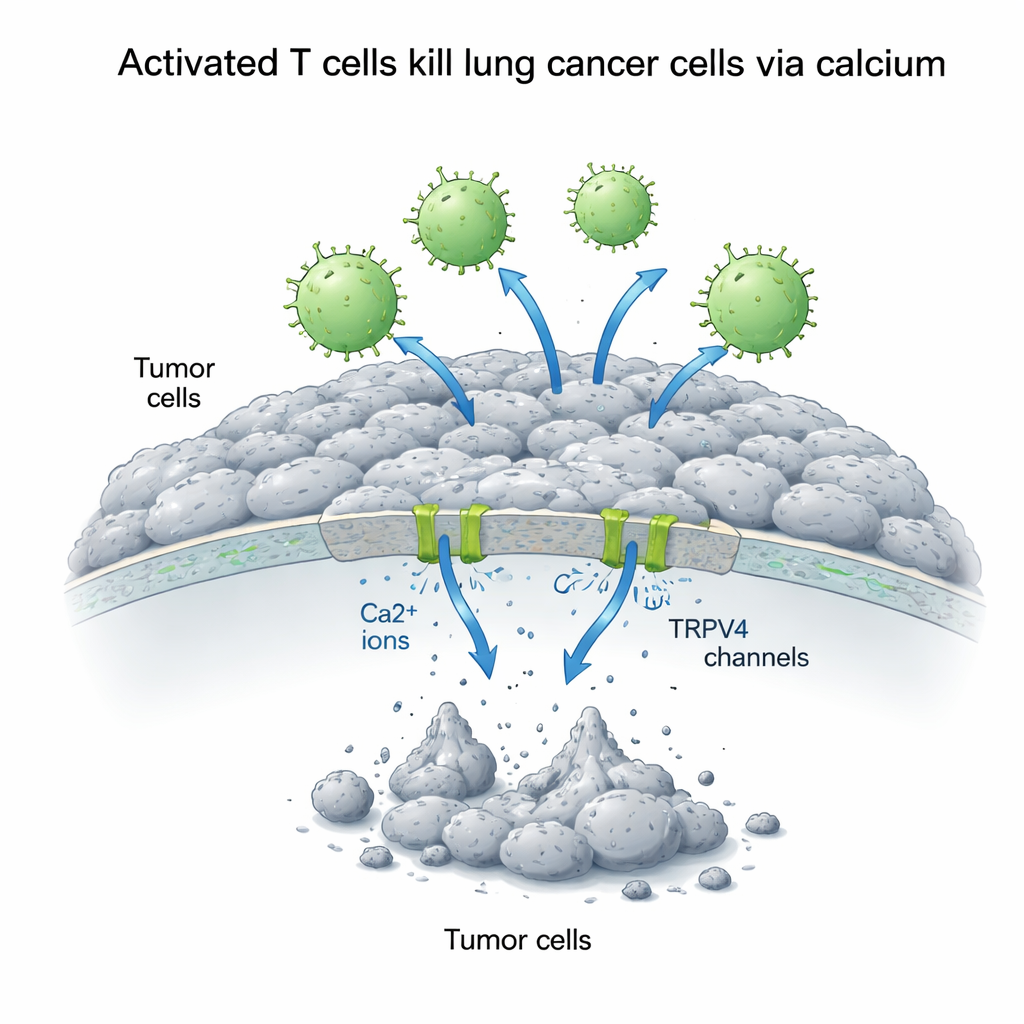
钙:对癌细胞而言的双刃信号
细胞内的钙离子像一种多功能的开关,视其处理方式不同可以促进生长或触发死亡。科学家们提高了A549细胞外的钙浓度,并测量这对T细胞与肿瘤细胞之间“较量”的影响。出人意料的是,单独增加外部钙会促进肺癌细胞的生长,表明在平稳条件下钙可支持生存通路。但当活化T细胞存在时,情况发生反转:更高的外钙显著增强了T细胞介导的杀伤。在72小时内,当活化T细胞与额外钙同时存在时,癌细胞存活率降至正常水平的不到三分之一,而未活化的T细胞几乎没有效果,且在加钙时甚至可能支持肿瘤生长。
与应激和细胞死亡相关的钙“闸门”
为弄清这种从生长到死亡的开关如何发生,团队关注了TRPV4——细胞膜上的一种允许钙流入的蛋白质通道。通过蛋白分析,他们发现无论是否存在T细胞,A549细胞在暴露于额外钙时TRPV4水平都会显著上升,而在钙与活化T细胞共同作用时达到最高。与此同时,癌细胞表现出明显的氧化应激特征:抗氧化保护能力下降(总体抗氧化能力降低),有害氧化物增加(总体氧化状态升高)。流式细胞术(一种用荧光染料标记细胞的技术)证实,活化T细胞导致早期和晚期凋亡双双激增,尤其在钙充足时更为明显。这些观察综合表明一系列事件:TRPV4通道允许更多钙进入,进而在细胞内驱动化学应激并促使其走向死亡。
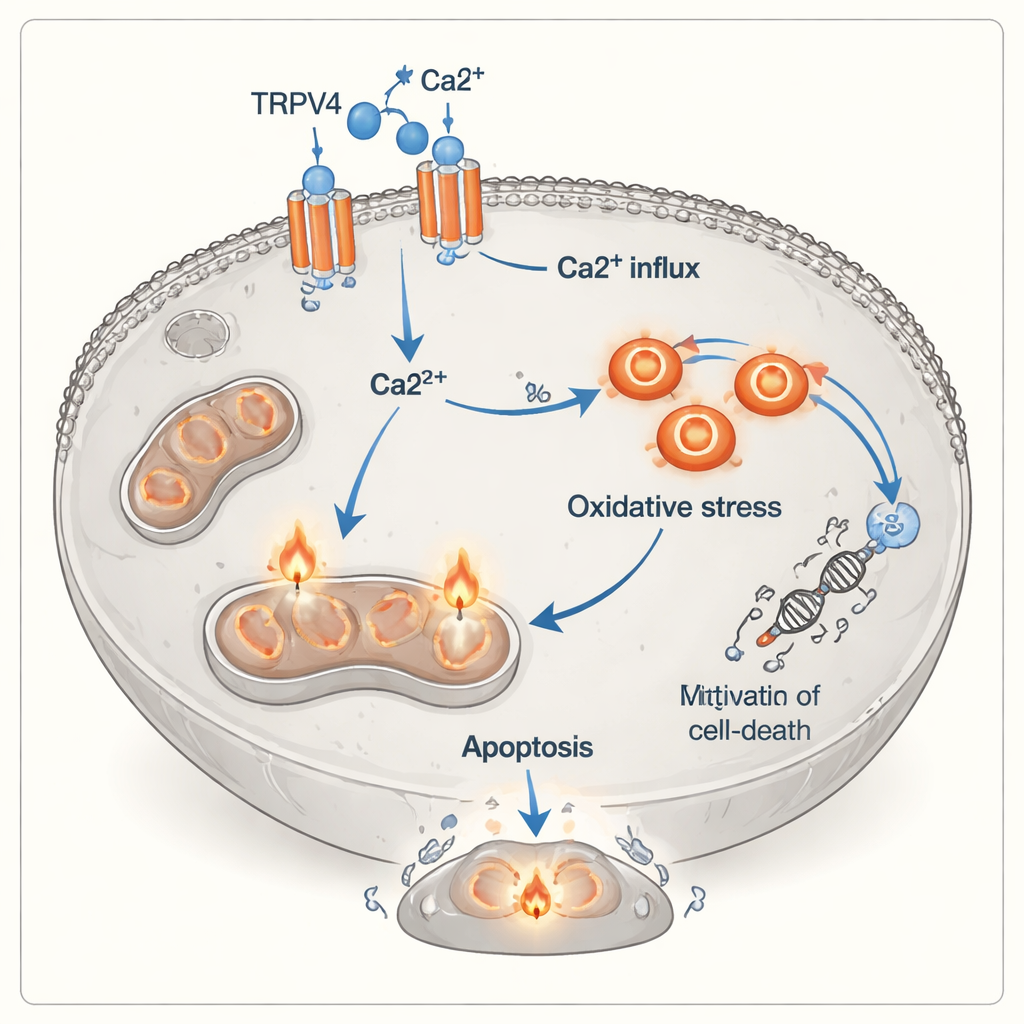
免疫细胞杀伤肿瘤的一个新层面
传统上,杀伤性T细胞通过释放毒性蛋白或触发癌细胞表面的死亡受体来摧毁靶细胞。本研究提示存在另一条更间接的路径:活化T细胞释放的信号——包括炎性分子和紧密的细胞接触——似乎使肺癌细胞更依赖TRPV4,并更易受到钙过载和氧化损伤的影响。在这种观点下,TRPV4像一个敏化开关,将本可促进生长的钙转换为致命信号。尽管这些实验在培养皿中完成且仅使用了单一癌细胞系,但它们突出了免疫攻击、离子通道与肿瘤细胞内部应激机制之间可能的重要桥梁。
这对未来治疗可能意味着什么
对非专业读者而言,结论是:免疫疗法的成功可能不仅取决于增强T细胞的功能,也取决于让癌细胞更容易被杀死。通过针对TRPV4或相关的钙通道,未来医生或许能提升T细胞清除肺肿瘤的能力,或更精细地调整疗法以避免损伤健康组织。这项工作仍处于早期阶段,作者强调需要在动物和更复杂模型中进一步实验。即便如此,发现TRPV4–钙–氧化应激轴为改进基于免疫的肺癌治疗提供了一个有前景的新靶点。
引用: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
关键词: 肺癌免疫疗法, T细胞, 钙信号, TRPV4通道, 氧化应激